Giải SBT Hóa 11 Bài 38: Hệ thống hóa về hidrocacbon
Lời giải sách bài tập Hóa học lớp 11 Bài 38: Hệ thống hóa về hidrocacbon chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong sách bài tập Hóa 11 Bài 38. Mời các bạn đón xem:
Mục lục Giải SBT Hóa 11 Bài 38: Hệ thống hóa về hidrocacbon
Bài 38.1 trang 59 sbt Hóa 11: Trong các nhận xét dưới đây, nhận xét nào sai?
A. Khi đốt cháy hoàn toàn một hiđrocacbon thì sản phẩm thu được chỉ là CO2 và H2O.
C. Khi đốt cháy hoàn toàn một ankan, thì trong sản phẩm thu được, số mol H2O lớn hơn số mol CO2.
Lời giải:
Đáp án B
B sai vì Vì chất mang đốt có thể chứa cả oxi.
Bài 38.2 trang 59 sbt Hóa 11: Chất nào trong 4 chất dưới đây có thể tham gia cả 4 phản ứng: phản ứng cháy trong oxi; phản ứng cộng với brom; phản ứng cộng với H2 (chất xúc tác Ni, nhiệt độ); phản ứng-với dung dịch AgNO3 trong amoniac?
Lời giải:
Đáp án C
Sử dụng phương pháp loại trừ, chọn axetilen vì trong bốn đáp án chỉ có axetilen phản ứng được với AgNO3/ NH3.
Bài 38.3 trang 59 sbt Hóa 11: Cho các chất: stiren, toluen, isopentan, propin, đivinyl, p-xilen, metylpropen. Trong các chất đó, có mấy chất không phản ứng với nước brom?
Lời giải:
Đáp án B
Các chất không phản ứng với nước brom là toluen, isopentan, p – xilen.
Bài 38.4 trang 59 sbt Hóa 11: Tên gọi của chất C6H5Br là
Lời giải:
Đáp án C
C6H5Br: phenyl clorua
Bài 38.5 trang 60 sbt Hóa 11: Hỗn hợp M chứa hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khi đốt cháy hoàn toàn 13,2 g hỗn hợp M thu được 20,72 lít CO2 (đktc).
Hãy xác định công thức phân tử và phần trăm khối lượng từng chất trong hỗn hợp M.
Lời giải:
Số mol CO2 là: = mol
Khối lượng C trong đó là: 9,25.1−1.12= 11,1(g)
Đó cũng là khối lượng C trong 13,2 g hỗn hợp M.
Khối lượng H trong 13,2 g M là: 13,2 - 11,1 = 2,1 (g)
Số mol H2O tạo thành: mol
Vì số mol H2O tạo thành > số mol CO2 nên hai chất trong hỗn hợp M đều là ankan.
![]()
suy ra = 7,4
Công thức phân tử hai chất là C7H16 (x mol) và C8H18 (y mol).
Khối lượng hai chất là: 100x + 114y = 13,2.
Số mol CO2 là: 7x + 8y = 9,25.10-1
Suy ra x = 0,75.10-1; y = 0,5.10-1.
Thành phần phần trăm theo khối lượng:
C7H16 chiếm:
C8H18 chiếm: 100% - 56,8% = 43,2%
Bài 38.6 trang 60 sbt Hóa 11: Hỗn hợp khí A chứa hiđro, một ankan và một anken. Dẫn 15,68 lít A đi qua chất xúc tác Ni nung nóng thì nó biến thành 13,44 lít hỗn hợp khí B. Dẫn B đi qua bình đựng dung dịch brom thì màu của dung dịch nhạt đi và khối lượng bình tăng thêm 5,6 g. Sau phản ứng còn lại 8,96 lít hỗn hợp khí c có tỉ khối đối với hiđro là 20,25. (Biết các thể tích đo ở đktc; các phản ứng đều xảy ra hoàn toàn).
Hãy xác định công thức phân tử và phần trăm thể tích của từng chất trong mỗi hỗn hợp A, B và C.
Lời giải:
Số mol các chất trong A là: mol
Khi A qua chất xúc tác Ni:
Hỗn hợp B chứa 3 chất: ankan ban đầu CnH2n+2, ankan mới tạo ra CmH2m+2 và anken còn dư CmH2m với số mol tổng cộng là : mol
Số mol H2 trong A là: 0,7 - 0,6 = 0,1(mol).
Khi B qua nước brom thì anken bị giữ lại hết:
CmH2m + Br2 → CmH2mBr2
Hỗn hợp C chỉ còn CnH2n+2 và CmH2m+2 với
tổng số moi là mol
Như vậy, 0,2 mol CmH2m có khối lượng 5,6 g,
do đó 1 mol CmH2m có khối lượng 28 (g) suy ra m = 2.
CTPT của anken là C2H4; ankan do chất này tạo ra là C2H6.
Trong hỗn hợp C có 0,1 mol C2H6 và 0,3 mol CnH2n+2
Khối lượng hỗn hợp C là: 20,25.2.0,4 = 16,2 (g)
Trong đó 0,1 mol C2H6 có khối lượng 3 g và 0,3 mol CnH2n+2 có khối lượng là: 16,2 - 3 = 13,2(g).
Khối lương 1 mol CnH2n+2 là 44,0 (g) suy ra n = 3
Hỗn hợp A: C3H8 (42,86%); C2H4 (42,86%); H2 (14,29%).
Hỗn hợp B: C3H8 (50%); C2H6 (16,67%); C2H4 (33,33%).
Hỗn hợp C: C3H8 (75%); C2H6 (25%).
Bài 38.7 trang 60 sbt Hóa 11: Hỗn hợp A chứa 3 ankin với tổng số mol là 0,10 mol. Chia A làm hai phần như nhau. Đốt cháy hoàn toàn phần 1, thu được 2,34 g nước. Phần 2 tác dụng với 250 ml dung dịch AgNO3 0,12M trong NH3 tạo ra 4,55 gam kết tủa.
Lời giải:
Số mol ankin trong mỗi phần = mol
Khi đốt cháy hoàn toàn phần (1):
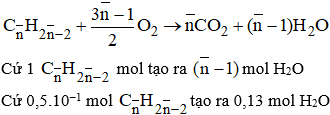
Như vậy trong hỗn hợp A phải có ankin có số nguyên tử cacbon nhỏ hơn 3,6 tức là phải có C2H2 hoặc C3H4.
Nếu có C2H2 thì số mol chất này ở phần 2 là:
n = mol
Khi chất này tác dụng với dung dịch AgNO3 trong NH3:
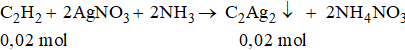
Khối lượng 0,02 mol C2Ag2 là: 0,02. 240 = 4,8 (g) > 4,55 g.
Vậy hỗn hợp A không thể có C2H2 mà phải có C3H4.
Khi chất này tác dụng với dung dịch AgNO3 trong NH3:
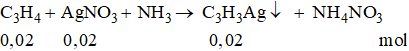
Khối lượng C3H3Ag là 0,02.147 = 2,94 (g).
Số mol AgNO3 đã phản ứng với các ankin là: 0,25.0,12 = 0,03 (mol)
Trong đó lượng AgNO3 tác dụng với C3H4 là 0,02 mol, vậy lượng AgNO3 tác dụng với ankin khác là 0,01 mol.
Trong phần 2, ngoài 0,02 mol C3H4 còn 0,03 mol 2 ankin khác. Vậy mà lượng AgNO3 phản ứng chỉ là 0,01 mol, do đó trong 2 ankin còn lại, chỉ có 1 chất có phản ứng với AgNO3, 1 chất không có phản ứng:
![]()
Khối lượng 0,010 mol CnH2n-3Ag là: 4,55 - 2,94 = 1,61(g).
Khối lượng 1 mol CnH2n−3Ag là 161 g.
14n + 105 = 161 ⇒ n = 4.
Công thức phân tử là C4H6 và CTCT: CH3 - CH2 - C ≡ CH (but-1-in)
Đặt công thức chất ankin chưa biết là Cn′H2n′−2:
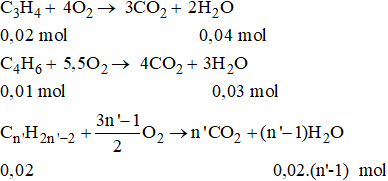
Tổng số mol H2O: 0,04 + 0,03 + 0,02(n' - 1) = 0,13 suy ra n' = 4.
Chất ankin thứ ba có CTPT C4H6 nhưng không tác dụng với AgNO3 nên CTCT là CH3 − C ≡ C − CH3 (but-2-in).
Thành phần về khối lượng:
Propin chiếm: 33,1%; but-1-in: 22,3%; but-2-in: 44,6%.
Bài 38.8 trang 60 sbt Hóa 11: Hỗn hợp X chứa 3 chất A, B, C đều là đồng đẳng của benzen (các khối lượng mol: MA < MB < MC), trong đó A và C có số mol bằng nhau và cách nhau 2 chất trong dãy đồng đẳng.
Để đốt cháy hoàn toàn 48,8 g hỗn hợp X cần dùng vừa hết 153,6 g O2.
1. Xác định công thức phân tử của A, B, C biết rằng chất B không có đồng phân là hợp chất thơm.
2. Hãy tính phần trăm về khối lượng của từng chất trong hỗn hợp X.
Lời giải:
1. Trong dãy đồng đẳng của benzen, chỉ có C6H6 và C7H8 là không có đồng phân là hợp chất thơm.
A và B ở trong dãy đó và MA < MB vậy A là C6H6 và B là C7H8.
Chất C cách chất A hai chất trong dãy đồng đẳng nghĩa là chất C phải hơn chất A ba nguyên tử cacbon. Công thức phân tử chất C là C9H12.
2. Giả sử trong 48,8 g hỗn hợp X có a mol A, b mol B và c mol C; ta có:
78a + 92b + 120c = 48,8 (1)
a = c (2)\
7,5a + 9b + 12c =
Giải hệ (1), (2), (3), tìm được a = c = 0,2; b = 0,1.
Từ đó tính được thành phần phần phần trăm về khối lượng của hỗn hợp X:
C6H6: 31,9%; C7H8: 18,9%; C9H12: 49,2%
Bài 38.9 trang 60 sbt Hóa 11: Hỗn hợp khí A chứa một ankan và một ankin. Lấy 2,24 lít (đktc) A cho sục vào qua dung dịch AgNO3 trong amoniac (lấy dư) thì thể tích khí giảm đi 20% và thu được 2,94 kết tủa. Khi đi ra khỏi dung dịch AgNO3 được đốt cháy hoàn toàn rồi hấp thụ sản phẩm cháy vào dung dịch Ca(OH)2 (dư) tạo ra 16 g kết tủa.
Xác định công thức phân tử và phần trăm về khối lượng của từng chất trong hỗn hợp A.
Lời giải:
Số mol ankin: mol
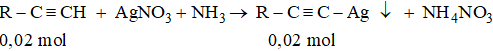
Khối lượng 1 mol R-C≡C-Ag là: gam
R-C≡C-Ag = 147 suy ra R = 147 - 24 - 108 = 15
R là CH3; ankin là CH3-C≡CH (propin)
![]()
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Số mol ankan là 0,08 mol
= 0,16 (mol)
Suy ra n =
Vậy ankan là C2H6
Khối lượng hỗn hợp A là: 0,02.40 + 0,08.30 = 3,2 (g)
Về khối lượng, C3H4 chiếm
và C2H6 chiếm 75%.
Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 39: Dẫn xuất halogen của hidrocacbon
Bài 42: Luyện tập dẫn xuất halogen, ancol, phenol
Xem thêm tài liệu Hóa học lớp 11 hay, chi tiết khác:
Lý thuyết Hệ thống hóa về hiđrocacbon
Trắc nghiệm Hệ thống hóa về hidrocacbon thiên nhiên có đáp án
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
