Giải SBT Hóa 11 Bài 45: Axit cacboxylic
Lời giải sách bài tập Hóa học lớp 11 Bài 45: Axit cacboxylic chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong sách bài tập Hóa 11 Bài 45. Mời các bạn đón xem:
Mục lục Giải SBT Hóa 11 Bài 45: Axit cacboxylic
Bài 45.1 trang 71 sbt Hóa 11: Chất sau có tên là: 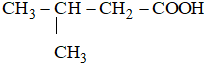
Lời giải:
Đáp án D
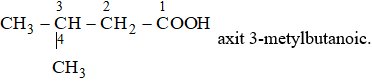
Bài 45.2 trang 71 sbt Hóa 11: Axit propionic có công thức cấu tạo:
Lời giải:
Đáp án B
Axit propionic: CH3-CH2-COOH.
Bài 45.3 trang 71 sbt Hóa 11: Axit propenoic có công thức cấu tạo là
Lời giải:
Đáp án C
Axit propenoic: CH2 = CH - COOH.
Bài 45.4 trang 71 sbt Hóa 11: Bốn chất sau đây đều có phân tử khối là 60. Chất nào có nhiệt độ sôi cao nhất?
Lời giải:
Đáp án C
CH3COOH có nhiệt độ sôi cao nhất, do giữa các phân tử axit có liên kết hiđro bền.
Bài 45.5 trang 71 sbt Hóa 11: Trong 4 chất dưới đây, chất nào dễ tan trong nước nhất?
D. CH3 - CH2 - CH2 - CH2 - COỌH.
Lời giải:
Đáp án C
Do các axit có thể tạo liên kết hiđro với nước nên dễ tan trong nước → loại A, B
Mà độ tan của axit trong nước giảm dần theo chiều tăng của phân tử khối nên chọn CH3 - CH2 - CH2 - COOH.
Bài 45.6 trang 71 sbt Hóa 11: Trong 4 chất dưới đây, chất nào phản ứng được với cả 3 chất: Na, NaOH và NaHCO3?
Lời giải:
Đáp án D
C6H5 – COOH là axit cacboxylic nên phản ứng được với cả Na, NaHCO3 và NaOH.
Bài 45.7 trang 71 sbt Hóa 11: Có bao nhiêu axit cacboxylic có cùng công thức phân thức C5H10O2?
Lời giải:
Đáp án C
Các axit cacboxylic C5H10O2 phải có dạng C4H9-COOH. Có 4 đồng phân gốc -C4H9 vì vậy có 4 axit.
Bài 45.8 trang 72 sbt Hóa 11: Dãy nào sau đây gồm các chất đều có thể điều chế trực tiếp ra axit axetic?
C. CH3COONa, H-CHO, CH3(CH2)2CH3
Lời giải:
Đáp án D
C2H5OH + O2 men→ CH3COOH + H2O
2CH3CHO + O2 xt→ CH3COOH
CH3OH + CO xt→ CH3COOH
Bài 45.9 trang 72 sbt Hóa 11: Cho 1,08 g axit cacboxylic đơn chức tác dụng vừa đủ với dung dịch KOH rồi cô cạn dung dịch, thu được 1,65g muối khan. Axit đó là
Lời giải:
Đáp án C
Đặt axit đơn chức là RCOOH
Cứ 1 mol axit phản ứng thu được 1 mol muối, khối lượng tăng 38 gam
Vậy cứ 1,08 gam axit phản ứng thu được 1,65 gam muối, khối lượng tăng 1,65 – 1,08 = 0,57 gam
⇒naxit=0,5738=0,015 mol
Vậy Maxit = 1,08 : 0,015 = 72 → R + 45 = 72 hay R = 27
Vậy axit là C2H3 – COOH.
Bài 45.10 trang 72 sbt Hóa 11: Người ta có thể điều chế axit axetic xuất phát từ một trong các hiđrocacbon dưới đây (cùng với các chất vô cơ cần thiết):
Lời giải:
1. Từ CH4
2CH4 1500°C→ CH ≡ CH + 3H2
CH≡CH + H2O H2SO4, 80°C → CH3-CHO
2CH3−CHO + O2 xt→ 2CH3COOH
2. Từ C2H4
C2H4 + HOH H+→ CH3−CH2−OH
C2H5OH + O2 enzim→ CH3COOH + H2O
3. Từ C2H2: Hai phản ứng cuối ở phần 1.
CH≡CH + H2O H2SO4, 80°C → CH3-CHO
2CH3−CHO + O2 xt→ 2CH3COOH
4. Từ C4H10:
2CH3−CH2−CH2−CH3 + 5O2 xt→180°C, 50atm 4CH3COOH + 2H2O
Bài 45.11 trang 72 sbt Hóa 11: Dung dịch axit fomic 0,092% có khối lượng riêng xấp xỉ 1 g/ml. Trong dịch đó, chỉ có 5,0% số phân tử axit fomic phân li thành ion.
Lời giải:
Khối lượng của 1 lít (1000 ml) dung dịch axit fomic 0,092% là 1000 g. Trong đó khối lượng của axit fomic là:
1000.0,092100=0,92 (g)
Số mol axit fomic là : 0,9246=0,02 mol
Số mol axit fomic phân li thành ion là: 0,02.5100=0,001 mol
HCOOH ⇄ HCOO− + H+0,001 mol 0,001 mol
Nồng độ [H+] = 0,001 mol/l = 1.10−3 mol/l.
Vậy pH = 3.
Bài 45.12 trang 72 sbt Hóa 11: Hoàn thành các phương trình hoá học dưới đây (nếu phản ứng có xảy ra):
Lời giải:
1. CH3COOH + NaHCO3 → CH3COONa + H2O + CO2
2. Không có phản ứng
3. Không có phản ứng
4. CH3COOH + C6H5CH2OH ⇄ CH3COOCH2C6H5 + H2O
5. Không có phản ứng
6. 2CH3COONa + H2SO4 → 2CH3COOH + Na2SO4
7. 2CH3COOH + CuO → (CH3COO)2Cu + H2O
8. Không có phản ứng
Bài 45.13 trang 72 sbt Hóa 11: Chất A là một axit no, đơn chức, mạch hở. Để đốt cháy hoàn toàn 2,55 g A phải dùng vừa hết 3,64 lít O2 (đktc).
Hãy xác định công thức phân tử, công thức cấu tạo và tên của chất A.
Lời giải:
![]()
Theo phương trình:
(14n + 32)g axit tác dụng với 3n−22 mol O2.
Theo đầu bài:
2,55 g axit tác dụng với 3,6422,4=0,1625 mol O2.
14n+322,55=3n−22.0 suy ra n = 5
CTPT của axit là C5H10O2.
Bài 45.14 trang 72 sbt Hóa 11: Chất A là một axit cacboxylic đơn chức, dẫn xuất của anken. Khi đốt cháy hoàn toàn 0,9 g A, người ta thấy trong sản phẩm tạo thành, khối lượng CO2 lớn hơn khối lượng H2O 1,2 g.
Lời giải:
Chất A là axit cacboxylic đơn chất, dẫn xuất anken nên có công thức tổng quát: CnH2n -2O2
![]()
Theo phương trình: Nếu đốt (14n + 30) g A, khối lượng CO2 nhiều hơn khối lượng H2O (26n + 1,08) g.
Theo đầu bài: Nếu đốt 0,9 g A, khối lượng CO2 nhiều hơn khối lượng H2O là 1,2 g.
Vậy suy ra n = 3
CTPT của axit là C3H4O
CTCT: CH2 = CH - COOH (Axit propenoic).
Bài 45.15 trang 73 sbt Hóa 11: Dung dịch X có chứa đồng thời hai axit cacboxylic no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng.
Hãy xác định công thức phân tử và nồng độ mol của từng axit trong dung dịch X.
Lời giải:
Đặt công thức chung của 2 axit là
Phần 1:
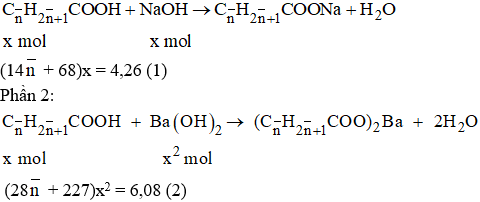
Từ (1) và (2) tìm được n = 2,75; x = 0,04.
Axit thứ nhất là C2H5COOH (C3H8O2) có số mol là a mol.
Axit thứ hai là C3H7COOH (C4H8O2) có số mol là b mol.
Suy ra a = 0,01, b = 0,03
CM của C2H5COOH là: (mol/l)
CM của C3H7COOH là: (mol/l)
Bài 45.16 trang 73 sbt Hóa 11: Hỗn hợp M gồm axit cacboxylic no, đơn chức, mạch hở A và anol no đơn chức mạch hở B. Hai chất A và B có cùng số nguyên tử cacbon.
Lời giải:
Chất A có CTPT là CnH2nO2, CTCT là Cn-1H2n-1COOH Chất B có CTPT là CnH2n+2O, CTCT là CnH2n+1OH.
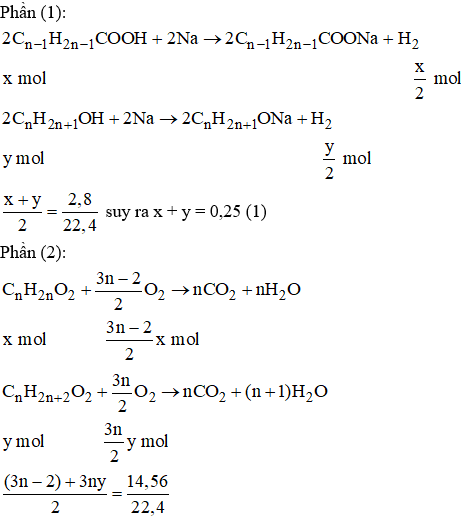
Suy ra (3n - 2)x + 3ny = 1,3 (2)
Khối lượng mỗi phần: (14n + 32)x + (14n + 18)y = 12,9 (3)
Từ hệ các phương trình (1), (2), (3), tìm được n = 2; x = 0,1; y = 0,15.
Chất A: C2H4O2 hay CH3COOH (axit axetic) chiếm:
Khối lượng hỗn hợp.
Chất B: C2H6O hay CH3-CH2-OH (ancol etylic) chiếm: 100% - 46,5% = 53,5% khối lượng hỗn hợp.
Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 42: Luyện tập dẫn xuất halogen, ancol, phenol
Bài 46: Luyện tập anđehit - xeton - axit cacboxylic
Xem thêm tài liệu Hóa học lớp 11 hay, chi tiết khác:
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
