Giải SBT Hóa 11 Bài 46: Luyện tập anđehit - xeton - axit cacboxylic
Lời giải sách bài tập Hóa học lớp 11 Bài 46: Luyện tập anđehit - xeton - axit cacboxylic chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong sách bài tập Hóa 11 Bài 46. Mời các bạn đón xem:
Mục lục Giải SBT Hóa 11 Bài 46: Luyện tập anđehit - xeton - axit cacboxylic
Bài 46.1 trang 73 sbt Hóa 11: Trong các nhận xét dưới đây, nhận xét nào không đúng?
A. Tất cả các anđehit no, đơn chức, mạch hở đều có các đồng phân thuộc chức xeton và chức ancol.
B. Tất cả các xeton no đơn chức, mạch hở đều có các đồng phân thuộc chức anđehit và chức ancol.
D. Tất cả các ancol đơn chức, mạch vòng no đều có các đồng phân thuộc chức anđehit và chức xeton.
Lời giải:
Đáp án A
Ví dụ HCHO, CH3CHO không có đồng phân thuộc chức ancol và chức xeton.
Bài 46.2 trang 73 sbt Hóa 11: Chất X là một anđehit mạch hở chứa a nhóm chức anđehit và b liên kết 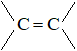 ở gốc hiđrocacbon. Công thức phân tử của chất X có dạng là?
ở gốc hiđrocacbon. Công thức phân tử của chất X có dạng là?
Lời giải:
Đáp án D
Số liên kết pi trong X là a + b
Vậy công thức phân tử của X có dạng: CnH2n+2−2a−2bOa
Bài 46.3 trang 74 sbt Hóa 11: Axit ađipic có công thức là HOOC[CH2]4COOH. Tên thay thế của chất này là
Lời giải:
Đáp án D
Axit ađipic còn có tên gọi là axit hexan-1,6-đioic
Bài 46.4 trang 74 sbt Hóa 11: Có bao nhiêu axit cacboxylic thơm (có vòng benzen) ứng với công thức phân tử C8H8O2?
Lời giải:
Đáp án B
Có 3 chất CH3-C6H4-COOH (-o, -m, -p) và 1 chất C6H5-CH2-COOH
Bài 46.5 trang 74 sbt Hóa 11: Độ linh động của nguyên tử H trong nhóm OH của các chất C2H5OH, C6H5OH, HCOOH và CH3COOH tăng dần theo trật tự:
A. C2H5OH < C6H5OH < HCOOH < CH3COOH
B. CH3COOH < HCOOH < C6H5OH < C2H5OH.
C. C2H5OH < C6H5OH < CH3COOH < HCOOH.
D. C6H5OH < C2H5OH < CH3COOH < HCOOH.
Lời giải:
Đáp án C
Độ linh động: ancol < phenol < axit
Với các axit no có M càng lớn độ linh động của nguyên tử H trong OH càng giảm.
Bài 46.6 trang 74 sbt Hóa 11: Trong các chất dưới đây, chất nào không có phản ứng hóa học với cả 3 chất: Na, NaOH, NaHCO3?
Lời giải:
Đáp án C
Anđehit không phản ứng được với Na, NaOH, NaHCO3.
Bài 46.7 trang 74 sbt Hóa 11: Ghép tên chất với công thức cấu tạo cho phù hợp.
Lời giải:
1 – D
2 – F
3 – A
4 – B
5 – E
6 - C.
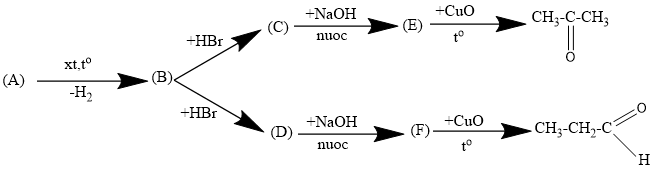
Bài 46.8 trang 75 sbt Hóa 11: Viết phương trình hóa học thực hiện các biến đổi dưới đây. Các chất hữu cơ được viết dưới dạng công thức cấu tạo và ghi tên.
Lời giải:
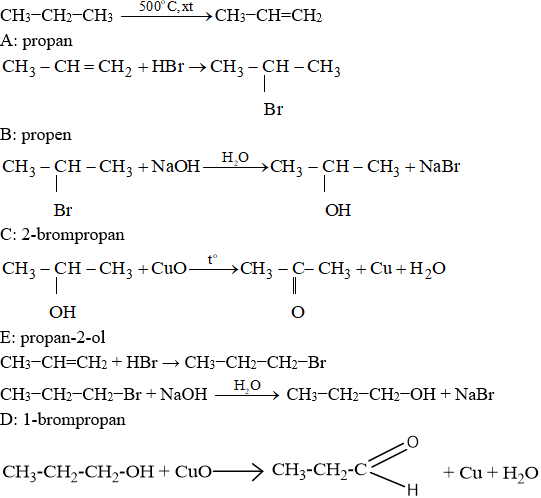
Bài 46.9 trang 75 sbt Hóa 11: Anđehit axetic có thể khử được đồng (II) hiđroxit tạo ra kết tủa đồng (I) oxit có màu đỏ gạch.
Hãy viết phương trình hóa học biểu diễn phản ứng nói trên.
Lời giải:
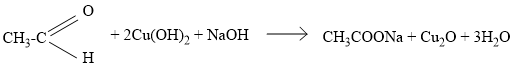
Bài 46.10 trang 75 sbt Hóa 11: Chất hữu cơ A chỉ chứa cacbon, hiđro, oxi và chỉ có một loại nhóm chức.
Cho 0,9 g chất A tác dụng với lượng dư dung dịch AgNO3 trong amoniac, thu được 5,4 g Ag.
Xác định công thức và tên chất A.
Lời giải:
A tác dụng với dung dịch AgNO3 trong amoniac tạo ra Ag; vậy A có chức anđehit.
0,2 mol anđehit kết hợp với hiđro phải tạo ra 0,2 mol ancol B có công thức R(CH2OH)x
![]()
Theo phương trình 1 mol B tạo ra mol H2
Theo đầu bài 0,2 mol B tạo ra 0,2 mol H2
suy ra x = 2
Vậy B là ancol hai chức và A là anđehit hai chức.
R(CHO)2 + 4AgNO3 + 6NH3 + 2H2O → R(COONH4)2 + 4NH4NO3 + 4Ag↓
= mol
Khối lượng 1 mol A = gam
R(CHO)2 = 72
Suy ra R = 72 - 2.29 = 14. Vậy R là CH2
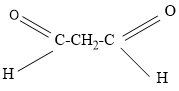
(propanđial)
Bài 46.11 trang 75 sbt Hóa 11: Chất hữu cơ X chỉ có chức anđehit. Biết 0,1 mol X có thể kết hợp với 4,48 lít H2 (lấy ở đktc) khi có chất xúc tác Ni và nhiệt độ thích hợp.
Mặt khác, nếu cho 7 g X tác dụng với lượng dư dung dịch AgNO3 trong amoniac, thu được 27 g Ag.
Hãy xác định công thức phân tử, công thức cấu tạo và tên của chất X.
Lời giải:
Theo đầu bài 0,1 mol anđehit X kết hợp được với 0,2 mol H2. Vậy X có thể là:
- Anđehit no hai chức CnH2n (CHO)2 hoặc
- Anđehit đơn chức có 1 liên kết đôi ở gốc CnH2n-1CHO.
1. Nếu X là CnH2n(CHO)2 thì:
CnH2n(CHO)2 + 4AgNO3 + 6NH3 + 2H2O → CnH2n(COONH4)2 + 4NH4NO3 + 4Ag↓
mol
g/mol
MCnH2n(CHO)2 = 112 (g/mol) hay 14n + 2.29 = 112 suy ra n = 3,86 (loại)
2. Nếu X là CnH2n-1CHO:
CnH2n-1CHO + 2AgNO3 + 3NH3 + H2O → CnH2n-1COONH4 + 2NH4NO3 + 2Ag↓
mol
g/mol
MCnH2n−1CHO = 56 (g/mol) suy ra 14n + 28 = 56 suy ra n = 2
CTPT: C3H4O
CTCT: CH2 = CH-CHO propenal.
Bài 46.12 trang 75 sbt Hóa 11: Hỗn hợp M chứa ba hợp chất hữu cơ X, Y và Z. Hai chất X và Y kế tiếp nhau trong một dãy đồng đẳng (MY < MX). Chất Z là đồng phân của chất Y.
Nếu cho 48g M tác dụng với Na (lấy dư), thu được 1,68 lít H2 (đktc).
Lời giải:
Số mol 3 chất trong 3,20 g hỗn hợp M: mol
Số mol 3 chất trong 16 g M:
Khi đốt hỗn hợp M ta chỉ thu được CO2 và H2O.
Vậy, các chất trong hỗn hợp đó chỉ có thể chứa C, H và O.
Đặt công thức chất X là CxHyOz thì chất Y là Cx+1Hy+2Oz. Chất Z là đồng phân của Y nên công thức phân tử giống chất Y.
Giả sử trong 16 g hỗn hợp M có a mol chất X và b mol hai chất Y và Z:
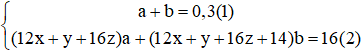
Khi đốt 16 g M thì tổng khối lượng CO2 và H2O thu được bằng tổng khối lượng của M và O2 và bằng:
Mặt khác,
44n + 18n = 49,6 suy ra n = 0,8
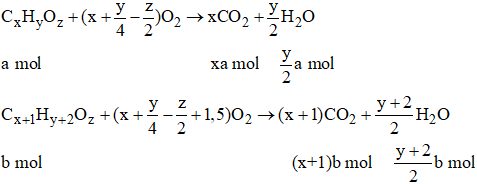
Số mol CO2 là: xa + (x + 1)b = 0,8 (mol) (3)
Số mol H2O là: mol
do đó: ya + (y + 2)b = 1,6 (4)
Giải hệ phương trình:
Biến đổi (3) ta có x(a + b) + b = 0,8
Vì a + b = 0,3 nên b = 0,8 - 0,3x
Vì 0 < b < 0,3 nên 0 < 0,8 - 0,3x < 0,3 suy ra 1,66 < x < 2,66
x nguyên suy ra x = 2 suy ra b = 0,8 - 0,3.2 = 0,2
suy ra a = 0,3 - 0,2 = 0,1
Thay giá trị của a và b vào (4), tìm được y = 4.
Thay giá trị của a, b, x và y vào (2), tìm được z = 1.
Vậy chất X có CTPT là C2H4O, hai chất Y và z có cùng CTPT là C3H6O.
Chất X chỉ có thể có CTCT là 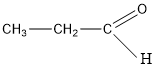 (etanal) vì chất CH2 = CH - OH không bền và chuyển ngay thành etanal.
(etanal) vì chất CH2 = CH - OH không bền và chuyển ngay thành etanal.
Chất Y là đồng đẳng của X nên CTCT là 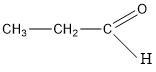 (propanal).
(propanal).
Hỗn hợp M có phản ứng với Na. Vậy, chất Z phải là ancol CH2 = CH - CH2 - OH (propenol):
2CH2 = CH - CH2 - OH + 2Na → 2CH2 = CH - CH2 - ONa + H2↑
Số mol Z trong 48 g M là: 2. số mol H2 = 0,15 (mol).
Số mol Z trong 16 g M là:
Số mol Y trong 16 g M là: 0,2 - 0,05 = 0,15 (mol).
Thành phần khối lượng của hỗn hợp M:
Chất X chiếm:
Chất Y chiếm:
Chất Z chiếm:
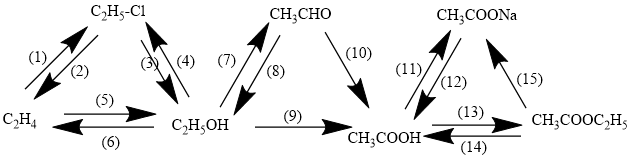
Bài 46.13 trang 76 sbt Hóa 11: Viết phương trình hoá học thưc hiện các biến hoá dưới đây (mỗi mũi tên là một phản ứng):
Lời giải:
(1) CH2=CH2 + HCl CH3−CH2−Cl
(2) C2H5Cl + NaOH CH2=CH2 + NaCl + H2O
(3) C2H5Cl + NaOH C2H5OH + NaCl
(4) C2H5OH + HCl C2H5Cl + H2O
(5) C2H4 + H2O C2H5OH
(6) C2H5OH C2H4 + H2O
(7) C2H5OH + CuO CH3CHO + Cu + H2O
(8) CH3CHO + H2 C2H5OH
(9) C2H5OH + O2 CH3COOH + H2O
(10) 2CH3CHO + H2 2CH3COOH
(11) CH3COOH + NaOH → CH3COONa + H2O
(12) 2CH3COONa + H2SO4 → 2CH3COOH + Na2SO4
(13) CH3COOH + C2H5OH CH3COOC2H5 + H2O
(14) CH3COOC2H5 + H2O CH3COOH + C2H5OH
(15) CH3COOC2H5 + NaOH CH3COONa + C2H5OH
Bài 46.14 trang 76 sbt Hóa 11: Có 4 bình (không ghi nhãn), mỗi bình đựng 1 trong các dung dịch (dung môi là nước): propan-1-ol, propanal, axit propanoic và axit propenoic.
Lời giải:
Cho 4 dung dịch thử phản ứng với dung dịch AgNO3 trong amoniac; dung dịch nào có phản ứng tráng bạc là dung dịch propanal (3 dung dịch còn lại không phản ứng):
C2H5CHO + 2AgNO3 + 3NH3 + H2O → C2H5COONH4 + 2NH4NO3 + 2Ag↓
Thử 3 dung dịch còn lại với nước brom, chỉ có axit propenoic làm mất màu nước brom:
CH2 = CH - COOH + Br2 → CH2Br - CHBr - COOH
Thử 2 dung dịch còn lại với CaCO3, chỉ có axit propanoic hoà tan CaCO3 tạo ra chất khí:
2C2H5COOH + CaCO3 → (C2H5COO)2Ca + H2O + CO2↑
Dung dịch cuối cùng là dung dịch propan-1-ol.
Bài 46.15 trang 76 sbt Hóa 11: Chất A là một axit cacboxylic no, mạch hở. Để trung hoà 50 g dung dịch A có nồng độ 5,20% cần dùng vừa đúng 50 ml dung dịch NaOH 1 M. Mặt khác, nếu đốt cháy hoàn toàn 15,6 g chất A, thu được 10,080 lít CO2 (đktc).
Hãy xác định công thức phân tử và công thức cấu tạo của A.
Vận dụng quy tắc đọc tên thay thế của axit, hãy cho biết tên của A.
Lời giải:
A là axit no, mạch hở, chưa rõ là đơn chức hay đa chức
Vậy chất A là CnH2n+2-x(COOH)x; CTPT là Cn+xH2n+2O2x
Khối lượng mol A là (14n + 44x + 2) gam.
Khối lượng A trong 50 g dung dịch 5,2% là (g)
Số mol NaOH trong 50 ml dung dịch 1 M là: mol
CnH2n+2-x(COOH)x + xNaOH → CnH2n+2-x(COONa)x +xH2O
Theo phương trình: cứ (14n + 44x + 2) g A tác dụng với x mol NaOH
Theo đầu bài: cứ 2,6 g A tác dụng với 0,05 mol NaOH
![]()
Theo phương trình: Khi đốt (14n + 44x + 2) g A thu được (n + x) mol CO2
Theo đầu bài:
Khi đốt 15,6 g A thu được (mol) CO2
Từ (1) và (2), tìm được n = 1, x = 2 CTPT của A: C3H4O4
CTCT của A: HOOC - CH2 - COOH (Axit propanđioic)
Bài 46.16 trang 76 sbt Hóa 11: Hỗn hợp M chứa ancol no A và axit cacboxylic đơn chức B, cả hai đều mạch hở. Tổng số mol 2 chất trong hỗn hợp M là 0,5 mol. Để đốt cháy hoàn toàn hỗn hợp M cần dùng vừa hết 30,24 lít O2. Sản phẩm cháy gồm có 23,4 g H2O và 26,88 lít CO2. Các thể tích đo ở đktc.
Lời giải:
Khi đốt 0,5 mol hỗn hơp M, số mol CO2 thu đươc là: mol
Nếu đốt 1 mol hỗn hợp M, số mol CO2 thu được sẽ là 2,4 (mol).
Như vậy chất A và chất B có chứa trung bình 2,40 nguyên tử cacbon, chất A lại kém chất B 1 nguyên tử cacbon. Vậy, A có 2 và B có 3 nguyên tử cacbon.
A là ancol no có 2 cacbon: C2H6-x(OH)x hay C2H6Ox
B là axit đơn chức có 3 cacbon: C3HyO2.
Đặt số mol A là a, số mol B là b: a + b = 0,5 (1)
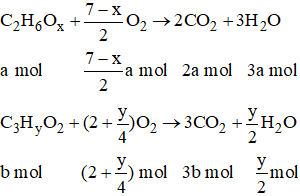
Số mol O2 là: (3,5 - 0,5x)a + (2 + 0,25y)b = 1,35 (mol) (2)
Số mol CO2 là: 2a + 3b = 1,2 (mol) (3)
Số mol CO2 là: mol (4)
Giải hệ phương trình đại số tìm được: a = 0,3; b = 0,2; x = 2; y = 4.
Chất A: C2H6O2 hay etanđiol (hay etylenglicol)
Chiếm khối lượng M.
Chất B: C3H4O2 hay CH2 = CH - COOH, axit propenoic chiếm 43,64% khối lượng M.
Bài 46.17 trang 76 sbt Hóa 11: Hỗn hợp M chứa 3 axit cacboxylic đơn chức mạch hở, trong đó hai chất là axit no kế tiếp nhau trong dãy đồng đẳng và một chất là axit không no có một liên kết kép ở gốc hiđrocacbon.
Lời giải:
Các axit đơn chức tác dụng với NaOH như sau:
RCOOH + NaOH → RCOONa + H2O
Cứ 1 mol RCOOH biến thành 1 mol RCOONa thì khối lượng sẽ tăng thêm là:
23 - 1 = 22 (g).
Khi 29,6 g M biến thành hỗn hợp muối, khối lượng đã tăng thêm là:
40,6 - 29,6= 11 (g).
Vậy số mol 3 axit trong 29,60 g M là : mol
Khối lượng trung bình của 1 mol axit trong hỗn hợp là: (g)
Vậy trong hỗn hợp M phải có axit có phân tử khối nhỏ hơn 59,2. Chất đó chỉ có thể là H-COOH. Nhưng M có 2 axit no kế tiếp nhau trong dãy đồng đẳng nên đã có HCOOH thì phải có CH3COOH.
Giả sử trong 8,88 gam M có x mol HCOOH, Y mol CH3COOH và z mol CnH2n+1COOH
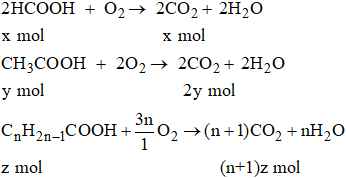
x + 2y + (n + 1)z = 0,3 (3)
Cách giải hệ phương trình:
Nhân 2 vế của phương trình (3) với 14 ta có
14x + 28y + (14n + 14)z = 4,2 (3’)
Lấy (2) trừ đi (3'):
32x + 32y + 30z = 4 68 (2')
Nhân (1) với 30 ta có:
30x + 30y + 30z = 4,50 (1')
Lấy (2') trừ đi (1'):
2x + 2y = 0,18 suy ra x + y = 0,09 suy ra z = 0,15 - 0,09 = 0,06
Thay các giá trị vừa tìm được vào phương trình (3), ta có:
0,09 + y + 0,06(n + 1) = 0,3
y = 0,15 - 0,06n
0 < y < 0,09 suy ra 0 < 0,15 - 0,06n < 0,09
1 < n < 2,5
Suy ra n = 2; y = 0,15 - 0,06.2 = 0,03 suy ra x = 0,06.
Thành phần khối lượng của hỗn hợp:
H-COOH(CH2O2) axit metanoic là:
CH3-COOH(C2H4O2) axit etanoic là:
CH2 = CH-COOH(C3H4O2) axit propenoic là:
Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 42: Luyện tập dẫn xuất halogen, ancol, phenol
Xem thêm tài liệu Hóa học lớp 11 hay, chi tiết khác:
Lý thuyết Luyện tập: Anđehit – Xeton – Axit cacboxylic
Trắc nghiệm Luyện tập: Anđehit, xeton và axit cacboxylic có đáp án
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11