Một bình kín dung tích 8,4 lít có chứa 4,96 g 02 và 1,3 gam hỗn hợp khí A
Với giải bài 33.7 trang 52 sbt Hóa học lớp 11 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 11. Mời các bạn đón xem:
Giải SBT Hoá 11 Bài 33: Luyện tập ankin
Bài 33.7 trang 52 Sách bài tập Hóa học 11: Một bình kín dung tích 8,4 lít có chứa 4,96 g 02 và 1,3 gam hỗn hợp khí A gồm 2 hiđrocacbon. Nhiệt độ trong bình t1 = 0oC và áp suất trong bình p1 = 0,5 atm.
Bật tia lửa điện trong bình kín đó thì hỗn hợp A cháy hoàn toàn. Sau phản ứng, nhiệt độ trong bình là t2 = 136,5oC và áp suất là p2 atm. Dẫn các chất trong bình sau phản ứng đi qua bình thứ nhất đựng H2SO4 đặc, sau đó qua bình 2 đựng dung dịch NaOH (có dư) thì khối lượng bình thứ hai tăng 4,18 g.
1. Tính p2, biết rằng thể tích bình không đổi.
2. Xác định công thức phân tử và phần trăm theo thể tích của từng chất trong hỗn hợp A nếu biết thêm rằng trong hỗn hợp đó có một chất là anken và một chất là ankin.
Lời giải:
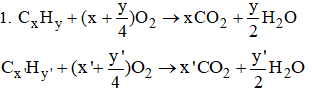
H2SO4 + nH2O → H2SO4.nH2O
2NaOH + CO2 → Na2CO3 + H2O
Số mol CO2 là: mol
Khối lượng C trong hỗn hợp A là: 0,095.12 = 1,14 (g).
Khối lượng H trong hỗn hợp A là: 1,3 - 1,14 = 0,16 (g).
Số mol H2O sau phản ứng là: mol
Để tạo ra 0,095 mol CO2 cần 0,095 mol O2;
Để tạo ra 0,08 mol H2O cần 0,04 (mol) O2.
Số mol O2 đã tham gia phản ứng là: 0,095 + 0,04 = 0,135 (mol).
Số mol O2 ban đầu là: mol
Số mol O2 còn dư là: 0,155 - 0,135 = 0,02 (mol).
Số mol 3 chất trong bình sau phản ứng:
0,095 + 0,08 + 0,02 = 0,195 (mol).
Nếu ở đktc thì Vo = 0,195.22,4 = 4,37 (lít).
Thực tế V2 = 8,4 lít
Suy ra
= 0,78 atm
2. Đổi thể tích hỗn hợp khí trước phản ứng về đktc:
Số mol khí trước phản ứng: mol
Số mol 2 hiđrocacbon: 0,1875 - 0,155 = 0,0325 (mol).
Đặt lượng CnH2n là a mol, lượng CmH2m-2 là b mol,
ta có a + b = 0,0325.
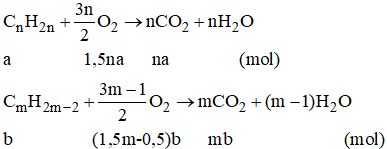
Số mol O2: l,5na + (l,5m - 0,5)b = 0,135 (2)
Số mol CO2: na + mb = 0,095 (3)
Từ (2) và (3), tìm được b = 0,015 ⇒ a = 0,0175
Thay các giá trị của a và b vào (3), ta có:
1,75.10−2n + 1,5.10−2m = 9,5.10−2
7n + 6m = 38
Nếu n = 2 thì
Nếu n = 3 thì (loại)
Nếu n > 3 thì m < 2 (loại).
% về thể tích của C2H4:
% về thể tích của C4H6 là 46,2%
Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 33.1 trang 51 sbt Hóa 11: Công thức phân tử nào cho dưới đây phù hợp với penten?...
Bài 33.2 trang 51 sbt Hóa 11: Trong 4 chất sau, chất nào có nhiệt độ sôi cao nhất là?...
Bài 33.3 trang 51 sbt Hóa 11: Cho propin tác dụng với HCl theo hai gian đoạn liên tiếp thì sản phẩm chính thu được là:...
Bài 33.8 trang 52 sbt Hóa 11: Trình bày phương pháp hoá học để phân biệt các hiđrocacbon sau:...
Bài 33.9 trang 52 sbt Hóa 11: Cho biết phương pháp làm sạch chất khí:...
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
