Lý thuyết Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch– Hóa lớp 12 Chân trời sáng tạo
Với lý thuyết Hóa lớp 12 Bài 20: Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch chi tiết, ngắn gọn và bài tập tự luyện có lời giải chi tiết sách Chân trời sáng tạo sẽ giúp học sinh nắm vững kiến thức trọng tâm để học tốt môn Hóa 12.
Lý thuyết Hóa 12 Bài 20: Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch - Chân trời sáng tạo
A. Lý thuyết Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
1. Thành phần và dạng hình học của phức chất
- Trong phức chất có nguyên tử trung tâm (còn gọi là nhân trung tâm) và phối tử. Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận, trong đó phối tử cho cặp electron chưa liên kết vào orbital trống của nguyên tử trung tâm.
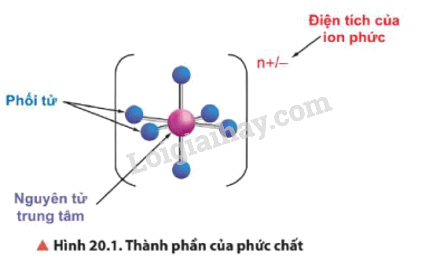
Ví dụ: phức chất [Cr(NH3)6]3+ có nguyên tử trung tâm là Cr3+ và phối tử là NH3
- Dạng hình học của phức chất phổ biến là tứ diện, vuông phẳng và bát diện
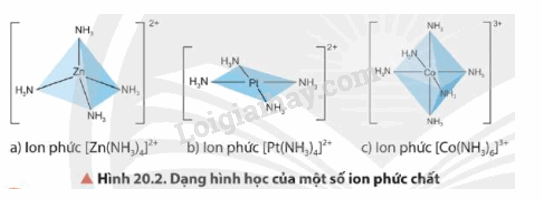
2. Sự hình thành phức chất trong dung dịch
- Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:;
Mn+(aq) + m H2O(l) → [M(OH2)m]n+(aq)
Với: n là giá trị điện tích của cation kim loại M
m là số phối tử H2O
[M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
- Phản ứng thay thế phối tử trong phức chất
Ở những điều kiện phù hợp, các anion và phân tử như OH-, X- (halide), NH3,…. Có thể thay thế được một, một số hoặc tất cả các phối tử trong phức chất
Ví dụ: [Cr(OH2)6]3+(aq) + 6OH-(aq) → [Cr(OH)6]3-(aq) + 6H2O(l)
- Dấu hiệu của phản ứng tạo phức chất trong dung dịch
Các phản ứng tạo phức chất thường có một số dấu hiệu dễ quan sát như sự biến đổi máu sắc, sự hòa tan, sự kết tủa. Trong các dấu hiệu trên, sự biến đổi màu sắc là phổ biến hơn cả
- Phản ứng thay thế phối tử trong phức chất
Ở những điều kiện phù hợp, các anion và phân tử như OH-, X- (halide), NH3,…. Có thể thay thế được một, một số hoặc tất cả các phối tử trong phức chất
Ví dụ: [Cr(OH2)6]3+(aq) + 6OH-(aq) → [Cr(OH)6]3-(aq) + 6H2O(l)
3. Một số ứng dụng của phức chất
- Phức chất có nhiều ứng dụng trong lĩnh vực, như y họcc, dược hóa, hóa học,…
- Phức chất có ý nghĩa to lớn trong ngành y học và dược học. Nhiều dẫn xuất có hoạt tính sinh học trên cơ thể người là phức chất của các kim loại như Cu, Zn, Co, Pt, Au,… Đây là cơ sở cho việc sản xuất thuốc chữa bệnh.
B. Trắc nghiệm Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
Đang cập nhật …
C. Sơ đồ tư duy Sơ lược về phức chất và sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
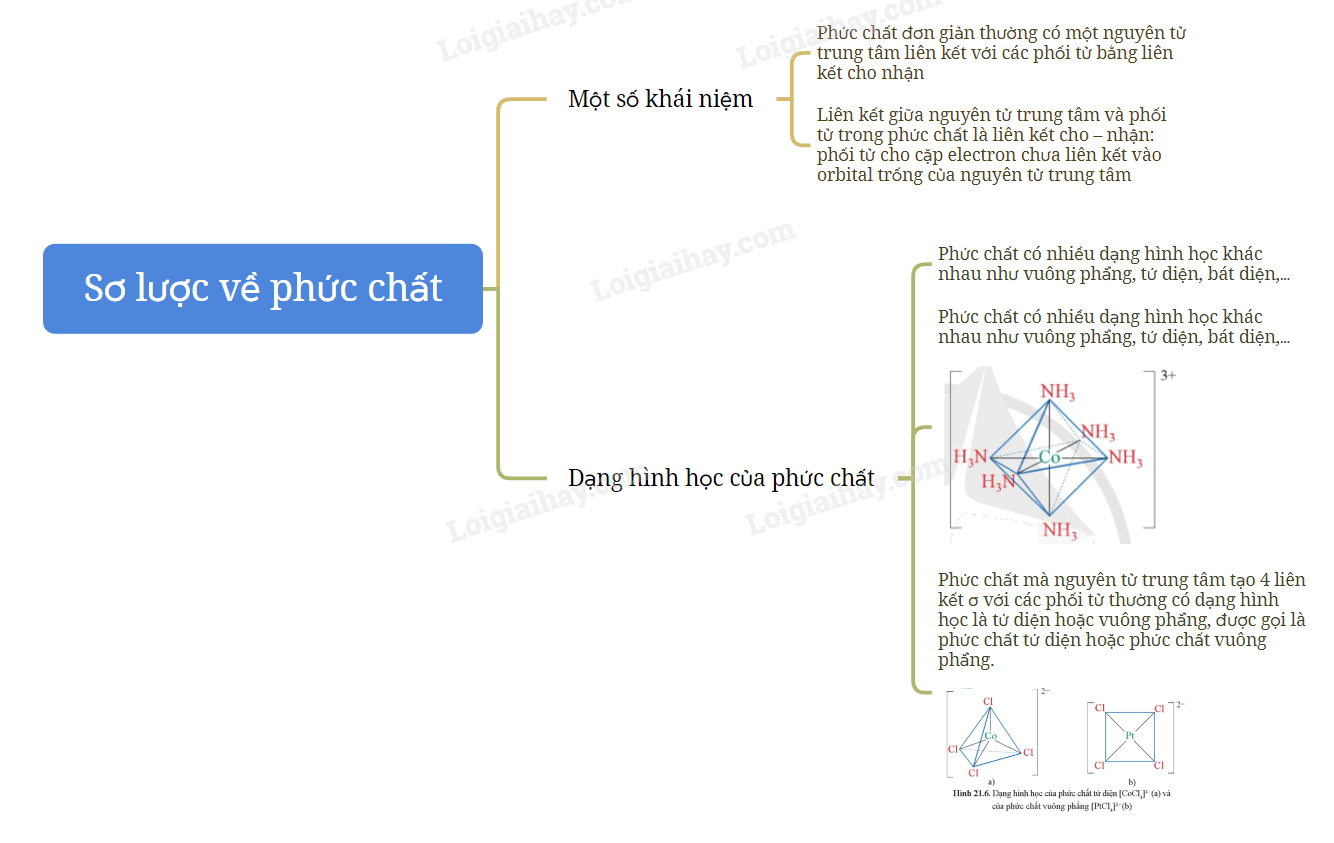
Xem thêm các chương trình khác:
- Soạn văn 12 Chân trời sáng tạo (hay nhất)
- Văn mẫu 12 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 12 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn 12 - Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn 12 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn 12 – Chân trời sáng tạo
- Giải sgk Toán 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Toán 12 – Chân trời sáng tạo
- Lý thuyết Toán 12 – Chân trời sáng tạo
- Giải sbt Toán 12 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 12 - Friends Global
- Trọn bộ Từ vựng Tiếng Anh lớp 12 Friends Global đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh lớp 12 Friends Global đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Friends Global
- Giải sgk Lịch sử 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Lịch sử 12 – Chân trời sáng tạo
- Giải sbt Lịch sử 12 – Chân trời sáng tạo
- Giải sgk Địa lí 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Địa lí 12 – Chân trời sáng tạo
- Giải sbt Địa lí 12 – Chân trời sáng tạo
- Giải sgk Tin học 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Tin học 12 – Chân trời sáng tạo
- Giải sbt Tin học 12 – Chân trời sáng tạo
- Lý thuyết Tin học 12 - Chân trời sáng tạo
- Giải sgk Công nghệ 12 – Chân trời sáng tạo
- Giải sgk Kinh tế pháp luật 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Chân trời sáng tạo
- Giải sbt Kinh tế pháp luật 12 – Chân trời sáng tạo
- Giải sgk Giáo dục quốc phòng 12 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 12 – Chân trời sáng tạo
- Giải sgk Vật lí 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Vật lí 12 – Chân trời sáng tạo
- Lý thuyết Vật lí 12 – Chân trời sáng tạo
- Giải sbt Vật lí 12 – Chân trời sáng tạo
- Giải sgk Sinh học 12 – Chân trời sáng tạo
- Giải Chuyên đề học tập Sinh học 12 – Chân trời sáng tạo
- Lý thuyết Sinh học 12 – Chân trời sáng tạo
- Giải sbt Sinh học 12 – Chân trời sáng tạo
