Lý thuyết KHTN 8 Bài 3 (Kết nối tri thức): Mol và tỉ khối chất khí
Tóm tắt lý thuyết Khoa học tự nhiên lớp 8 Bài 3: Mol và tỉ khối chất khí ngắn gọn, chi tiết sách Kết nối tri thức sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt KHTN 8.
Lý thuyết KHTN 8 Bài 3: Mol và tỉ khối chất khí
A. Kiến thức trọng tâm KHTN 8 Bài 3: Mol và tỉ khối chất khí
- Khái niệm: Trong khoa học, khối lượng nguyên tử carbon được quy ước là đơn vị khối lượng 1/12 nguyên tử (amu).
- Khối lượng 1 nguyên tử carbon là 12 amu và khối lượng này rất nhỏ.
- Số Avogadro (Ng) là số nguyên tử trong 12 gam carbon và có giá trị là 6,022x10²³.

- (M) của một chất là khối lượng của NA nguyên tử hoặc phân tử chất đó tính theo đơn vị gam.
- Khối lượng mol (g/mol) và khối lượng nguyên tử hoặc phân tử của chất đó (amu) bằng nhau về trị số, khác về đơn vị đo.
- Thể tích mol của chất khí là thể tích chiếm bởi NA phân tử của chất khi đó và ở cùng điều kiện nhiệt độ và áp suất, hai bình khí có thể tích bằng nhau có cùng số mol khí.
- Ở điều kiện chuẩn (25 °C và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lit.
- Thể tích mol của a mol khi ở điều kiện chuẩn là V = 24,79 (L).
- Để xác định khí A nặng hơn hay nhẹ hơn khí B bao nhiêu lần, ta dựa vào tỉ số giữa khối lượng mol của khí A (MA) và khối lượng mol của khí B (MB). Tỉ số này được gọi là tỉ khối của khÍ A đối với khÍ B, được biểu diễn bằng công thức: dA/B = MA/MB.
- Để xác định một khi A nặng hơn hay nhẹ hơn không khí bao nhiêu lần, ta dựa vào tỉ số giữa khối lượng mol của khí A và "khối lượng mol" của không khí:
- Coi không khí gồm 20% oxygen và 80% nitrogen về thể tích. Vậy trong 1 mol không khí có 0,2 mol oxygen và 0,8 mol nitrogen. Khối lượng mol của không khí là: Mkk= 0,2×32 + 0,8×28 = 28.8 (g/mol).
Tỉ khối của khí A so với không khí là: d = m/Mkk.
Sơ đồ tư duy KHTN 8 Bài 3: Mol và tỉ khối chất khí
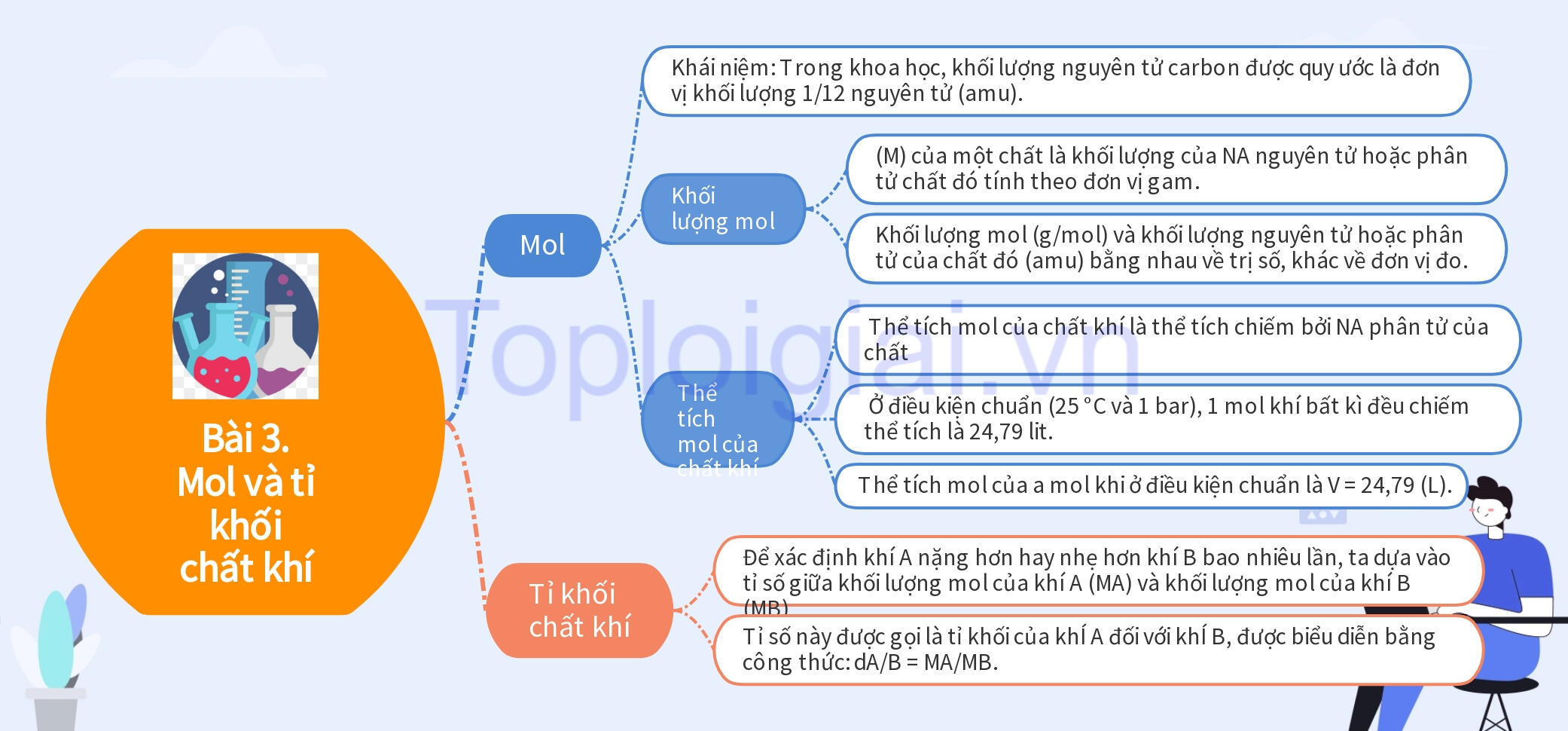
B. Bài tập KHTN 8 Bài 3: Mol và tỉ khối chất khí
Đang cập nhật
Xem thêm tóm tắt lý thuyết KHTN 8 sách Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 4: Dung dịch và nồng độ
Lý thuyết Bài 5: Định luật bảo toàn khối lượng và phương trình hóa học
Lý thuyết Bài 6: Tính theo phương trình hóa học
Xem thêm các chương trình khác:
- Soạn văn 8 Kết nối tri thức (hay nhất)
- Văn mẫu lớp 8 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 8 – Kết nối tri thức
- Bố cục tác phẩm Ngữ văn lớp 8 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn lớp 8 - Kết nối tri thức
- Giải SBT Ngữ văn 8 – Kết nối tri thức
- Giải Vở thực hành Ngữ văn 8 Kết nối tri thức | VTH Ngữ văn 8 Tập 1, Tập 2
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Kết nối tri thức
- Soạn văn 8 Kết nối tri thức (ngắn nhất)
- Giải sgk Toán 8 – Kết nối tri thức
- Lý thuyết Toán 8 – Kết nối tri thức
- Giải sbt Toán 8 – Kết nối tri thức
- Vở thực hành Toán 8 Kết nối tri thức | Giải VTH Toán 8 Tập 1, Tập 2
- Chuyên đề dạy thêm Toán 8 cả 3 sách (2024 có đáp án)
- Bài tập Tiếng Anh 8 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 8 – Global success
- Giải sbt Tiếng Anh 8 - Global Success
- Trọn bộ Từ vựng Tiếng Anh 8 Global success đầy đủ nhất
- Ngữ pháp Tiếng Anh 8 Global success
- Giải sgk Lịch sử 8 – Kết nối tri thức
- Lý thuyết Lịch sử 8 - Kết nối tri thức
- Giải sbt Lịch sử 8 – Kết nối tri thức
- Giải sgk Địa lí 8 – Kết nối tri thức
- Lý thuyết Địa lí 8 - Kết nối tri thức
- Giải sbt Địa lí 8 – Kết nối tri thức
- Giải VTH Địa lí 8 Kết nối tri thức | Vở thực hành Địa lí 8
- Giải sgk Giáo dục công dân 8 – Kết nối tri thức
- Lý thuyết Giáo dục công dân 8 – Kết nối tri thức
- Giải sbt Giáo dục công dân 8 – Kết nối tri thức
- Giải sgk Công nghệ 8 – Kết nối tri thức
- Lý thuyết Công nghệ 8 - Kết nối tri thức
- Giải sbt Công nghệ 8 – Kết nối tri thức
- Giải sgk Tin học 8 – Kết nối tri thức
- Lý thuyết Tin học 8 - Kết nối tri thức
- Giải sbt Tin học 8 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 8 – Kết nối tri thức
