TOP 15 câu Trắc nghiệm Nguyên tố hóa học (Kết nối tri thức 2024) có đáp án - Hóa học 10
Bộ 15 bài tập trắc nghiệm Hóa học lớp 10 Bài 2: Nguyên tố hóa học có đáp án đầy đủ các mức độ sách Kết nối tri thức giúp học sinh ôn luyện trắc nghiệm Hóa học 10 Bài 2.
Chỉ 150k mua trọn bộ Trắc nghiệm Hóa lớp 10 Kết nối tri thức bản word (cả năm) có đáp án chi tiết:
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận tài liệu.
Xem thử tài liệu tại đây: Link tài liệu
Trắc nghiệm Hóa 10 Bài 2: Nguyên tố hóa học - Kết nối tri thức
Câu 1. Nguyên tố hóa học là
A. tập hợp các nguyên tử có cùng số neutron trong nguyên tử.
B. tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân.
C. tập hợp các nguyên tử có cùng số khối.
D. tập hợp các nguyên tử có cùng kích thước.
Đáp án: B
Giải thích:
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân.
Câu 2. Các nguyên tử của cùng một nguyên tố hóa học có
A. tính chất hóa học giống nhau.
B. khối lượng nguyên tử giống nhau.
C. kích thước nguyên tử giống nhau.
D. tổng số hạt proton, neutron và electron giống nhau.
Đáp án: A
Giải thích:
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân. Trong nguyên tử, số đơn vị điện tích hạt nhân bằng số electron ở vỏ nguyên tử. Các electron trong nguyên tử quyết định tính chất hóa học của nguyên tử, nên các nguyên tử của cùng một nguyên tố hóa học có tính chất hóa học giống nhau.
Câu 3. Cho các nguyên tử sau: A (Z = 8, A = 16), B (Z = 9, A = 19), E (Z = 8, A = 18), G (Z = 11, A = 23). Trong các nguyên tử trên, các nguyên tử nào thuộc cùng một nguyên tố hóa học?
A. A và B.
B. A, B và E.
C. A và E.
D. E và G.
Đáp án: C
Giải thích:
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số đơn vị điện tích hạt nhân.
® Nguyên tử A (Z = 8, A = 16) và nguyên tử E (Z = 8, A = 18) thuộc cùng một nguyên tố hóa học.
Câu 4. Những đặc trưng cơ bản của một nguyên tử là
A. số đơn vị điện tích hạt nhân nguyên tử và khối lượng nguyên tử.
B. số đơn vị điện tích hạt nhân và kích thước nguyên tử.
C. số khối và khối lượng nguyên tử.
D. số đơn vị điện tích hạt nhân và số khối.
Đáp án: D
Giải thích:
Số đơn vị điện tích hạt nhân nguyên tử của một nguyên tố hóa học (còn được gọi là số hiệu nguyên tử (Z) của nguyên tố đó) và số khối (A) là những đặc trưng cơ bản của một nguyên tử.
Câu 5. Cho biết kí hiệu nguyên tử của nguyên tố nitrogen là ![]() . Phát biểu nào sau đây không đúng?
. Phát biểu nào sau đây không đúng?
A. Nguyên tố nitrogen kí hiệu là N.
B. Nguyên tử nitrogen có 7 proton, 8 neutron và 7 electron.
C. Số khối của nguyên tử nitrogen là 14.
D. Số hiệu nguyên tử nitrogen bằng 7.
Đáp án: B
Giải thích:
Kí hiệu ![]() cho biết nguyên tử nitrogen có:
cho biết nguyên tử nitrogen có:
+ Kí hiệu là N.
+ Số hiệu nguyên tử nitrogen bằng 7, nên trong hạt nhân nitrogen có 7 proton, vỏ nguyên tử có 7 electron.
+ Số khối (A) của nguyên tử nitrogen là 14 nên trong hạt nhân có số neutron là
14 – 7 = 7.
® Phát biểu không đúng: Nguyên tử nitrogen có 7 proton, 8 neutron và 7 electron.
Câu 6. Nguyên tử của nguyên tố phosphorus có 15 proton và 16 neutron. Kí hiệu của nguyên tử phosphorus là
A. ![]() .
.
B. ![]() .
.
C. ![]() .
.
D. ![]() .
.
Đáp án: D
Giải thích:
Khi viết kí hiệu nguyên tử, đặt hai chỉ số đặc trưng ở bên trái kí hiệu nguyên tố, trong đó số hiệu nguyên tử Z ở phía dưới và số khối A ở phía trên.
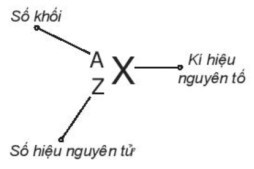
Nguyên tử của nguyên tố phosphorus có 15 proton và 16 neutron.
® Số hiệu nguyên tử (Z) = Số proton = 15.
Số khối: A = Z + N = 15 + 16 = 31.
® Kí hiệu của nguyên tử phosphorus là ![]() .
.
Câu 7. Đồng vị là
A. những nguyên tử có cùng số đơn vị điện tích hạt nhân (cùng số proton) nhưng có số neutron khác nhau.
B. những nguyên tử có cùng số electron và có số neutron khác nhau.
C. những nguyên tử có cùng số hiệu nguyên tử và có cùng số neutron.
D. những nguyên tử có cùng kích thước nhưng có số neutron khác nhau.
Đáp án: A
Giải thích:
Đồng vị là những nguyên tử có cùng số đơn vị điện tích hạt nhân (cùng số proton) nhưng có số neutron khác nhau.
Câu 8. Phát biểu nào sau đây không đúng?
A. Các đồng vị khác nhau về số neutron.
B. Các đồng vị khác nhau về khối lượng của hạt nhân nguyên tử.
C. Các đồng vị khác nhau về một số tính chất vật lí.
D. Các đồng vị khác nhau về số proton.
Đáp án: D
Giải thích:
Đồng vị là những nguyên tử có cùng số đơn vị điện tích hạt nhân (cùng số proton) nhưng có số neutron khác nhau.
Các đồng vị khác nhau về số neutron nên khác nhau về khối lượng của hạt nhân nguyên tử, đồng thời khác nhau về một số tính chất vật lí.
® Phát biểu không đúng: Các đồng vị khác nhau về số proton.
Câu 9. Cho các nguyên tử: X (Z = 17, A = 35); Y (Z = 12, A = 24), E (Z = 17, A = 37); G (Z = 15, A = 31). Các nguyên tử nào là đồng vị của nhau?
A. X và G.
B. Y và E.
C. X và E.
D. Y và G.
Đáp án: C
Giải thích:
Đồng vị là những nguyên tử có cùng số đơn vị điện tích hạt nhân (cùng số proton) nhưng có số neutron khác nhau.
® X và E là đồng vị của nhau (đều có Z = 17 và số neutron khác nhau).
Câu 10. Số neutron của các đồng vị ![]() lần lượt là:
lần lượt là:
A. 14, 15, 17.
B. 14, 15, 16.
C. 16, 15, 14.
D. 15, 16, 17.
Đáp án: B
Giải thích:
Nguyên tử ![]() có:
có:
Số hiệu nguyên tử Z = 14 = Số proton.
Số khối: A = Z + N ® N = A – Z = 28 – 14 = 14.
Nguyên tử ![]() có:
có:
Số hiệu nguyên tử Z = 14 = Số proton.
Số khối: A = Z + N ® N = A – Z = 29 – 14 = 15.
Nguyên tử ![]() có:
có:
Số hiệu nguyên tử Z = 14 = Số proton.
Số khối: A = Z + N ® N = A – Z = 30 – 14 = 16.
® Số neutron của các đồng vị ![]() lần lượt là: 14, 15, 16.
lần lượt là: 14, 15, 16.
Câu 11. Vì sao có thể coi khối lượng nguyên tử xấp xỉ số khối?
A. Vì khối lượng proton nhỏ hơn rất nhiều khối lượng của electron và neutron.
B. Vì khối lượng electron nhỏ hơn rất nhiều khối lượng của proton và neutron.
C. Vì hạt nhân nguyên tử có kích thước nhỏ hơn rất nhiều so với nguyên tử.
D. Vì nguyên tử có cấu tạo rỗng.
Đáp án: B
Giải thích:
Nguyên tử khối là khối lượng tương đối của nguyên tử. Do khối lượng proton và neutron đều xấp xỉ 1,0 amu, còn khối lượng electron nhỏ hơn rất nhiều (0,00055 amu), nên có thể coi nguyên tử khối xấp xỉ số khối.
Câu 12. Nguyên tử aluminium (nhôm) có số proton là 13, số neutron là 14. Nguyên tử khối của aluminium là
A. 13.
B. 14.
C. 27.
D. 30.
Đáp án: C
Giải thích:
Có thể coi nguyên tử khối xấp xỉ số khối.
® Nguyên tử khối của aluminium xấp xỉ là 13 + 14 = 27.
Câu 13. Bằng phương pháp phổ khối lượng, người ta xác định được trong tự nhiên, nguyên tố neon (Ne) có ba đồng vị bền là N2010e (chiếm 90,0%), N2110e (chiếm 1,0%) và N2210e (chiếm 9,0%).Tính nguyên tử khối trung bình của Ne.
A. 21,85.
B. 20,85.
C. 21,19.
D. 20,19.
Đáp án: D
Giải thích:
Nguyên tử khối trung bình của Ne là:
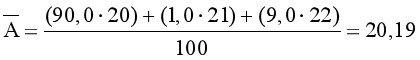
Câu 14. Bằng phương pháp phổ khối lượng, người ta xác định được trong tự nhiên, nguyên tố chlorine có hai đồng vị bền là ![]() và
và ![]() . Nguyên tử khối trung bình của chlorine là 35,48. Tính phần trăm số nguyên tử của đồng vị
. Nguyên tử khối trung bình của chlorine là 35,48. Tính phần trăm số nguyên tử của đồng vị ![]() tồn tại trong tự nhiên.
tồn tại trong tự nhiên.
A. 76%.
B. 24%.
C. 32%.
D. 68%.
Đáp án: A
Giải thích:
Gọi phần trăm số nguyên tử của đồng vị lần lượt là x, y (%).
Ta có: x + y = 100 (1)
Nguyên tử khối trung bình của chlorine là 35,48.
® 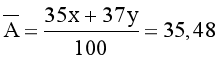 (2)
(2)
Từ (1) và (2), suy ra: x = 76, y = 24.
Vậy phần trăm số nguyên tử của đồng vị ![]() tồn tại trong tự nhiên là 76%.
tồn tại trong tự nhiên là 76%.
Câu 15. Nguyên tử khối trung bình của copper bằng 63,546. Copper tồn tại trong tự nhiên dưới dạng hai dạng đồng vị, trong đó có một đồng vị là ![]() chiếm 72,7%. Số khối của đồng vị còn lại là
chiếm 72,7%. Số khối của đồng vị còn lại là
A. 64.
B. 65.
C. 66.
D. 67.
Đáp án: B
Giải thích:
Gọi đồng vị còn lại của copper là ![]() , chiếm: 100% - 72,7% = 27,3%.
, chiếm: 100% - 72,7% = 27,3%.
Nguyên tử khối trung bình của copper bằng 63,546.
®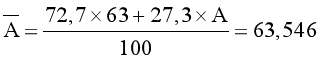 ® A = 65.
® A = 65.
Vậy, số khối của đồng vị còn lại là 65.
Các câu hỏi trắc nghiệm Hóa học lớp 10 sách Kết nối tri thức có đáp án, chọn lọc khác:
Trắc nghiệm Bài 3: Cấu trúc lớp vỏ electron nguyên tử
Trắc nghiệm Bài 4: Ôn tập chương 1
Trắc nghiệm Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Trắc nghiệm Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Xem thêm các chương trình khác:
- Trắc nghiệm Toán lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm Địa Lí lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm GDTC lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm Lịch sử lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm Sinh học lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm Kinh tế pháp luật lớp 10 có đáp án - Chân trời sáng tạo
- Trắc nghiệm Vật lí lớp 10 có đáp án - Chân trời sáng tạo
- Trắc nghiệm Hóa học lớp 10 có đáp án - Chân trời sáng tạo
- Trắc nghiệm Hóa học lớp 10 có đáp án – Cánh Diều
- Trắc nghiệm Vật Lí lớp 10 có đáp án – Cánh Diều
- Trắc nghiệm Địa Lí lớp 10 có đáp án – Cánh Diều
- Trắc nghiệm Công nghệ lớp 10 có đáp án – Cánh Diều
- Trắc nghiệm Giáo Dục Quốc Phòng lớp 10 có đáp án – Cánh Diều
- Trắc nghiệm GDTC lớp 10 có đáp án – Cánh Diều
