Giải KHTN 8 Bài 3 (Chân trời sáng tạo): Phản ứng hoá học và năng lượng trong các phản ứng hoá học
Với lời giải bài tập Khoa học tự nhiên lớp 8 Bài 3: Phản ứng hoá học và năng lượng trong các phản ứng hoá học sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi và làm bài tập KHTN 8 Bài 3.
Giải KHTN 8 Bài 3: Phản ứng hoá học và năng lượng trong các phản ứng hoá học
Trả lời:
- Khi một chất bị biến đổi hoá học sẽ có chất mới được tạo thành, quá trình này được gọi là phản ứng hoá học.
- Dấu hiệu chứng tỏ có phản ứng hoá học xảy ra: xuất hiện chất khí, chất kết tủa; thay đổi màu sắc, mùi; phát sáng, giải phóng hoặc hấp thụ nhiệt năng, …
1. Phản ứng hoá học
Trả lời:
Hỗn hợp sau khi đun nóng không còn tính chất của iron do hỗn hợp này không bị nam châm hút.
Trả lời:
- Chất tham gia: sắt, lưu huỳnh;
- Chất mới tạo thành: iron(II) sulfide (FeS).
Trả lời:
- Chất đầu: hydrogen; nitrogen.
- Sản phẩm: ammonia.
2. Diễn biến của phản ứng hoá học
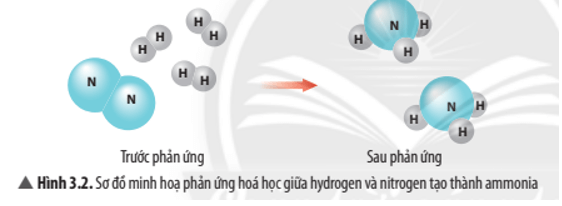
Câu hỏi thảo luận 3 trang 20 KHTN 8: Quan sát Hình 3.2, hãy cho biết:
a) trước và sau phản ứng những nguyên tử nào liên kết với nhau.
b) số nguyên tử H cũng như số nguyên tử N có thay đổi không.
Trả lời:
a) Trước phản ứng H liên kết với H; N liên kết với N. Sau phản ứng N liên kết với H.
b) Số nguyên tử H cũng như số nguyên tử N không thay đổi.
3. Một số dấu hiệu nhận biết có phản ứng hoá học xảy ra
Trả lời:
Dấu hiệu chứng tỏ đã có phản ứng hoá học xảy ra:
- Hình 3.3: có sự phát sáng và giải phóng nhiệt năng;
- Hình 3.4: đường chuyển từ màu trắng sang màu nâu rồi màu đen;
- Hình 3.5: xuất hiện bọt khí.
- Hình 3.6: có chất kết tủa tạo thành sau phản ứng.
Luyện tập trang 21 KHTN 8: Hãy chỉ ra dấu hiệu của phản ứng hoá học trong các trường hợp dưới đây:
a) Đinh sắt để lâu trong không khí sẽ xuất hiện lớp gỉ sét màu nâu bám bên ngoài đinh sắt.
b) Dùng củi để nhóm lửa để sưởi ấm.
Trả lời:
Dấu hiệu của phản ứng hoá học xảy ra:
a) Xuất hiện lớp gỉ sét màu nâu bám bên ngoài đinh sắt.
b) Có sự phát sáng và giải phóng nhiệt năng
4. Năng lượng trong phản ứng hoá học
Trả lời:
- Giống nhau: Đều có sự thay đổi năng lượng.
- Khác nhau:
+ Phản ứng toả nhiệt: giải phóng nhiệt năng ra môi trường.
+ Phản ứng thu nhiệt: nhận năng lượng từ môi trường xung quanh.
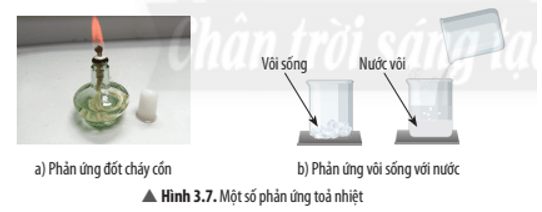
Trả lời:
- Đốt cháy cồn: cồn cháy, toả nhiều nhiệt;
- Cho vôi sống vào nước: nước sôi, toả nhiều nhiệt.
Luyện tập trang 22 KHTN 8: Hãy cho biết phản ứng toả nhiệt hay thu nhiệt trong mỗi trường hợp sau:
b) Hoà tan viên vitamin C sủi vào nước.
Trả lời:
a) Ngọn nến đang cháy: phản ứng toả nhiệt;
b) Hoà tan viên vitamin C sủi vào nước: phản ứng thu nhiệt.
Trả lời:
Do xăng, dầu, than dễ cháy và khi cháy toả nhiều nhiệt nên được sử dụng làm nhiên liệu trong đời sống và sản xuất
Trả lời:
Nguồn nhiệt này chủ yếu được tạo ra từ quá trình đốt cháy nhiên liệu.
Kiến thức trọng tâm KHTN 8 Bài 3: Phản ứng hoá học và năng lượng trong các phản ứng hoá học
I. Phản ứng hoá học
Quá trình biến đổi chất này thành chất khác được gọi là phản ứng hoá học.
Chất tham gia phản ứng gọi là chất đầu.
Chất mới tạo thành gọi là sản phẩm.
Ví dụ: Hỗn hợp sắt (iron) và lưu huỳnh (sulfur) đã phản ứng với nhau khi đun nóng để tạo thành hợp chất iron(II) sulfide (FeS).
Trong đó chất đầu là sắt và lưu huỳnh; sản phẩm là iron(II) sulfide.
II. Diễn biến của phản ứng hoá học
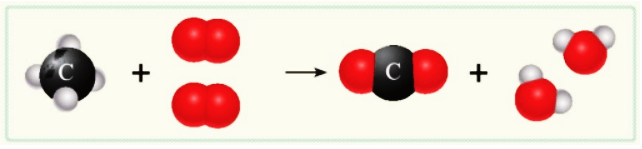
Trong phản ứng hoá học, có sự phá vỡ liên kết cũ và hình thành liên kết mới. Kết quả là chất này biến đổi thành chất khác.
Sơ đồ mô tả phản ứng đốt cháy khí methane trong không khí thu được carbon dioxide và nước
III. Một số dấu hiệu nhận biết có phản ứng hoá học xảy ra
Một số dấu hiệu có thể nhận biết phản ứng hoá học xảy ra: xuất hiện chất khí, chất kết tủa; thay đổi màu sắc, mùi; phát sáng, giải phóng hoặc hấp thụ nhiệt năng, …
 |
 |
|
Gas cháy sẽ toả nhiệt |
Phản ứng phân huỷ đường thành than và hơi nước |
 |
 |
|
Kẽm tác dụng với dung dịch hydrochloric acid tạo bọt khí |
Chất kết tủa tạo thành sau phản ứng |
IV. Năng lượng trong phản ứng hoá học
1. Phản ứng toả nhiệt, phản ứng thu nhiệt
Trong một phản ứng hoá học, luôn có sự thay đổi năng lượng. Năng lượng có thể toả ra hoặc nhận vào, thường dưới dạng nhiệt. Vì vậy, ta có thể chia phản ứng thành hai nhóm: phản ứng toả nhiệt và phản ứng thu nhiệt.
+ Phản ứng toả nhiệt là phản ứng có sự giải phóng năng lượng ra môi trường bên ngoài, thể hiện ở sự gia tăng nhiệt độ.
Những phản ứng toả nhiệt có thể được viết tổng quát như sau:
Chất phản ứng → Sản phẩm + năng lượng
+ Phản ứng thu nhiệt là những phản ứng hấp thụ năng lượng từ môi trường xung quanh.
Những phản ứng thu nhiệt có thể được viết tổng quát như sau:
Chất phản ứng + năng lượng → Sản phẩm
2. Các ứng dụng phổ biến của phản ứng toả nhiệt
Sự đốt cháy nhiên liệu (than, dầu hoả, gas, …) tạo ra năng lượng nhiệt phục vụ cho việc nấu nướng, sưởi ấm, …
Quá trình hô hấp trong cơ thể cung cấp năng lượng để cơ thể hoạt động, đồng thời tạo nên thân nhiệt ổn định và hỗ trợ quá trình vận động.
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 8 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Định luật bảo toàn khối lượng và phương trình hoá học
Bài 5: Mol và tỉ khối của chất khí
Xem thêm các chương trình khác:
- Soạn văn lớp 8 Chân trời sáng tạo (hay nhất)
- Văn mẫu lớp 8 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 8 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 8 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 8 - Chân trời sáng tạo
- Giải SBT Ngữ văn 8 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Chân trời sáng tạo
- Soạn văn 8 Chân trời sáng tạo (ngắn nhất)
- Giải sgk Toán 8 – Chân trời sáng tạo
- Lý thuyết Toán 8 – Chân trời sáng tạo
- Giải sbt Toán 8 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 8 – Friends Plus
- Giải sbt Tiếng Anh 8 - Friends plus
- Trọn bộ Từ vựng Tiếng Anh 8 Friends plus đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 8 Friends plus đầy đủ nhất
- Giải sgk Lịch sử 8 – Chân trời sáng tạo
- Lý thuyết Lịch sử 8 - Chân trời sáng tạo
- Giải sbt Lịch sử 8 – Chân trời sáng tạo
- Giải sgk Địa lí 8 – Chân trời sáng tạo
- Lý thuyết Địa lí 8 - Chân trời sáng tạo
- Giải sbt Địa lí 8 – Chân trời sáng tạo
- Giải sgk Giáo dục công dân 8 – Chân trời sáng tạo
- Lý thuyết Giáo dục công dân 8 – Chân trời sáng tạo
- Giải sbt Giáo dục công dân 8 – Chân trời sáng tạo
- Giải sgk Công nghệ 8 – Chân trời sáng tạo
- Lý thuyết Công nghệ 8 - Chân trời sáng tạo
- Giải sbt Công nghệ 8 – Chân trời sáng tạo
- Giải sgk Tin học 8 – Chân trời sáng tạo
- Lý thuyết Tin học 8 - Chân trời sáng tạo
- Giải sbt Tin học 8 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 8 – Chân trời sáng tạo