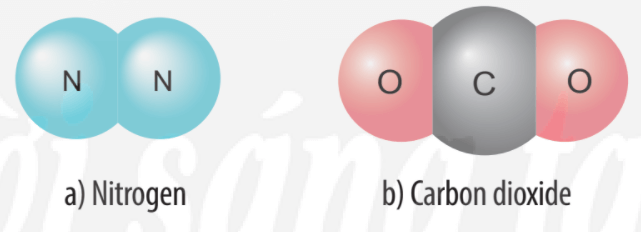Giải Khoa học tự nhiên 7 Bài 6 (Chân trời sáng tạo): Giới thiệu về liên kết hóa học
Với lời giải bài tập Khoa học tự nhiên lớp 7 Bài 6: Giới thiệu về liên kết hóa học sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi và làm bài tập KHTN 7 Bài 6.
Giải bài tập Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học
Video giải bài tập Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học
Các nguyên tử của nguyên tố kết hợp với nhau theo quy tắc nào?
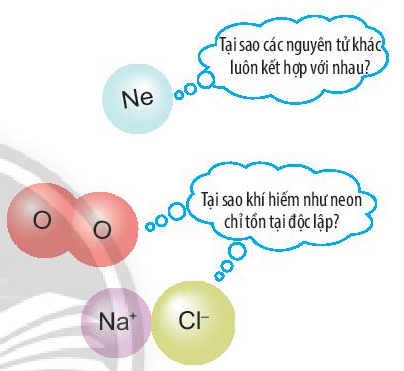
Trả lời:
Các nguyên tử của nguyên tố có xu hướng kết hợp với nhau để có số electron ở lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm.
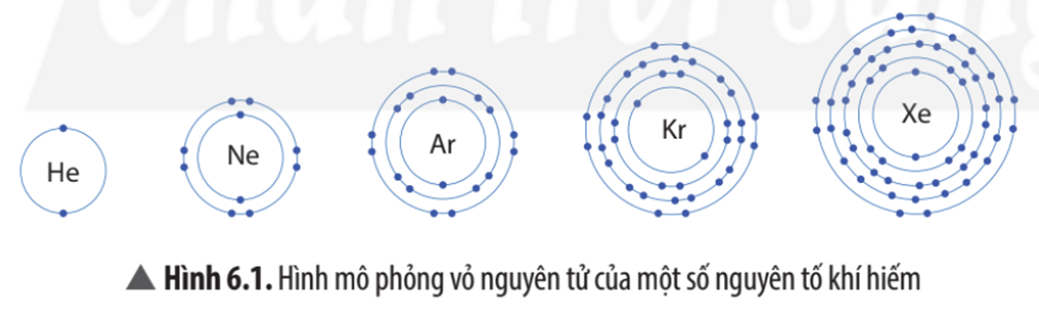
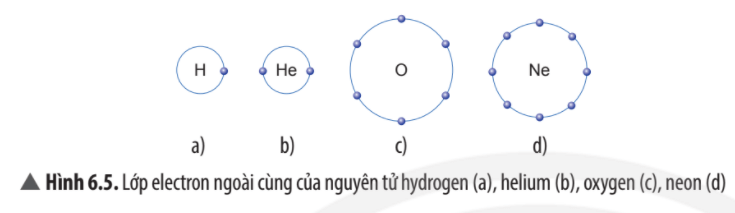
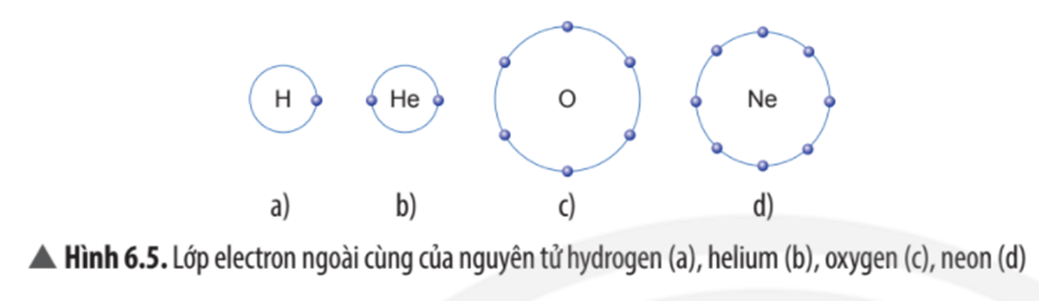
1. Vỏ nguyên tử khí hiếm
Trả lời:
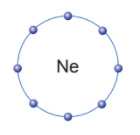
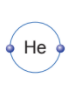
Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng chỉ có 2 electron.
2. Liên kết ion
Trả lời:
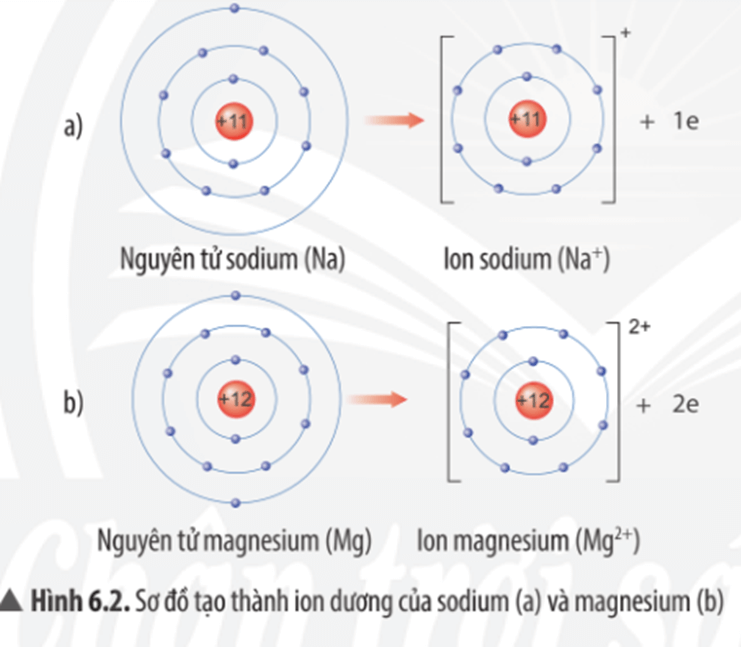
Mô tả sự tạo thành ion sodium, ion magnesium:
- Nguyên tử sodium (Na) nhường đi 1 electron ở lớp vỏ ngoài cùng để trở thành ion sodium mang điện tích dương, kí hiệu Na+.
- Nguyên tử magnesium (Mg) nhường đi 2 electron ở lớp vỏ ngoài cùng để trở thành ion magnesium mang điện tích dương, kí hiệu Mg2+.
Nhận xét:
- Các ion này đều có 8 electron lớp ngoài cùng.
- Sự phân bố electron của ion sodium (Na+) và ion magnesium (Mg2+) đều giống với sự phân bố electron của nguyên tử khí hiếm neon (Ne).
Trả lời:
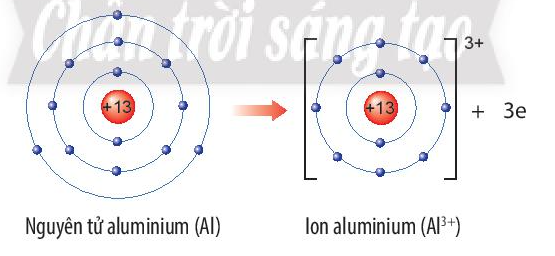
Aluminium (Al) thuộc ô số 13, chu kì 3, nhóm IIIA trong bảng tuần hoàn.
Nguyên tử aluminium nhường 3 electron ở lớp ngoài cùng để trở thành ion aluminium, kí hiệu Al3+
Sơ đồ tạo thành ion aluminium:
Trả lời:
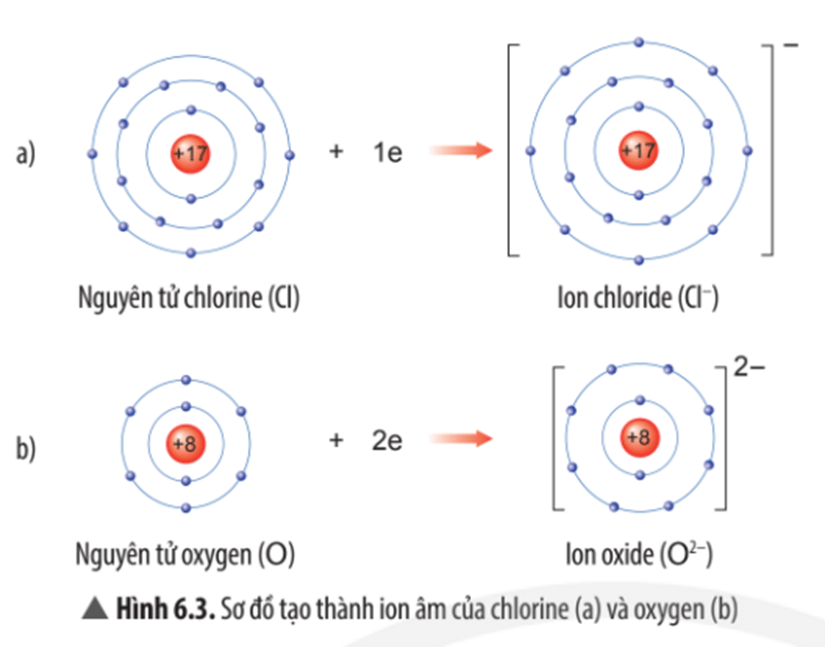
Mô tả sự tạo thành ion chloride, ion oxide:
- Nguyên tử chlorine nhận thêm 1 electron vào lớp electron ngoài cùng để trở thành ion chloride mang điện tích âm, kí hiệu Cl-;
- Nguyên tử oxygen nhận thêm 2 electron vào lớp electron ngoài cùng để trở thành ion oxide mang điện tích âm, kí hiệu O2-.
Nhận xét:
- Lớp vỏ của các ion chloride và ion oxide đều có 8 electron lớp ngoài cùng.
- Sự phân bố electron của ion chloride giống với sự phân bố electron của nguyên tử khí hiếm argon (Ar).
 - Sự phân bố electron của ion oxide giống với sự phân bố electron của nguyên tử khí hiếm neon (Ne).
- Sự phân bố electron của ion oxide giống với sự phân bố electron của nguyên tử khí hiếm neon (Ne).

Trả lời:
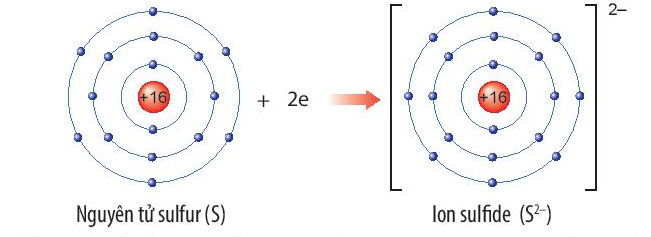
Nguyên tố sulfur (S) thuộc ô thứ 16, chu kì 3, nhóm VIA trong bảng tuần hoàn.
Nguyên tử sulfur nhận thêm 2 electron để trở thành ion ion sulfide (S2-). Ion sulfide (S2-) có 8 electron lớp ngoài cùng, sự phân bố electron trên ion sulfide (S2-) giống với sự phân bố electron của nguyên tử khí hiếm argon (Ar).
Trả lời:
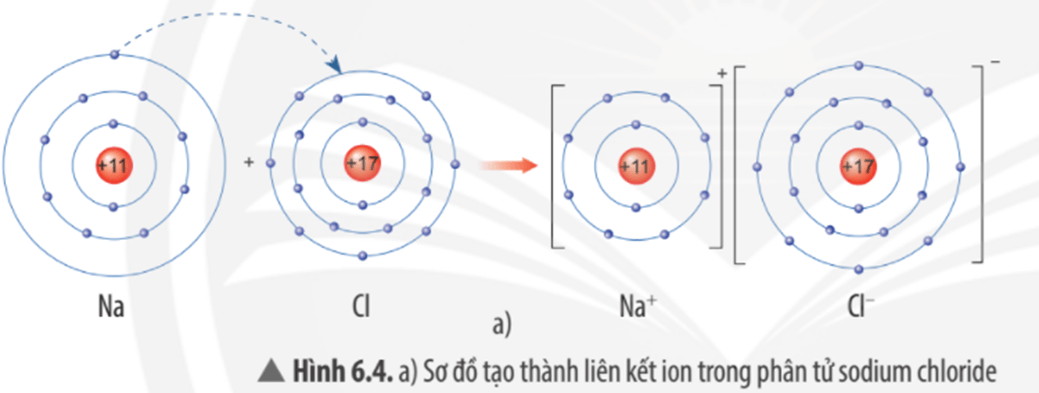
Mô tả quá trình tạo thành liên kết ion trong phân tử sodium chloride:
Khi nguyên tử sodium (Na) kết hợp với nguyên tử chlorine (Cl), nguyên tử Na nhường 1 electron tạo thành ion dương, kí hiệu là Na+, đồng thời nguyên tử Cl nhận 1 electron từ nguyên tử Na tạo thành ion âm, kí hiệu Cl-. Ion Na+ và Cl- hút nhau tạo phân tử sodium chloride (NaCl).
Một số ứng dụng của sodium chloride trong đời sống:
- Trong công nghiệp:
+ Sodium chloride dùng sản xuất giấy, thuốc nhuộm;…
+ Sử dụng trong công nghiệp dệt may và sản xuất vải, sản xuất xà phòng, chất tẩy rửa.
+ Nguyên liệu ban đầu để sản xuất chlorine và xút.
+ Trong công nghiệp sản xuất giày da, người ta sử dụng sodium chloride để bảo vệ da.
+ Trong sản xuất cao su, sodium chloride được dùng để làm trắng các loại cao su.
+ Trong dầu khí, sodium chloride là thành phần quan trọng trong dung dịch khoan giếng.
+ Từ sodium chloride có thể chế ra các loại hóa chất dùng trong các ngành khác như sản xuất nhôm, đồng, thép, điều chế nước Javen, … bằng cách điện phân nóng chảy hoặc điện phân dung dịch sodium chloride có màng ngăn.
- Trong nông nghiệp và trong đời sống:
+ Giúp cân bằng sinh lí trong cơ thể con người, gia súc, gia cầm, …
+ Cung cấp thêm vi lượng khi trộn với các loại phân hữu cơ để tăng hiệu quả của phân bón;
+ Sodium chloride có tính hút ẩm, do đó được sử dụng để bảo quản thực phẩm, nó làm tăng áp suất thẩm thấu khiến vi khuẩn mất nước và chết.
+ Sodium chloride dùng để ướp thực phẩm tươi sống như tôm, cá, … để không bị ươn, ôi trước khi thực phẩm được nấu, vận chuyển đi xa, …
- Trong y tế:
+ Sát trùng vết thương;
+ Pha huyết thanh, thuốc tiêu độc và một số loại thuốc khác để chữa bệnh,
+ Cung cấp muối khoáng cho cơ thể;
+ Khử độc, thanh lọc cơ thể, làm đẹp da, chữa viêm họng, hôi miệng …
Trả lời:
Khi nguyên tử magnesium (Mg) kết hợp với nguyên tử oxygen (O), nguyên tử magnesium nhường 2 electron tạo thành ion magnesium, mang điện tích dương, kí hiệu là Mg2+, đồng thời nguyên tử oxygen (O) nhận 2 electron từ nguyên tử Mg tạo thành ion oxide, mang điện tích âm, kí hiệu O2-. Ion Mg2+ và O2- hút nhau tạo phân tử magnesium oxide (MgO).
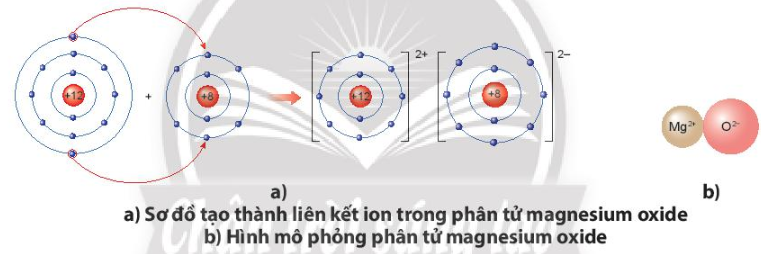

Trả lời:
Sơ đồ tạo thành liên kết trong phân tử calcium chloride:
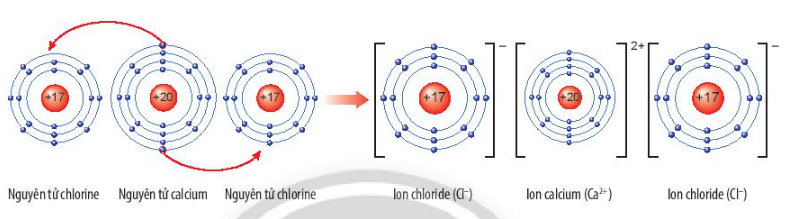
Ứng dụng của CaCl2:
- Dùng để làm khô trong quy trình chế biến thực phẩm đóng hộp và các loại tinh bột;
- Làm chất chống đóng băng trên mặt đường ở những quốc gia ôn đới hoặc làm chất chống diệt bụi, nấm mốc.
- Trong xây dựng, calcium chloride là chất làm tăng thời gian đông của bê tông.
- Trong công nghiệp luyện kim và sản xuất giấy, chất này đóng vai trò là chất phụ gia trong quá trình tải nhiệt và làm khô.
- Calcium chloride được ứng dụng trong hệ thống tiêu nước và xử lý nước thải công nghiệp;
- Là chất hỗ trợ giúp hút oxygen trong không khí, được ứng dụng làm thiết bị cứu hỏa.
3. Liên kết cộng hóa trị
Trả lời:
Nguyên tố khí hiếm gần nhất của hydrogen là helium (He).
Nguyên tử hydrogen có 1 electron lớp ngoài cùng, để có lớp electron ngoài cùng giống nguyên tố helium (2 electron lớp ngoài cùng) nguyên tử hydrogen có xu hướng thêm 1 electron.
Nguyên tố khí hiếm gần nhất của oxygen là neon (Ne).
Nguyên tử oxygen có 6 electron lớp ngoài cùng, để có lớp electron ngoài cùng giống nguyên tố neon (8 electron lớp ngoài cùng) nguyên tử oxygen có xu hướng thêm 2 electron.
Trả lời:
- Trong phân tử hydrogen (H2), mỗi nguyên tử hydrogen (H) đều có 2 electron ở lớp ngoài cùng. Khi đó, lớp electron ngoài cùng của nguyên tử hydrogen giống với khí hiếm helium (He)
- Trong phân tử oxygen (O2), mỗi nguyên tử oxygen (O) đều có 8 electron ở lớp ngoài cùng. Khi đó, lớp electron ngoài cùng của nguyên tử oxygen giống với khí hiếm neon (Ne).
Trả lời:
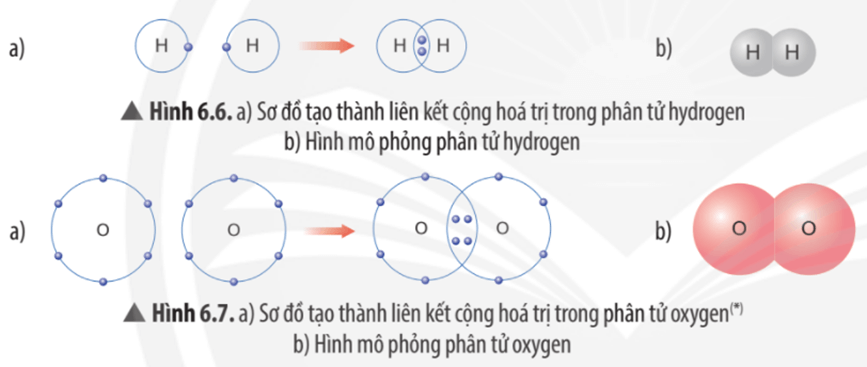
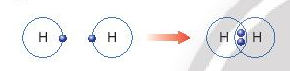
- Quá trình tạo thành liên kết cộng hóa trị trong phân tử hydrogen:
+ Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử H liên kết với nhau, mỗi nguyên tử góp chung 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử H cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử hydrogen.
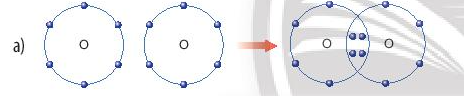
 - Quá trình tạo thành liên kết cộng hóa trị trong phân tử oxygen:
- Quá trình tạo thành liên kết cộng hóa trị trong phân tử oxygen:
+ Nguyên tử O có 6 electron lớp ngoài cùng, cần thêm 2 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử O liên kết với nhau, mỗi nguyên tử góp 2 electron để tạo ra hai cặp electron dùng chung.
+ Hạt nhân của hai nguyên tử O cùng hút các cặp electron dùng chung và liên kết với nhau tạo thành phân tử oxygen.
Trả lời:
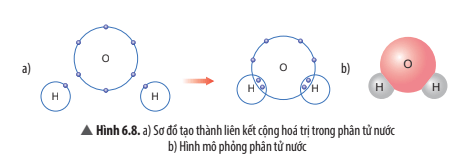
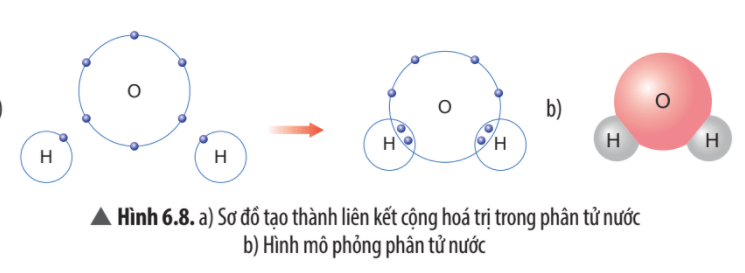
- Mỗi nguyên tử H góp chung 1 electron, nguyên tử O góp chung 1 electron với mỗi nguyên tử H. Trong phân tử nước có 2 nguyên tử H, vậy nguyên tử O góp chung 2 electron với 2 nguyên tử H.
- Trong phân tử nước, số electron ở lớp ngoài cùng của O là 8 electron giống với khí hiếm neon (Ne).
Trong phân tử nước, số electron ở lớp ngoài cùng của H là 2 electron giống với khí hiếm helium (He),
Trả lời:
Khi tạo thành phân tử nước, nguyên tử O góp 2 electron, mỗi nguyên tử H góp 1 electron. Như vậy, giữa nguyên tử O và nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử O và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử nước.
Luyện tập trang 41 KHTN lớp 7: Vẽ sơ đồ hình thành liên kết cộng hóa trị trong các phân tử sau
Trả lời:
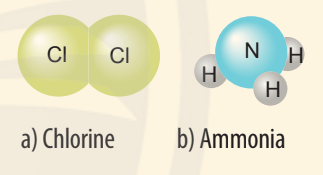
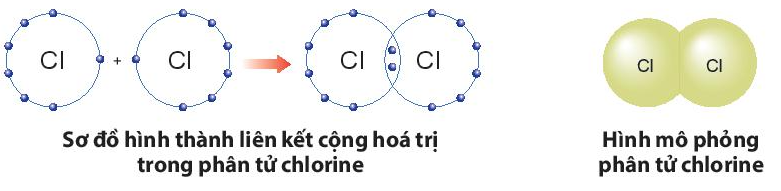
a) Sự hình thành liên kết trong phân tử chlorine:
- Nguyên tử Cl có 7 electron lớp ngoài cùng, cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
- Khi hai nguyên tử Cl liên kết với nhau, mỗi nguyên tử góp 1 electron để tạo ra đôi electron dùng chung.
- Hạt nhân của hai nguyên tử Cl cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử chlorine.
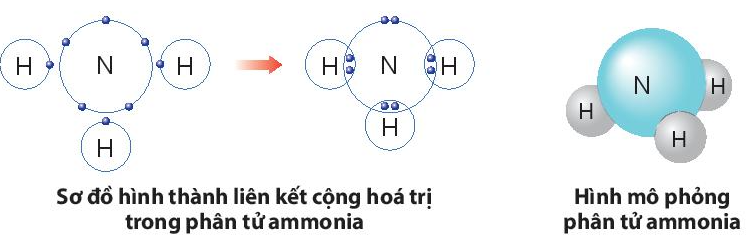
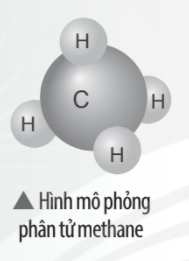
b) Sự hình thành liên kết trong phân tử ammonia.
- Nguyên tử N có 5 electron lớp ngoài cùng, cần thêm 3 electron để có lớp vỏ bền vững tương tự khí hiếm.
- Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
- Khi tạo thành phân tử NH3, nguyên tử N góp 3 electron, mỗi nguyên tử H góp 1 electron. Như vậy giữa nguyên tử N và mỗi nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử N và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử ammonia.
Trả lời:
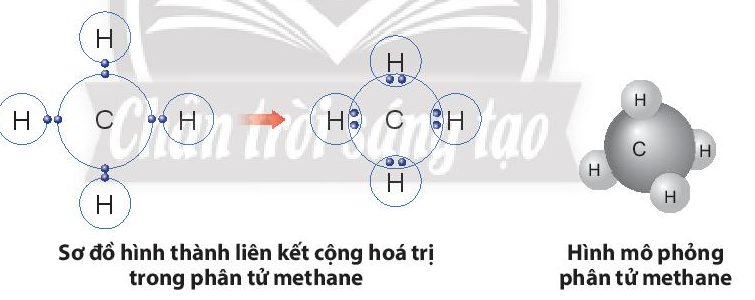
Sự hình thành liên kết trong phân tử methane:
- Nguyên tử C có 4 electron lớp ngoài cùng, cần thêm 4 electron để có lớp vỏ bền vững tương tự khí hiếm.
- Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
- Khi C kết hợp với H, nguyên tử C góp 4 electron, mỗi nguyên tử H góp 1 electron. Như vậy giữa nguyên tử C và mỗi nguyên tử H có 1 đôi electron dùng chung. Hạt nhân nguyên tử C và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử methane.
- Ứng dụng của methane:
+ Làm nhiên liệu đun nấu thay cho các nhiên liệu khác, thắp sáng.
+ Trong công nghiệp: dùng trong nhiều phản ứng hóa công nghiệp; làm nguyên liệu sản xuất hydrogen, methanol, acetic acid và acetic anhydride.
4. Chất ion, chất cộng hóa trị

Trả lời:
Hình 6.9 a) Phân tử sodium chloride (NaCl) được tạo bởi ion Na+ và Cl-;
Hình 6.9 b) Phân tử calcium chloride (CaCl2) được tạo bởi ion Ca2+ và Cl-;
Hình 6.9 c) Phân tử magnesium oxide (MgO) được tạo bởi ion Mg2+ và O2-;
Ở điều kiện thường, các chất này đều tồn tại ở thể rắn.
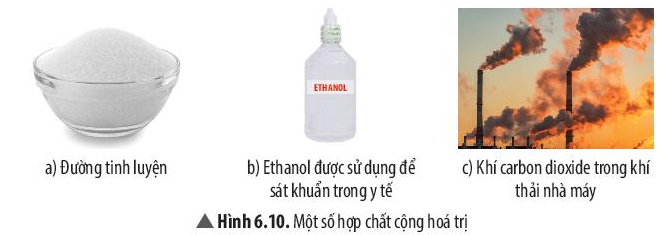
Câu hỏi thảo luận 11 trang 42 KHTN lớp 7: Quan sát và cho biết thể của các chất có trong Hình 6.10.
Trả lời:
- Hình 6.10 a) Đường tinh luyện ở thể rắn.
- Hình 6.10 b) Ethanol ở thể lỏng.
- Hình 6.10 c) Carbon dioxide ở thể khí.
Trả lời:
- Thể rắn: iodine, nước đá khô, …
- Thể lỏng: nước; ethanol; bromine …
- Thể khí: nitrogen; chlorine; sulfur dioxide …
a) Hãy cho biết chất nào là hợp chất ion, chất nào là hợp chất cộng hóa trị.
b) Nguyên tử của nguyên tố nào trong các chất trên có số electron ở lớp ngoài cùng nhiều nhất?

Trả lời:
a) Chất ion: sodium chloride (NaCl), potassium chloride (KCl);
Chất cộng hóa trị: hơi nước (H2O), carbon dioxide (CO2), sulfur dioxide (SO2)
b) Trong các chất trên nguyên tử của chlorine (Cl) có số electron ở lớp ngoài cùng nhiều nhất với 7 electron.
5. Một số tính chất của chất ion và chất cộng hóa trị
Trả lời:
|
Tính chất |
Muối |
Đường |
|
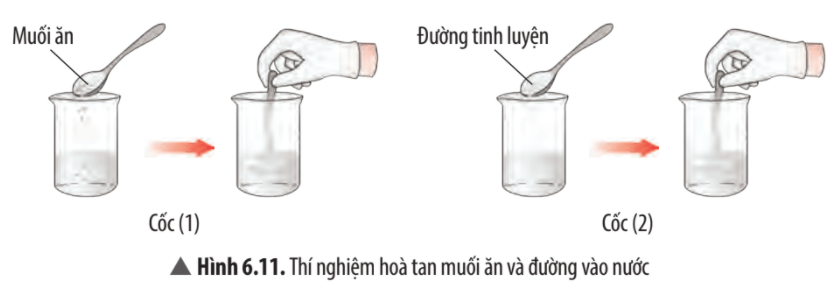
Tan trong nước |
√ |
√ |
|
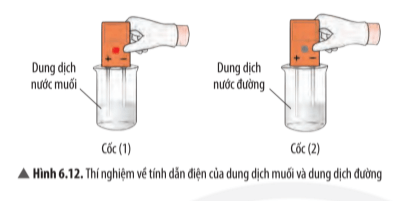
Dẫn điện được |
√ |
|
Trả lời:
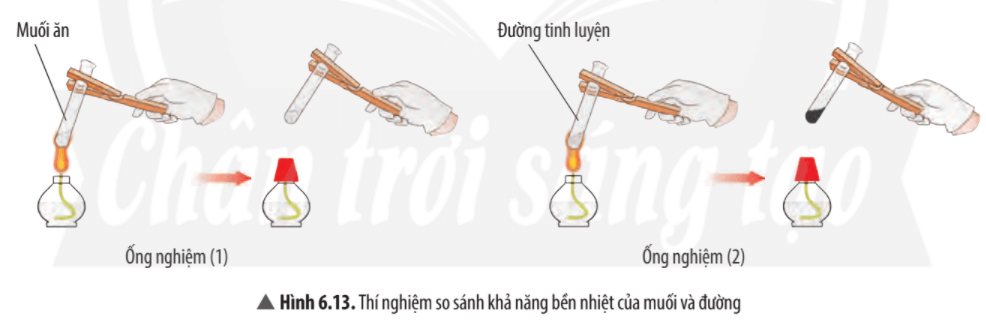
Quan sát thí nghiệm ta thấy muối ăn không bị nhiệt phân hủy (không bị biến đổi khi đun), đường bị nhiệt phân hủy thành chất mới có màu đen.
⇒ Muối ăn bền với nhiệt hơn đường.
Mở rộng: Đường nóng chảy ở 186oC, muối ăn (sodium chloride) nóng chảy ở 810oC. Ở thí nghiệm này nếu tăng thêm thời gian đun nóng, muối rắn sẽ nóng chảy ra thành lỏng. Tính chất này vẫn là tính chất vật lí.
Trả lời:
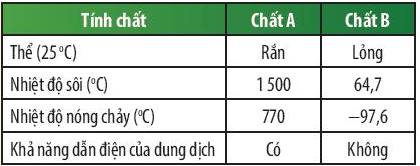
Dựa vào kết quả được trình bày ở bảng trên ta thấy: Chất A có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn rất nhiều so với chất B, chất A tồn tại ở thể rắn và dung dịch chất A có khả năng dẫn điện, dung dịch chất B không có khả năng dẫn điện.
⇒ Chất A là hợp chất ion, chất B là chất cộng hóa trị.
Dự đoán chất A có thể là potassium chloride; chất B có thể là methanol.
Trong trường hợp không có oresol thì có thể thay thế bằng cách nào khác không? Giải thích.
Trả lời:
Thành phần chính của oresol:
- Các hợp chất ion: Sodium chloride (NaCl); potassium chloride…
- Hợp chất cộng hóa trị: glucose.
 Một số loại oresol
Một số loại oresol
Công dụng chính của osresol là bổ sung nước và các chất điện giải cho cơ thể.
Trong trường hợp không có oresol thì có thể thay thế bằng:
- Nước muối đường: Có thành phần tương tự như oresol. Pha theo tỷ lệ 1 thìa cà phê muối, 8 thìa đường và 1 lít nước.
- Nước cháo muối (1,2 lít nước, 1 thìa muối, 1 nắm gạo), đồng thời uống bổ sung nước dừa, nước cam, ăn thêm chuối để bổ sung thêm potassium.
Bài tập (trang 44)
Trả lời:
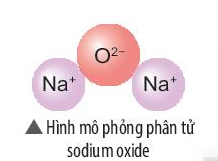
Sự tạo thành liên kết trong phân tử sodium oxide (Na2O)
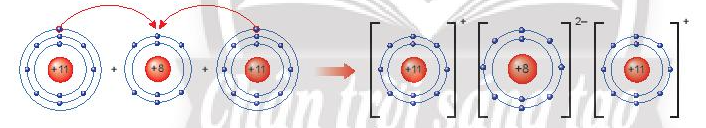 Khi nguyên tử sodum (Na) kết hợp với nguyên tử oxygen (O), 2 nguyên tử sodium mỗi nguyên tử nhường 1 electron tạo thành ion dương, kí hiệu là Na+, đồng thời nguyên tử oxygen (O) nhận 2 electron từ nguyên tử Na tạo thành ion âm, kí hiệu O2-. Hai ion Na+ và O2- hút nhau tạo phân tử sodium oxide (Na2O).
Khi nguyên tử sodum (Na) kết hợp với nguyên tử oxygen (O), 2 nguyên tử sodium mỗi nguyên tử nhường 1 electron tạo thành ion dương, kí hiệu là Na+, đồng thời nguyên tử oxygen (O) nhận 2 electron từ nguyên tử Na tạo thành ion âm, kí hiệu O2-. Hai ion Na+ và O2- hút nhau tạo phân tử sodium oxide (Na2O).
Trả lời:
Vị trí trong bảng tuần hoàn, số electron lớp ngoài cùng của nguyên tử mỗi nguyên tố N, C, O được xác định theo bảng sau:
|
Nguyên tố |
Vị trí các nguyên tố trong bảng tuần hoàn |
Số electron lớp ngoài cùng |
|
N |
Ô thứ 7, chu kì 2, nhóm VA |
5 |
|
C |
Ô thứ 6, chu kì 2, nhóm IVA |
4 |
|
O |
Ô thứ 8, chu kì 2, nhóm VIA |
6 |
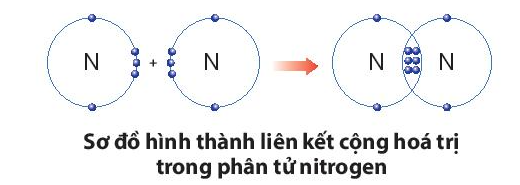
Sự tạo thành liên kết trong phân tử nitrogen:
+ Nguyên tử N có 5 electron lớp ngoài cùng, cần thêm 3 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử N liên kết với nhau, mỗi nguyên tử góp chung 3 electron để tạo ra 3 cặp electron dùng chung, theo sơ đồ sau:
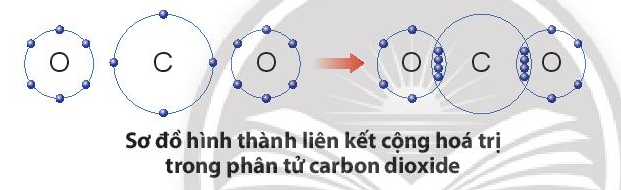
 Sự tạo thành liên kết trong phân tử carbon dioxide:
Sự tạo thành liên kết trong phân tử carbon dioxide:
+ Nguyên tử C có 4 electron ở lớp ngoài cùng và cần thêm 4 electron để đạt được lớp vỏ bền vững tương tự khí hiếm Ne.
+ Trong phân tử khí carbon dioxide, nguyên tử C góp 4 electron, mỗi nguyên tử O góp 2 electron. Như vậy, giữa nguyên tử C và O có hai đôi electron dùng chung theo sơ đồ sau:

Trả lời:
Hợp chất potassium chloride (KCl) có liên kết ion trong phân tử.
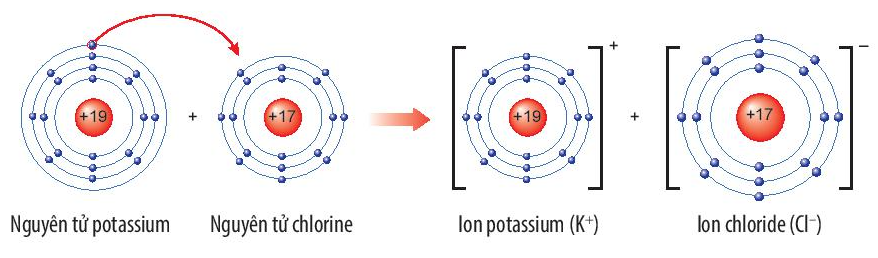
Sự hình thành liên kết trong phân tử potassium chloride
+ Nguyên tử K nhường đi 1 electron ở lớp ngoài cùng trở thành ion potassium, mang điện tích dương, kí hiệu là K+.
+ Nguyên tử Cl nhận 1 electron từ nguyên tử K trở thành ion chloride, mang điện tích âm, kí hiệu là Cl-.
Các ion K+ và Cl- hút nhau tạo thành liên kết trong phân tử potassium chloride.
Lý thuyết Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học
I. Vỏ nguyên tử khí hiếm
- Nhóm khí hiếm là nhóm các nguyên tố hoạt động hóa học kém.
Nhóm khí hiếm gồm: helium (He); neon (Ne); argon (Ar); krypton (Kr); xenon (Xe), …
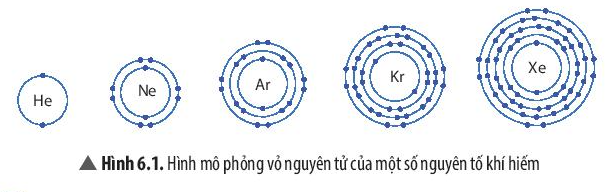 - Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng có 2 electron.
- Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng có 2 electron.
Chú ý:
Để có số electron ở lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm, các nguyên tử của các nguyên tố có khuynh hướng nhường hoặc nhận hoặc góp chung electron.
+ Nguyên tử của các nguyên tố kim loại thường có khuynh hướng nhường electron ở lớp ngoài cùng.
+ Nguyên tử của các nguyên tố phi kim thường có khuynh hướng nhận thêm hoặc góp chung electron để có lớp electron ngoài cùng bền vững.
II. Liên kết ion
1. Sự tạo thành ion dương
- Các nguyên tử của nguyên tố kim loại thường có xu hướng nhường electron ở lớp ngoài cùng để có lớp electron ngoài cùng giống nguyên tử của nguyên tố khí hiếm gần nhất trong bảng tuần hoàn.
- Nguyên tử kim loại khi nhường electron sẽ tạo thành ion dương tương ứng.
Ví dụ: Nguyên tử magnesium nhường 2 electron lớp ngoài cùng tạo thành ion magnesium. Ion magnesium là ion dương, có 8 electron lớp ngoài cùng, cấu hình electron giống với khí hiếm Ne.
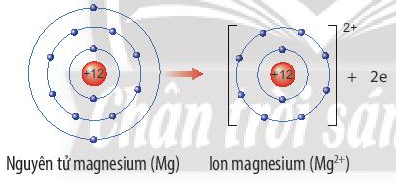
Hay viết gọn: Mg → Mg2+ + 2e
2. Sự tạo thành ion âm
- Các nguyên tử của nguyên tố phi kim (Cl, O, N …) có số electron lớp ngoài cùng là 7, 6, 5, … nên khi kết hợp với các nguyên tử kim loại, nguyên tử phi kim có xu hướng nhận electron từ nguyên tử kim loại để có lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm gần nhất trong bảng tuần hoàn.
- Nguyên tử phi kim khi nhận electron sẽ tạo thành ion âm tương ứng.
Ví dụ: Nguyên tử oxygen nhận thêm 2 electron vào lớp ngoài cùng tạo thành ion oxygen. Ion oxygen có 8 electron lớp ngoài cùng, cấu hình electron giống với nguyên tử khí hiếm Ne.
 Hay viết gọn: O + 2e → O2-
Hay viết gọn: O + 2e → O2-
3. Sự tạo thành liên kết ion
- Khi nguyên tử kim loại kết hợp với nguyên tử phi kim, nguyên tử kim loại nhường electron tạo thành ion dương, đồng thời nguyên tử phi kim nhận electron tạo thành ion âm.
- Ion âm và ion dương mang điện tích trái dấu, hút nhau, tạo thành liên kết ion.
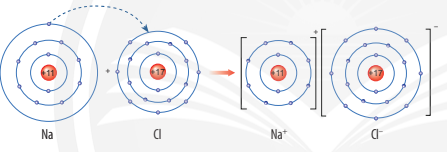
Ví dụ 1: Sơ đồ tạo thành liên kết ion trong phân tử NaCl (sodium chloride).
Nguyên tử sodium nhường 1 electron tạo thành ion sodium (điện tích dương), nguyên tử chlorine nhận 1 electron tạo thành ion chlorine (điện tích âm), hai ion trên trái dấu nên hút nhau tạo thành phân tử sodium chlorine.
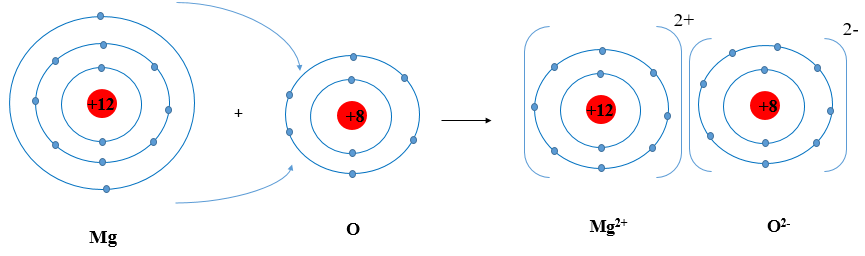
 Ví dụ 2: Sơ đồ tạo thành liên kết ion trong phân tử MgO (magnesium oxide).
Ví dụ 2: Sơ đồ tạo thành liên kết ion trong phân tử MgO (magnesium oxide).
Nguyên tử magnesium nhường 2 electron tạo thành ion magnesium (điện tích dương), nguyên tử oxygen nhận 2 electron tạo thành ion oxygen (điện tích âm), hai ion trên trái dấu nên hút nhau tạo thành phân tử magnesium oxide
Kết luận:
- Liên kết ion là liên kết giữa ion dương và ion âm.
- Các ion dương và ion âm đơn nguyên tử có lớp electron ngoài cùng giống với nguyên tử của nguyên tố khí hiếm.
III. Liên kết cộng hóa trị
- Liên kết cộng hóa trị là liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử.
- Liên kết cộng hóa trị thường là liên kết giữa hai nguyên tử của nguyên tố phi kim với phi kim.
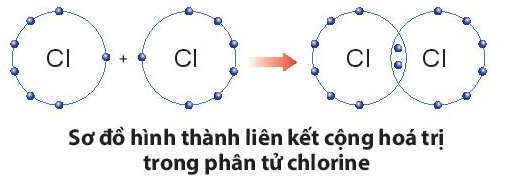
Ví dụ 1: Quá trình tạo thành liên kết cộng hóa trị trong phân tử chlorine:
+ Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử Cl liên kết với nhau, mỗi nguyên tử góp 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử Cl cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử chlorine.
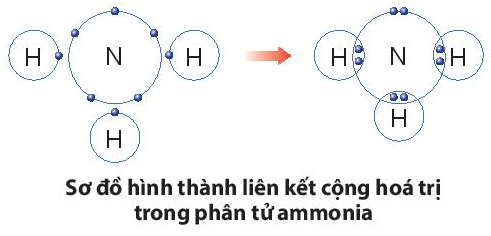
 Ví dụ 2: Quá trình tạo thành liên kết cộng hóa trị trong phân tử ammonia:
Ví dụ 2: Quá trình tạo thành liên kết cộng hóa trị trong phân tử ammonia:
+ Nitrogen thuộc nhóm VA, có 5 electron lớp ngoài cùng, nguyên tử nitrogen sẽ góp chung 3 electron.
+ Hydrogen thuộc nhóm IA, có 1 electron lớp ngoài cùng, mỗi nguyên tử hydrogen sẽ góp chung 1 electron, theo sơ đồ sau:
IV. Chất ion, chất cộng hóa trị
- Chất được tạo bởi các ion dương và ion âm được gọi là chất ion.
Ví dụ một số hợp chất ion:

- Chất được tạo thành nhờ liên kết cộng hóa trị được gọi là chất cộng hóa trị.
Ví dụ một số hợp chất cộng hóa trị:

- Ở điều kiện thường, chất ion thường ở thể rắn, chất cộng hóa trị ở thể rắn, thể lỏng hoặc thể khí.
V. Một số tính chất của chất ion và chất cộng hóa trị
- Chất ion khó bay hơi, khó nóng chảy, khi tan trong nước tạo dung dịch dẫn được điện.
- Chất cộng hóa trị thường dễ bay hơi, kém bền với nhiệt; một số chất tan được trong nước thành dung dịch. Tùy thuộc vào chất cộng hóa trị khi tan trong nước mà dung dịch thu được có thể dẫn điện hoặc không dẫn điện.
- Ví dụ 1: Dung dịch nước muối dẫn điện còn dung dịch nước đường thì không dẫn điện.
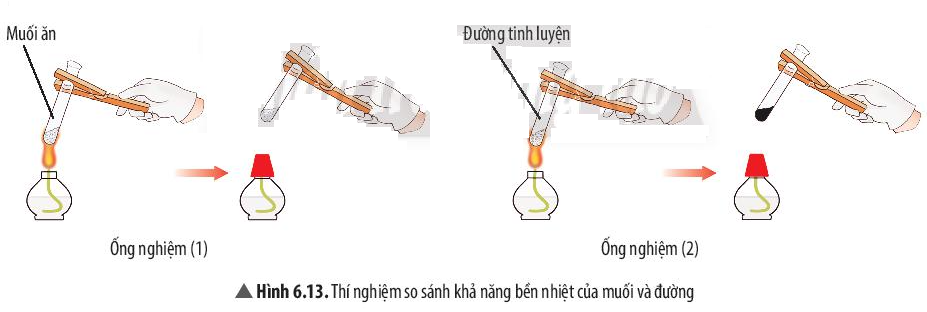
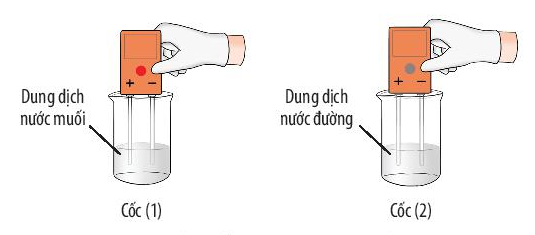 Ví dụ 2: Đường nóng chảy và biến đổi thành chất khác có màu đen. Muối ăn không bị nóng chảy.
Ví dụ 2: Đường nóng chảy và biến đổi thành chất khác có màu đen. Muối ăn không bị nóng chảy.
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Bài 7: Hóa trị và công thức hóa học
Bài 9: Đồ thị quãng đường - thời gian
Bài 11: Tốc độ và an toàn giao thông
Xem thêm tài liệu Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các chương trình khác:
- Giải sgk Toán 7 – Chân trời sáng tạo
- Giải sbt Toán 7 – Chân trời sáng tạo
- Lý thuyết Toán 7 – Chân trời sáng tạo
- Soạn văn lớp 7 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Soạn văn lớp 7 (ngắn nhất) – Chân trời sáng tạo
- Văn mẫu lớp 7 – Chân trời sáng tạo
- Giải sgk Lịch sử 7 – Chân trời sáng tạo
- Lý thuyết Lịch Sử 7 – Chân trời sáng tạo
- Giải sbt Lịch sử 7 – Chân trời sáng tạo
- Giải sgk Địa lí 7 – Chân trời sáng tạo
- Lý thuyết Địa Lí 7 – Chân trời sáng tạo
- Giải sbt Địa lí 7 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 7 Friend plus – Chân trời sáng tạo
- Giải sbt Tiếng Anh 7 Friend plus– Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 7 Friends plus đầy đủ nhất
- Bài tập Tiếng Anh 7 Friends plus theo Unit có đáp án
- Giải sgk Giáo dục công dân 7 – Chân trời sáng tạo
- Lý thuyết Giáo dục công dân 7 – Chân trời sáng tạo
- Giải sbt Giáo dục công dân 7 – Chân trời sáng tạo
- Giải sgk Công nghệ 7 – Chân trời sáng tạo
- Lý thuyết Công nghệ 7 – Chân trời sáng tạo
- Giải sbt Công nghệ 7 – Chân trời sáng tạo
- Giải sgk Tin học 7 – Chân trời sáng tạo
- Lý thuyết Tin học 7 – Chân trời sáng tạo
- Giải sbt Tin học 7 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 7 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 7 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 7 – Chân trời sáng tạo
- Giải sgk Âm nhạc 7 – Chân trời sáng tạo