Giải Khoa học tự nhiên 7 Bài 2 (Chân trời sáng tạo): Nguyên tử
Với lời giải bài tập Khoa học tự nhiên lớp 7 Bài 2: Nguyên tử sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi và làm bài tập KHTN 7 Bài 2.
Giải bài tập Khoa học tự nhiên 7 Bài 2: Nguyên tử
Video giải bài tập Khoa học tự nhiên 7 Bài 2: Nguyên tử

Trả lời:
Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó gọi là nguyên tử.
1. Mô hình nguyên tử Rutherford – Bohr

Trả lời:
Quan sát bằng mắt thường: Ruột bút chì
Quan sát bằng kính lúp: Hạt bụi trong không khí
Quan sát bằng kính hiển vi: Tế bào máu, vi khuẩn.
Trả lời:
Khí oxygen, sắt, than chì đều được tạo nên từ những hạt vô cùng nhỏ, gọi là nguyên tử.
Câu hỏi thảo luận 3 trang 15 KHTN lớp 7: Theo Rutherford – Bohr, nguyên tử có cấu tạo như thế nào?
Trả lời:
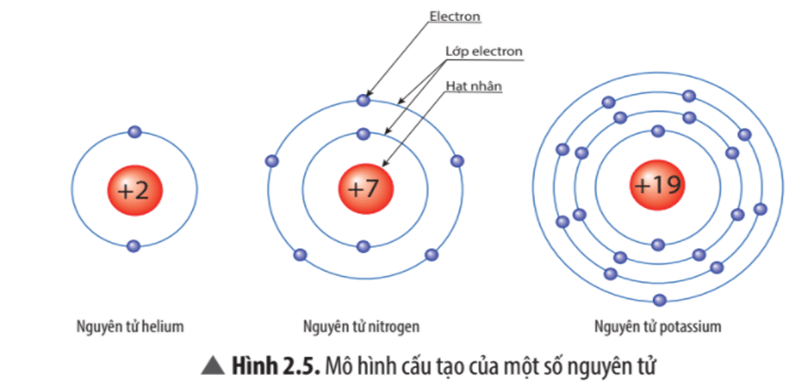
Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm hạt nhân ở bên trong và lớp vỏ tạo bởi một hay nhiều electron (kí hiệu là e) mang điện tích âm. Bên trong hạt nhân chứa các hạt proton (kí hiệu là p) mang điện tích dương.
Các electron được sắp xếp thành từng lớp và chuyển động xung quanh hạt nhân theo quỹ đạo tương tự như hành tinh trong hệ Mặt Trời.
a) điện tích hạt nhân nguyên tử?
Trả lời:
|
|
Nguyên tử nitrogen |
Nguyên tử potassium |
|
Điện tích hạt nhân nguyên tử |
+7 |
+19 |
|
Lớp electron |
2 |
4 |
|
Electron trên mỗi lớp |
2/5 |
2/8/8/1 |
Câu hỏi thảo luận 5 trang 16 KHTN lớp 7: Tại sao nguyên tử trung hòa về điện?
Trả lời:
Mỗi electron mang điện tích -1, mỗi proton mang điện tích +1, mà trong nguyên tử, số hạt proton và electron luôn bằng nhau do đó nguyên tử trung hòa về điện.
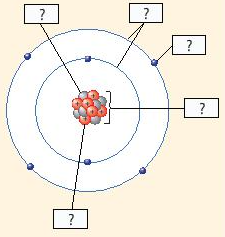 Trả lời:
Trả lời:
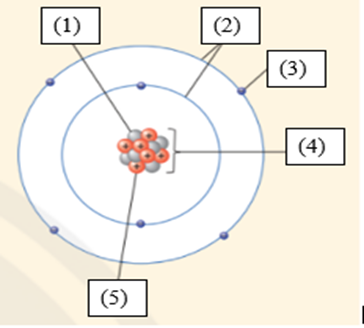
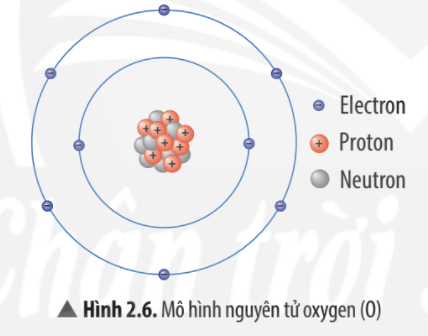
(1) Neutron
(2) Vỏ nguyên tử
(3) Electron
(4) Hạt nhân nguyên tử
(5) Proton
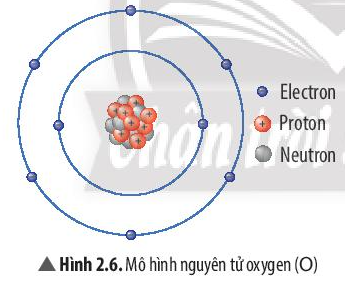
Luyện tập 2 trang 16 KHTN lớp 7: Quan sát Hình 2.6, hãy hoàn thành bảng sau:
Trả lời:
|
Số đơn vị điện tích hạt nhân |
Số proton |
Số electron trong nguyên tử |
Số electron ở lớp ngoài cùng |
|
8 |
8 |
8 |
6 |
Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa là 8 thì cần thêm 2 electron nữa.
2. Khối lượng nguyên tử
Trả lời:
Khối lượng của nguyên tử rất nhỏ, không thể cân đo dễ dàng bằng các dụng cụ bình thường (theo khối lượng g hay kg), bên cạnh đó phải sử dụng số mũ, lũy thừa âm lớn cho các đơn vị g hay kg nên không thuận tiện.Vì thế để biểu thị khối lượng nguyên tử người ta sử dụng đơn vị khối lượng nguyên tử, viết tắt là amu (atomic mass unit).
1 amu = 1,6605 × 10-24 gam
Trả lời:
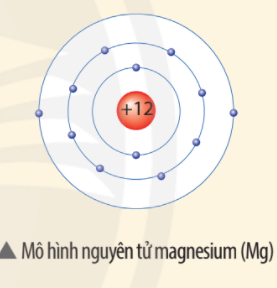
Điện tích hạt nhân nguyên tử Mg là +12.
⇒ Một nguyên tử magnesium (Mg) gồm: 12 proton, 12 electron.
Khối lượng nguyên tử Mg bằng 12 + 12 = 24 amu.
(do khối lượng 1p = 1n = 1 amu).
Bài tập (trang 17)
|
|
Trong nguyên tử, các electron (8) … xung quanh hạt nhân và (9) … thành từng lớp.
Trả lời:
(1) vô cùng nhỏ
(2) trung hòa về điện
(3) hạt nhân
(4) điện tích dương
(5) vỏ nguyên tử
(6) các electron
(7) điện tích âm
(8) chuyển động
(9) sắp xếp
Bài 2 trang 17 KHTN lớp 7: Vì sao nói khối lượng hạt nhân được coi là khối lượng nguyên tử?
Trả lời:
Proton và neutron có khối lượng xấp xỉ bằng nhau (gần bằng 1 amu). Electron có khối lượng rất bé (chỉ khoảng bằng 0,00055 amu), nhỏ hơn rất nhiều lần so với khối lượng của proton và neutron. Do đó khối lượng hạt nhân được coi là khối lượng nguyên tử.
Lý thuyết Khoa học tự nhiên 7 Bài 2: Nguyên tử
I. Mô hình nguyên tử Rutherford – Bohr
1. Sơ lược về nguyên tử
- Nguyên tử có kích thước vô cùng nhỏ, tạo nên các chất.
Ví dụ:
+ Kim cương được cấu tạo nên từ các nguyên tử carbon.

Chú ý: Không thể quan sát nguyên tử bằng kính hiển vi quang học thông thường. Người ta sử dụng kính hiển vi điện tử với độ phóng đại lớn để quan sát nguyên tử.
2. Khái quát về mô hình nguyên tử
∎ Theo Ernest Rutherford (1871 – 1937):
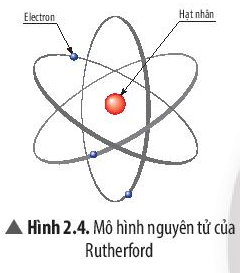 - Nguyên tử có cấu tạo gồm:
- Nguyên tử có cấu tạo gồm:
+ Vỏ tạo bởi một hay nhiều electron (kí hiệu là e), mỗi electron mang điện tích -1.
+ Hạt nhân ở bên trong chứa các hạt proton (kí hiệu là p), mỗi proton mang điện tích +1.
- Trong nguyên tử, số proton = số electron nên nguyên tử trung hòa về điện.
- Trong hạt nhân nguyên tử:
+ Điện tích hạt nhân = tổng điện tích các hạt proton.
+ Số đơn vị điện tích hạt nhân = số proton.
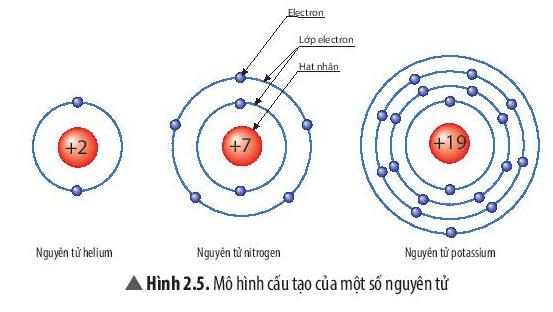
∎ Sau này, dựa trên mô hình của Rutherford, Niels Bohr đã phát triển một mô hình hoàn thiện hơn về nguyên tử:
- Mô hình Rutherford – Bohr: Trong nguyên tử, các electron ở vỏ được xếp thành từng lớp và chuyển động xung quanh hạt nhân theo những quỹ đạo như các hành tinh quay xung quanh Mặt Trời.
 Chú ý:
Chú ý:
Các electron chuyển động rất nhanh xung quanh hạt nhân và phân bố thành từng lớp với số lượng electron nhất định.
+ Lớp đầu tiên gần sát hạt nhân chứa tối đa 2 electron.
+ Lớp thứ hai chứa tối đa 8 electron, …
∎ Năm 1932, sau khi nghiên cứu sâu hơn về nguyên tử bằng các thiết bị tiên tiến, James Chadwick (1891 – 1974) đã phát hiện ra bên trong hạt nhân còn có hạt không mang điện, gọi là neutron.
 II. Khối lượng nguyên tử
II. Khối lượng nguyên tử
- Khối lượng nguyên tử là khối lượng của một nguyên tử, bằng tổng khối lượng các hạt (proton, neutron và electron) có trong nguyên tử.
- Tuy nhiên, khối lượng nguyên tử rất nhỏ nên để biểu thị khối lượng nguyên tử người ta sử dụng đơn vị khối lượng nguyên tử, viết tắt là amu (atomic mass unit, 1 amu = 1,6605 × 10-24 gam).
- Proton và neutron có khối lượng xấp xỉ nhau (gần bằng 1 amu); electron có khối lượng rất bé (chỉ bằng khoảng 0,00055 amu). Do đó, có thể xem như khối lượng của hạt nhân là khối lượng của nguyên tử.
- Cách tính: Khối lượng nguyên tử = số proton + số neutron.
Ví dụ: Nguyên tử magnesium (Mg) trong hạt nhân có 12 proton và 12 neutron
⇒ Khối lượng nguyên tử magnesium (Mg) = 12 + 12 = 24 (amu)
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Sơ lược bảng tuần hoàn các nguyên tố hóa học
Bài 5: Phân tử - Đơn chất – Hợp chất
Bài 6: Giới thiệu về liên kết hóa học
Bài 7: Hóa trị và công thức hóa học
Xem thêm tài liệu Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các chương trình khác:
- Giải sgk Toán 7 – Chân trời sáng tạo
- Giải sbt Toán 7 – Chân trời sáng tạo
- Lý thuyết Toán 7 – Chân trời sáng tạo
- Soạn văn lớp 7 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 7 – Chân trời sáng tạo
- Soạn văn lớp 7 (ngắn nhất) – Chân trời sáng tạo
- Văn mẫu lớp 7 – Chân trời sáng tạo
- Giải sgk Lịch sử 7 – Chân trời sáng tạo
- Lý thuyết Lịch Sử 7 – Chân trời sáng tạo
- Giải sbt Lịch sử 7 – Chân trời sáng tạo
- Giải sgk Địa lí 7 – Chân trời sáng tạo
- Lý thuyết Địa Lí 7 – Chân trời sáng tạo
- Giải sbt Địa lí 7 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 7 Friend plus – Chân trời sáng tạo
- Giải sbt Tiếng Anh 7 Friend plus– Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 7 Friends plus đầy đủ nhất
- Bài tập Tiếng Anh 7 Friends plus theo Unit có đáp án
- Giải sgk Giáo dục công dân 7 – Chân trời sáng tạo
- Lý thuyết Giáo dục công dân 7 – Chân trời sáng tạo
- Giải sbt Giáo dục công dân 7 – Chân trời sáng tạo
- Giải sgk Công nghệ 7 – Chân trời sáng tạo
- Lý thuyết Công nghệ 7 – Chân trời sáng tạo
- Giải sbt Công nghệ 7 – Chân trời sáng tạo
- Giải sgk Tin học 7 – Chân trời sáng tạo
- Lý thuyết Tin học 7 – Chân trời sáng tạo
- Giải sbt Tin học 7 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 7 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 7 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 7 – Chân trời sáng tạo
- Giải sgk Âm nhạc 7 – Chân trời sáng tạo