TOP 20 câu Trắc nghiệm Khoa học tự nhiên 7 Bài 6 (Chân trời sáng tạo 2024) có đáp án: Giới thiệu về liên kết hóa học
Bộ 20 bài tập trắc nghiệm Khoa học tự nhiên lớp 7 Bài 6: Giới thiệu về liên kết hóa học có đáp án đầy đủ các mức độ sách Chân trời sáng tạo giúp học sinh ôn luyện trắc nghiệm Khoa học tự nhiên 7 Bài 6.
Chỉ 100k mua trọn bộ Trắc nghiệm Khoa học tự nhiên lớp 7 Chân trời sáng tạo bản word (cả năm) có đáp án chi tiết:
B1: Gửi phí vào tài khoản 033000255833 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu
Trắc nghiệm Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học – Chân trời sáng tạo
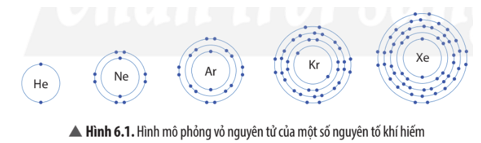
Câu 1. Cho mô hình sắp xếp các electron trong vỏ nguyên tử của các nguyên tố khí hiếm.
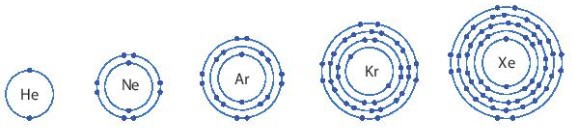
Trừ helium, vỏ nguyên tử của các nguyên tố còn lại có điểm giống nhau là
A. Đều có cùng số lớp electron.
B. Đều có 8 electron ở lớp ngoài cùng.
C. Đều có cùng số electron.
D. Đều có 2 electron ở lớp ngoài cùng.
Đáp án: B
Giải thích:
Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng chỉ có 2 electron.
Câu 2. Cho mô hình sắp xếp các electron trong vỏ nguyên tử Mg và nguyên tử Ne:
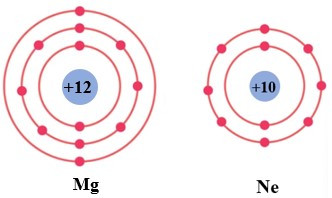
Để đạt được lớp vỏ bền vững giống vỏ nguyên tử khí hiếm Ne thì nguyên tử Mg cần nhường hay nhận bao nhiêu electron?
A. Nhường 2 electron.
B. Nhường 6 electron.
C. Nhận 2 electron.
D. Nhận 6 electron.
Đáp án: A
Giải thích:
Để đạt được lớp vỏ bền vững giống vỏ nguyên tử khí hiếm Ne thì nguyên tử Mg cần nhường 2 electron.
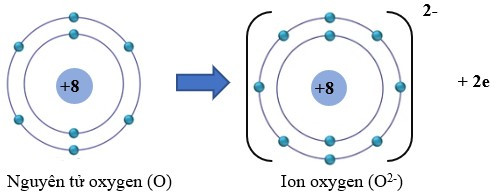
Câu 3. Cho mô hình sắp xếp các electron trong vỏ nguyên tử oxygen (O):
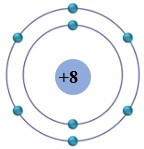
Khi tham gia hình thành liên kết ion, nguyên tử oxygen có xu hướng nhận thêm 2 electron để tạo thành ion
A. O2+.
B. O-.
C. O2-.
D. O+.
Đáp án: C
Giải thích:
Khi tham gia hình thành liên kết ion, nguyên tử aluminum có xu hướng nhận thêm 2 electron để tạo thành ion O2-.
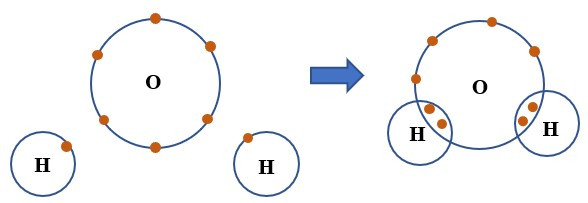
Câu 4. Phân tử nước gồm một nguyên tử oxygen liên kết với hai nguyên tử hydrogen. Khi hình thành liên kết cộng hóa trị trong phân tử nước, nguyên tử oxygen góp chung bao nhiêu electron với mỗi nguyên tử hygrogen?
A. Nguyên tử oxygen góp chung 4 electron với mỗi nguyên tử hygrogen.
B. Nguyên tử oxygen góp chung 3 electron với mỗi nguyên tử hygrogen.
C. Nguyên tử oxygen góp chung 2 electron với mỗi nguyên tử hygrogen.
D. Nguyên tử oxygen góp chung 1 electron với mỗi nguyên tử hygrogen.
Đáp án: D
Giải thích:
Mỗi nguyên tử oxygen có 6 electron ở lớp ngoài cùng, mỗi nguyên tử hydrogen có 1 electron ở lớp ngoài cùng. Để có cấu trúc bền vững của khí hiếm, khi hình thành phân tử nước, hai nguyên tử hydrogen đã liên kết với một nguyên tử oxygen bằng cách nguyên tử oxygen góp chung với mỗi nguyên tử hygrogen 1 electron tạo thành cặp electron dùng chung.
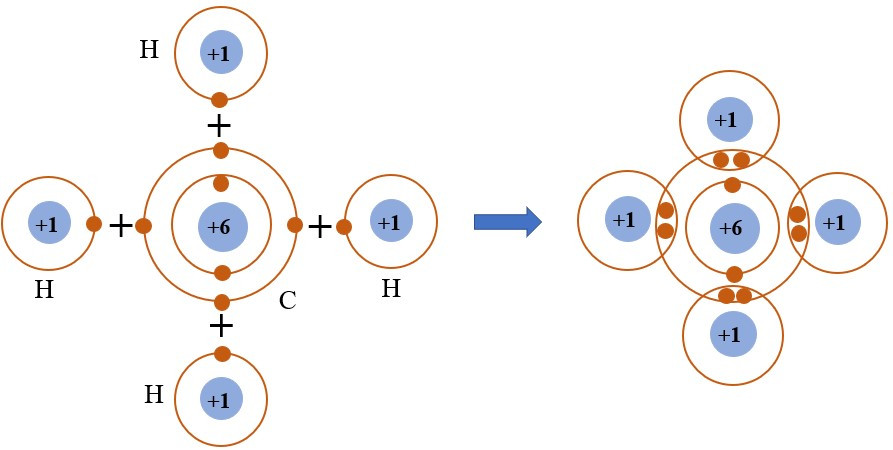
Câu 5. Cho hình mô phỏng phân tử methane:
Liên kết giữa các nguyên tử trong phân tử methane là liên kết
A. kim loại.
B. ion.
C. cộng hóa trị.
D. phi kim.
Đáp án: C
Giải thích:
Liên kết giữa các nguyên tử trong phân tử nước là liên kết cộng hóa trị. Khi hình thành phân tử methane, bốn nguyên tử hydrogen đã liên kết với một nguyên tử carbon bằng cách nguyên tử carbon góp chung với mỗi nguyên tử hygrogen 1 electron tạo thành cặp electron dùng chung.
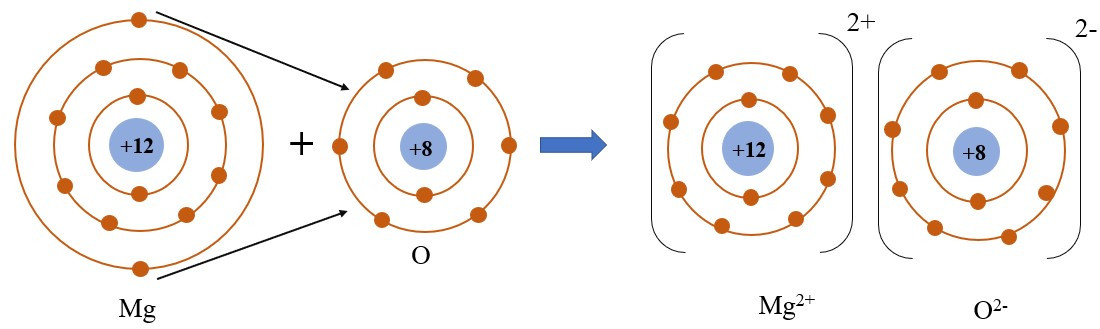
Câu 6. Trong phân tử MgO, nguyên tử Mg (magnesium) và nguyên tử O (oxygen) liên kết với nhau bằng liên kết
A. ion.
B. cộng hóa trị.
C. kim loại.
D. phi kim.
Đáp án: A
Giải thích:
Trong phân tử MgO, nguyên tử Mg (magnesium) và nguyên tử O (oxygen) liên kết với nhau bằng liên kết ion:
+ Nguyên tử Mg nhường 2 electron ở lớp electron ngoài cùng cho nguyên tử O để tạo thành ion dương Mg2+.
+ Nguyên tử O nhận vào ở lớp electron ngoài cùng 2 electron của nguyên tử Mg để tạo thành ion âm O2-.
+ Hai ion Mg2+ và O2- được tạo thành mang điện tích ngược dấu hút nhau để hình thành liên kết ion trong phân tử MgO.
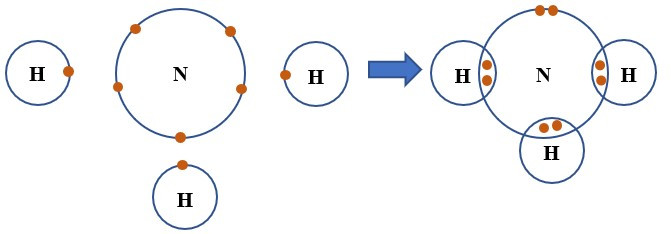
Câu 7. Liên kết hóa học giữa các nguyên tử nitrogen và hydrogen trong phân tử ammonia được hình thành bằng cách
A. Nguyên tử nitrogen và hydrogen góp chung proton.
B. Nguyên tử nitrogen và hydrogen góp chung electron.
C. Nguyên tử nitrogen nhận electron, nguyên tử hydrogen nhường electron.
D. Nguyên tử nitrogen nhường electron, nguyên tử hydrogen nhận electron.
Đáp án: B
Giải thích:
Khi hình thành phân tử amonia, ba nguyên tử H đã liên kết với một nguyên tử N bằng cách nguyên tử N góp chung với mỗi nguyên tử H một electron tạo thành cặp electron dùng chung.
Câu 8. Cho sơ đồ sự hình thành liên kết trong phân tử sodium chloride:
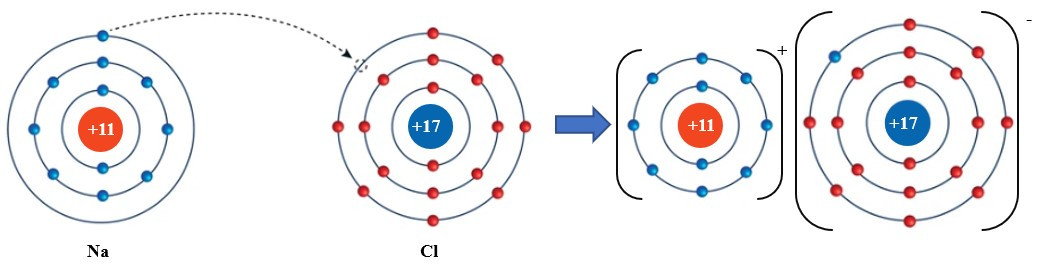
Nhận định nào sau đây sai?
A. Liên kết trong phân tử sodium chloride là liên kết ion.
B. Nguyên tử Na nhường 1 electron để tạo thành ion Na+.
C. Ion Na+ và Cl- góp chúng electron để tạo thành liên kết.
D. Nguyên tử Cl nhận 1 electron để tạo thành ion Cl-.
Đáp án: C
Giải thích:
Trong phân tử NaCl, nguyên tử Na và nguyên tử Cl liên kết với nhau bằng liên kết ion:
+ Nguyên tử Na nhường 1 electron ở lớp electron ngoài cùng cho nguyên tử Cl để tạo thành ion dương Na+.
+ Nguyên tử Cl nhận vào lớp electron ngoài cùng 1 electron của nguyên tử Na để tạo thành ion âm Cl-.
+ Hai ion Na+ và Cl- được tạo thành mang điện tích ngược dấu hút nhau để hình thành liên kết ion trong phân tử NaCl.
Câu 9. Khói của núi lửa ngầm phun trào từ dưới biển có chứa một số chất như: hơi nước, sodium chloride, potassium chloride, carbon dioxide, sulfur dioxide. Số chất là hợp chất cộng hóa trị là
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án: B
Giải thích:
Chất được tạo thành nhờ liên kết ion được gọi là chất ion.
Chất ion là sodium chloride, potassium chloride.
Chất được tạo thành nhờ liên kết cộng hóa trị được gọi là chất cộng hóa trị.
Chất cộng hóa trị là hơi nước, carbon dioxide, sulfur dioxide.
Câu 10. Kết quả thử thí nghiệm tính chất của 4 chất (1), (2), (3) và (4) được trình bày ở bảng sau:
|
Tính chất |
Chất (1) |
Chất (2) |
Chất (3) |
Chất (4) |
|
Thể (25oC) |
Rắn |
Lỏng |
Lỏng |
Khí |
|
Nhiệt độ sôi (oC) |
1500 |
64,7 |
78,4 |
-192 |
|
Nhiệt độ nóng chảy (oC) |
770 |
-97,6 |
-114,1 |
-205 |
|
Khả năng dẫn điện của dung dịch |
Có |
Không |
Không |
Không |
Chất ion là
A. (1).
B. (2).
C. (3).
D. (4).
Đáp án: A
Giải thích:
Chất ion khó nay hơi, khó nóng chảy, khi tan trong nước tạo dung dịch dẫn được điện.
Chất (1) có nhiệt độ nóng chảy, nhiệt độ sôi cao, khi tan trong nước tạo dung dịch dẫn được điện Chất (1) là chất ion
Chất cộng hóa trị thường dễ bay hơi, kém bền với nhiệt, một số chất tan được trong nước thành dung dịch. Tùy thuộc vào chất cộng hóa trị khi tan trong nước mà dung dịch thu được có thể dẫn điện hoặc không dẫn điện.
Chất (2), (3), (4) có nhiệt độ nóng chảy, nhiệt độ sôi thấp, khi tan trong nước tạo dung dịch không dẫn được điện Chất (2), (3), (4) là chất cộng hóa trị.
Câu 11. Vỏ nguyên tử của các nguyên tố khí hiếm thường chứa bao nhiêu electron ở lớp ngoài cùng?
A. 5;
B. 6;
C. 7;
D. 8.
Đáp án đúng là: D
Nhóm khí hiếm là nhóm các nguyên tố hoạt động hóa học kém gồm các nguyên tố: helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe),…
Vỏ nguyên tử của các nguyên tố khí hiếm thường chứa 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng chỉ có 2 electron.
Câu 12. Trong các phản ứng hóa học, nguyên tử kim loại có khuynh hướng
A. Nhận thêm electron;
B. Nhận hay nhường electron phụ thuộc vào từng phản ứng cụ thể;
C. Nhường bớt electron;
D. Nhận hay nhường electron phụ thuộc vào từng kim loại cụ thể.
Đáp án đúng là: C
Kim loại thường có 1, 2, 3 electron lớp ngoài cùng nên sẽ có khuynh hướng nhường electron.
Câu 13. Trong các phản ứng hóa học, nguyên tử phi kim có khuynh hướng
A. Nhận thêm electron;
B. Nhận hay nhường electron phụ thuộc vào từng phản ứng cụ thể;
C. Nhường bớt electron;
D. Nhận hay nhường electron phụ thuộc vào từng kim loại cụ thể.
Đáp án đúng là: C
Phi kim thường có 5, 6, 7 electron lớp ngoài cùng nên sẽ có khuynh hướng nhận electron.
Câu 14. Cho các ion: K+, Mg2+, SO42-, Cl-, NH4+, NO3-. Có bao nhiêu ion dương?
A. 3;
B. 4;
C. 5;
D. 6.
Đáp án đúng là: A
Các ion dương là K+, Mg2+, NH4+.
Câu 15. Cho các ion: Na+, SO42-, Fe3+, Cl-, NH4+, NO3-. Có bao nhiêu ion âm?
A. 3;
B. 4;
C. 5;
D. 6.
Đáp án đúng là: A
Các ion âm là SO42-, Cl-, NO3-.
Câu 16. Liên kết ion là liên kết được hình thành bởi:
A. Sự dùng chung electron giữa hai nguyên tử;
B. Sự cho nhận của cặp electron hóa trị;
C. Liên kết giữa ion dương và ion âm;
D. Liên kết giữa các ion dương trong phân tử.
Đáp án đúng là: C
Liên kết ion là liên kết giữa ion dương và ion âm.
Câu 17. Liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử là liên kết nào?
A. Liên kết ion;
B. Liên kết cộng hóa trị;
C. Liên kết hydrogen;
D. Liên kết kim loại.
Đáp án đúng là: B
Liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử là liên kết cộng hóa trị. Liên kết cộng hóa trị thường là liên kết giữa hai nguyên tử của nguyên tố phi kim với phi kim.
Ví dụ: Phân tử nước (H2O) có liên kết cộng hóa trị giữa nguyên tử hydrogen và oxygen.
Câu 18. Phát biểu nào sau đây là đúng về chất ion?
A. Chất ion là chất được tạo bởi các ion dương và ion âm;
B. Ở điều kiện thường, chất ion thường ở thể rắn, lỏng, khí;
C. Chất ion dễ bay hơi, kém bền nhiệt;
D. Chất ion không tan được trong nước.
Đáp án đúng là: A
Ở điều kiện thường, chất ion thường ở thể rắn.
Chất ion khó bay hơi, khó nóng chảy.
Chất ion khi tan trong nước tạo thành dung dịch dẫn được điện.
Câu 19. Phát biểu nào sau đây là sai về chất cộng hóa trị?
A. Chất cộng hóa trị là chất được tạo thành nhờ liên kết cộng hóa trị;
B. Ở điều kiện thường, chất cộng hóa trị có thể ở thể rắn, lỏng, khí;
C. Chất cộng hóa trị thường dễ bay hơi, kém bền nhiệt;
D. Chất cộng hóa trị không tan được trong nước.
Đáp án đúng là: D
Một số chất cộng hóa trị tan được trong nước thành dung dịch. Tùy thuộc vào chất cộng hóa trị khi tan trong nước mà dung dịch thu được có thể dẫn điện hoặc không dẫn điện.
Ví dụ: Đường tinh luyện (saccharose) tan được trong nước tạo thành dung dịch. Dung dịch saccharose không dẫn điện.
Câu 20. Nhóm hợp chất nào sau đây đều là hợp chất ion?
A. H2S, Na2O;
B. CH4, CO2;
C. CaO, KCl;
D. SO2, NaCl.
Đáp án đúng là: C
H2S, CH4, CO2, SO2 là các hợp chất cộng hóa trị.
Các câu hỏi trắc nghiệm Khoa học tự nhiên lớp 7 sách Chân trời sáng tạo có đáp án, chọn lọc khác:
Trắc nghiệm Bài 7: Hóa trị và công thức hóa học
Trắc nghiệm Bài 5: Phân tử - Đơn chất – Hợp chất
Trắc nghiệm Bài 3: Nguyên tố hóa học
Trắc nghiệm Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Xem thêm các chương trình khác: