TOP 20 câu Trắc nghiệm Khoa học tự nhiên 7 Bài 7 (Chân trời sáng tạo 2024) có đáp án: Hóa trị và công thức hóa học
Bộ 20 bài tập trắc nghiệm Khoa học tự nhiên lớp 7 Bài 7: Hóa trị và công thức hóa học có đáp án đầy đủ các mức độ sách Chân trời sáng tạo giúp học sinh ôn luyện trắc nghiệm Khoa học tự nhiên 7 Bài 7.
Chỉ 100k mua trọn bộ Trắc nghiệm Khoa học tự nhiên lớp 7 Chân trời sáng tạo bản word (cả năm) có đáp án chi tiết:
B1: Gửi phí vào tài khoản 033000255833 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu
Trắc nghiệm Khoa học tự nhiên 7 Bài 7: Hóa trị và công thức hóa học – Chân trời sáng tạo
Câu 1. Cho hình mô phỏng phân tử ammonia:
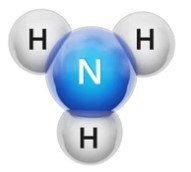
Hóa trị của nguyên tố nitrogen trong phân tử ammonia là
A. I.
B. II.
C. III.
D. IV.
Đáp án: C
Giải thích:
Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I, hóa trị của O là II.
Trong phân tử ammonia, nguyên tử N liên kết với 3 nguyên tử H (mỗi nguyên tử H hóa trị I) nên hóa trị của nguyên tử N là III.
Câu 2. Cho hình mô phỏng phân tử silicon dioxide:
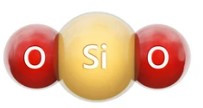
Trong tự nhiên, silicon dioxide có nhiều trong cát, đất sét, ... Hóa trị của nguyên tố silicon trong phân tử silicon dioxide là
A. IV.
B. III.
C. II.
D. I.
Đáp án: A
Giải thích:
Để xác định hóa trị của nguyên tố trong hợp chất cộng hóa trị, người ta dựa vào hóa trị của nguyên tố đã biết làm đơn vị, chẳng hạn hóa trị của H là I, hóa trị của O là II.
Trong phân tử silicon dioxide, nguyên tử Si liên kết với 2 nguyên tử O (mỗi nguyên tử O hóa trị II) nên hóa trị của nguyên tử Si là IV.
Câu 3. Phân tử khí ozone được tạo thành từ 3 nguyên tử ozone liên kết với nhau. Công thức hóa học của phân tử khí ozone là
A. 3O.
B. O3.
C. O3.
D. O3.
Đáp án: B
Giải thích:
Công thức hóa học dùng để biểu diễn chất, gồm một hoặc nhiều kí hiệu nguyên tố và chỉ số ở bên dưới mỗi kí hiệu.
Công thức hóa học của phân tử khí ozone là O3.
Câu 4. Phân tử methane gồm một nguyên tử carbon liên kết với 4 nguyên tử oxygen. Công thức hóa học của phân tử methane là
A. C4H.
B. C2H2.
C. C4H.
D. CH4.
Đáp án: D
Giải thích:
Công thức hóa học dùng để biểu diễn chất, gồm một hoặc nhiều kí hiệu nguyên tố và chỉ số ở bên dưới mỗi kí hiệu.
Công thức hóa học của phân tử methane là CH4.
Câu 5. Công thức hóa học của iron(III) oxide là Fe2O3. Nhận định nào sau đây là sai?
A. Iron(III) oxide do hai nguyên tố Fe, O tạo ra.
B. Trong một phân tử iron(III) oxide có hai nguyên tử Fe, ba nguyên tử O.
C. Khối lượng phân tử iron(III) oxide là 160 amu.
D. Trong phân tử iron(III) oxide tỉ lệ số nguyên tử Fe : O là 3 : 2.
Đáp án: D
Giải thích:
Iron(III) oxide do hai nguyên tố Fe, O tạo ra ® A đúng
Trong một phân tử iron(III) oxide có hai nguyên tử Fe, ba nguyên tử O ® B đúng
Khối lượng phân tử iron(III) oxide là:
2.56 + 3.16 = 160 amu ® C đúng
Trong phân tử iron(III) oxide tỉ lệ số nguyên tử Fe : O là 2 : 3 ® D sai
Câu 6. Một hợp chất có công thức NxOy, trong đó N chiếm 30,43%. Khối lượng phân tử hợp chất là 46 amu. Công thức hóa học của hợp chất là
A. N2O.
B. NO2.
C. N2O3.
D. N2O5.
Đáp án: B
Giải thích:
Ta có %O = 100% - %N = 100% - 30,43% = 69,57%.
%N = ×100% = ×100% = 30,43%
® x = 1
%O = ×100% = ×100% = 69,57%
® x = 2
Công thức hóa học của hợp chất là NO2.
Câu 7. Soda là hóa chất được dùng rộng rãi trong các ngành công nghiệp thủy tinh, đồ gốm, xà phòng, phẩm nhuộm. Xác định công thức hóa học của soda biết soda có cấu tạo từ Na hóa trị I và nhóm CO3 hóa trị II?
A. NaCO3.
B. Na(CO3)2.
C. Na2CO3.
D. Na2(CO3)3.
Đáp án: C
Giải thích:
Gọi công thức chung của soda là .
Áp dụng quy tắc hóa trị:
x.I = y.II → = =
Lấy x = 2 và y = 1.
Công thức hóa học của soda là Na2CO3.
Câu 8. Pháo hoa có thành phần nhiên liệu nổ gồm sulfur, than và potassium nitrate. Biết potassium nitrate có công thức hóa học là KNO3. Thành phần phần trăm khối lượng của các nguyên tố K, N và O trong potassium nitrate lần lượt là
A. 56,52%, 20,29%, 23,19%.
B. 38,61%, 13,86%, 15,84%.
C. 45,88%, 16,47%, 37,65%.
D. 38,61%, 13,86%, 47,53%.
Đáp án: D
Giải thích:
Khối lượng phân tử KNO3 là:
1.39 + 1.14 + 3.16 = 101 (amu)
Phần trăm khối lượng của các nguyên tố trong KNO3 là:
%K = = 38,61%
%N = = 13,86%
%O = 100% - %K - %N = 100% - 38,61% - 13,86% = 47,53%
Câu 9. Bột thạch cao có nhiều ứng dụng quan trọng trong đời sống. Thành phần chính của bột thạch cao là hợp chất A. Phân tử A có cấu tạo từ nguyên tố calcium (Ca), sulfur (S) và oxygen (O) với tỉ lệ phần trăm tương ứng là 29,41%, 23,53% và 47,06%. Biết khối lượng phân tử của A là 136 amu, công thức hóa học của A là
A. CaSO4.
B. CaSO2.
C. Ca2SO4.
D. CaSO3.
Đáp án: A
Giải thích:
Gọi công thức hóa học của hợp chất A là CaxSyOz.
Phần trăm khối lượng của các nguyên tố trong hợp chất là:
%Ca = ×100% = ×100% = 29,41%
® x = 1
%S = ×100% = ×100% = 23,53%
® y = 1
%O = ×100% = ×100% = 47,06%
® z = 4
Vậy công thức hóa học của hợp chất A là CaSO4.
Câu 10. Thạch nhũ trong hang động có thành phần chính là hợp chất T. Phân tử T có cấu tạo từ nguyên tố calcium, carbon và oxygen với tỉ lệ phần trăm tương ứng là 40%, 12% và 48%. Khối lượng phân tử của T là 100 amu. Nhận định nào sau đây là sai?
A. Trong phân tử T tỉ lệ số nguyên tử Ca : C : O là 1 : 1 : 3.
B. Trong một phân tử T có 2 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O.
C. Công thức hóa học của T là CaCO3.
D. Trong hai phân tử T có 2 nguyên tử Ca, 2 nguyên tử C và 6 nguyên tử O.
Đáp án: B
Giải thích:
Gọi công thức hóa học của hợp chất T là CaxCyOz.
Phần trăm khối lượng của các nguyên tố trong hợp chất là:
%Ca = ×100% = ×100% = 40%
® x = 1
%S = ×100% = ×100% = 12%
® y = 1
%O = ×100% = ×100% = 48%
® z = 3
Vậy công thức hóa học của hợp chất T là CaCO3 ® C đúng
Trong một phân tử T có 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O ® B sai.
Trong hai phân tử T có 2 nguyên tử Ca, 2 nguyên tử C và 6 nguyên tử O ® D đúng.
Trong phân tử T tỉ lệ số nguyên tử Ca: C: O là 1 : 1 : 3 ® A đúng.
Câu 11. Phát biểu nào sau đây không đúng?
A. Trong các hợp chất, hydrogen thường có hóa trị I và oxygen thường có hóa trị II;
B. Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố đó với các nguyên tử khác trong phân tử;
C. Trong phân tử hợp chất hai nguyên tố, tích hóa trị và số nguyên tử của nguyên tố này bằng tích hóa trị và số nguyên tử của nguyên tố kia;
D. Lưu huỳnh chỉ có hóa trị IV.
Đáp án đúng là: D
Lưu huỳnh có hóa trị là II, IV, VI.
Câu 12. Khi xác định hóa trị, hóa trị của nguyên tố nào được lấy làm đơn vị?
A. Hydrogen;
B. Sulfur;
C. Nitrogen;
D. Carbon.
Đáp án đúng là: A
Khi xác định hóa trị, hóa trị của nguyên tố hydrogen được lấy làm đơn vị. Hydrogen có hóa trị là I.
Câu 13. Copper có hóa trị II. Chọn công thức đúng?
A. CuSO4;
B. Cu2O;
C. Cu2Cl3;
D. CuOH.
Đáp án đúng là: A
Copper có hóa trị II trong công thức CuSO4.
Câu 14. Trong công thức hóa học SO2, S có hóa trị mấy?
A. I;
B. II;
C. III;
D. IV.
Đáp án đúng là: D
Đặt hóa trị của S là x.
Do O có hóa trị II nên theo quy tắc hóa trị: 1.x = 2.II
⇒ x = IV.
Câu 15. Xác định công thức hóa học của sulfur trioxit có cấu tạo từ S hoá trị VI và O.
A. SO2;
B. SO3;
C. SO;
D. S2O.
Đáp án đúng là: B
Công thức hóa học chung: SxOy
Theo quy tắc hóa trị: x.VI = II.y ⇒
Chọn x = 1, y = 3.
Công thức hóa học của sulfur trioxit là SO3.
Câu 16. Fe có hóa trị III trong công thức nào?
A. FeO;
B. Fe2O3;
C. FeSO4;
D. FeCl2.
Đáp án đúng là: B
Trong công thức Fe2O3 thì Fe có hóa trị III. Fe có hóa trị II trong các công thức FeO, FeSO4, FeCl2.
Câu 17. Cho hợp chất của X là X2O3 và Y là H2Y. Công thức hóa học của X và Y là
A. XY;
B. X2Y3;
C. X3Y;
D. XY2.
Đáp án đúng là: B
- Trong hợp chất X2O3 có O hóa trị II, đặt hóa trị của X là a, ta có:
Quy tắc hóa trị: 2.a = 3.II ⇒ a = III
Vậy X có hóa trị III.
- Trong hợp chất H2Y có H hóa trị I. Đặt hóa trị của Y là b ta có:
Quy tắc hóa trị: 2.I = 1.b ⇒ b = 2
Vậy Y có hóa trị II.
- Công thức hóa học chung:
Theo quy tắc hóa trị ta có: x.III = y.II
⇒
Lấy x = 2; y = 3
Vậy ông thức hóa học của X và Y là X2Y3.
Câu 18. Hóa trị của sulfur trong hợp chất nào sau đây là lớn nhất?
A. H2S;
B. SO2;
C. SO3;
D. FeS.
Đáp án đúng là: C
Hóa trị của sulfur trong hợp chất H2S, SO2, SO3, FeS lần lượt là II, IV, VI, II.
Câu 19. Thành phần phần trăm khối lượng của oxi trong hợp chất Fe2O3 là?
A. 30%;
B. 40%;
C. 50%;
D. 60%.
Đáp án đúng là: A
Câu 20. Tìm công thức hóa học của hợp chất CuxOy, biết A có 80% nguyên tử Cu và khối lượng phân tử là 80 amu.
A. Cu2O;
B. CuO;
C. Cu2O2;
D. CuO2.
Đáp án đúng là: B
%O = 100% - 80% = 20%
⇒ x = 1
⇒ y = 1
Công thức hóa học của hợp chất là CuO.
Các câu hỏi trắc nghiệm Khoa học tự nhiên lớp 7 sách Chân trời sáng tạo có đáp án, chọn lọc khác:
Trắc nghiệm Bài 1: Phương pháp và kĩ năng học tập môn Khoa học tự nhiên
Trắc nghiệm Bài 3: Nguyên tố hóa học
Trắc nghiệm Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Xem thêm các chương trình khác:
