Có 6 dung dịch đựng trong 6 lọ mất nhãn: Mg(NO3)2, Zn(NO3)2, Pb(NO3)2, AlCl3, KOH và NaCl
Với giải bài 5.11 trang 9 sbt Hóa học lớp 11 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 11. Mời các bạn đón xem:
Giải SBT Hoá 11 Bài 5: Luyện tập axit, bazơ và muối. Phản ứng trao đổi ion trong dung dịch các chất điện li
Bài 5.11 trang 9 Sách bài tập Hóa học 11: Có 6 dung dịch đựng trong 6 lọ mất nhãn: Mg(NO3)2, Zn(NO3)2, Pb(NO3)2, AlCl3, KOH và NaCl. Chỉ dùng thêm dung dịch AgNO3 và một thuốc thử nữa, hãy trình bày cách nhận biết từng dung dịch. Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng nhận biết đó.
Lời giải:
Dùng dung dịch phenolphtalein nhận ra dung dịch KOH.
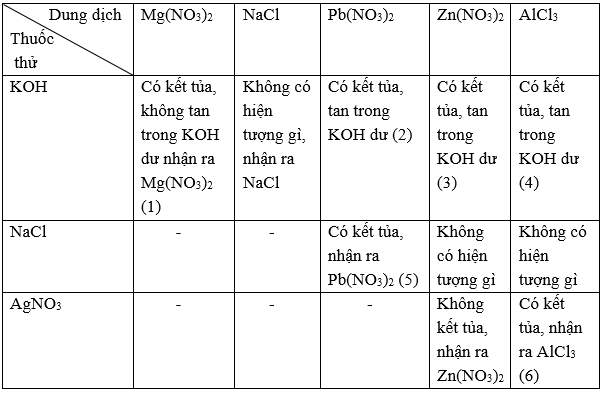
Các phương trình hoá học:
(1) Mg(NO3)2 + 2KOH → Mg(OH)2↓ + 2KNO3
Mg2+ + 2OH− → Mg(OH)2↓
(2) Pb(NO3)2 + 2KOH → Pb(OH)2↓ + 2KNO3
Pb2+ + 2OH− → Pb(OH)2↓
Pb(OH)2 + 2KOH → K2PbO2 + 2H2O
Pb(OH)2 + 2OH− → PbO22− + 2H2O
(3) Zn(NO3)2 + 2KOH → Zn(OH)2↓ + 2KNO3
Zn2+ + 2OH− → Zn(OH)2↓
Zn(OH)2 + 2KOH → K2ZnO2 + 2H2O
Zn(OH)2 + 2OH− → ZnO22− + 2H2O
(4) AlCl3 + 3KOH → Al(OH)3↓ + 3KCl
Al3+ + 3OH− → Al(OH)3↓
Al(OH)3 + KOH → KAlO2 + 2H2O
Al(OH)3 + OH− → AlO2− + 2H2O
(5) 2NaCl + Pb(NO3)2 → 2NaNO3 + PbCl2↓
Pb2+ + 2Cl− → PbCl2↓
(6) 3AgNO3 + AlCl3 → Al(NO3)3 + 3AgCl↓
Ag+ + Cl− → AgCl↓
Xem thêm lời giải sách bài tập Hóa học lớp 11 hay, chi tiết khác:
Bài 5.1 trang 8 sbt Hóa 11: Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là:...
Bài 5.3 trang 8 sbt Hóa 11: Dung dịch axit mạnh H2SO4 0,10M có:...
Bài 5.6 trang 8 sbt Hóa 11: Viết phương trình dạng phân tử ứng với phương trình ion rút gọn sau:...
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Vật Lí 11 | Giải bài tập Vật lí 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 11 (sách mới) | Sách bài tập Vật Lí 11
- Lý thuyết Vật Lí 11 (sách mới) | Kiến thức trọng tâm Vật Lí 11
- Các dạng bài tập Vật Lí lớp 11
- Giáo án Vật lí lớp 11 mới nhất
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
