Vở thực hành KHTN 8 Bài 4 (Kết nối tri thức): Dung dịch và nồng độ
Với giải vở thực hành Khoa học tự nhiên 8 Bài 4: Dung dịch và nồng độ sách Kết nối tri thức hay nhất, ngắn gọn sẽ giúp học sinh dễ dàng làm bài tập trong VTH KHTN 8 Bài 4.
Giải VTH KHTN 8 Bài 4: Dung dịch và nồng độ
1. Trong các cốc (1), (2), (3), cốc nào chứa dung dịch?
…………………………………………………………………………………………….
Dựa vào dấu hiệu nào để nhận biết?
…………………………………………………………………………………………….
Chỉ ra các chất tan, dung môi trong dung dịch thu được.
…………………………………………………………………………………………….
2. Phần dung dịch ở cốc (4) có phải là dung dịch bão hoà ở nhiệt độ phòng không? Giải thích.
…………………………………………………………………………………………….
Lời giải:
1.
- Cốc (1) và cốc (2) chứa dung dịch.
- Dấu hiệu nhận biết: Do hai cốc này là hỗn hợp đồng nhất của chất tan và dung môi.
- Chỉ ra các chất tan, dung môi trong dung dịch thu được:
Cốc (1): chất tan là muối ăn; dung môi là nước;
Cốc (2): chất tan là copper(II) sulfate; dung môi là nước.
2. Phần dung dịch ở cốc (4) là dung dịch bão hoà ở nhiệt độ phòng. Do ở điều kiện này dung dịch không thể hoà tan thêm chất tan được nữa.
Cho dần dần sodium carbonate (Na2CO3) vào cốc chứa một lượng nước xác định (giả sử 200 mL). Khuấy đều cho đến khi Na2CO3 không thể hoà tan thêm được nữa. Tách bỏ chất rắn không tan, ta thu được dung dịch bão hoà.
Lời giải:
Áp dụng công thức:
Trong đó: mnước= 20 gam; mct= 12 – 5 = 7 gam.
Vậy (g/100 g nước).
Lời giải:
Độ tan của Na2CO3 trong nước ở 18 oC là:
(g/ 100 g nước).
Bài 4.5 trang 14 Vở thực hành KHTN 8: Tính khối lượng H2SO4 có trong 20 gam dung dịch H2SO4 98%.
Lời giải:
Khối lượng H2SO4 có trong 20 gam dung dịch H2SO4 98% là:
a) Tính số mol urea trong dung dịch A, B và C.
b) Tính nồng độ mol của dung dịch C. Nhận xét về giá trị nồng độ mol của dung dịch C so với nồng độ mol của dung dịch A và B.
Lời giải:
a) Số mol urea trong dung dịch A là: n(A)= 0,02 . 2 = 0,04 (mol).
Số mol urea trong dung dịch B là: n(B)= 0,1 . 3 = 0,3 (mol).
Số mol urea trong dung dịch C là: n(C)= 0,04 + 0,3 = 0,34 (mol).
b) Nồng độ mol của dung dịch C là:
Ta có: Nồng độ mol của dung dịch A < Nồng độ mol của dung dịch C < Nồng độ mol của dung dịch B.
1. Tại sao phải dùng muối ăn khan để pha dung dịch?
2. Dung dịch muối ăn nồng độ 0,9% có thể được dùng để làm gì?
Lời giải:
1. Dùng muối ăn khan pha dung dịch để xác định được chính xác khối lượng chất tan.
2. Dung dịch muối ăn nồng độ 0,9% có thể được dùng để: Làm thuốc nhỏ mắt, thuốc nhỏ mũi, thuốc nhỏ tai, súc miệng và rửa vết thương,…; Dùng làm dịch truyền vào cơ thể để điều trị tình trạng mất nước do một số bệnh lí gây ra…
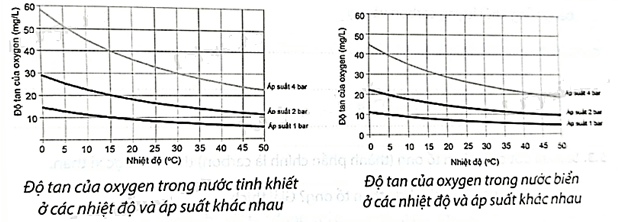
Từ các đồ thị trên hãy đưa ra nhận xét:
a) Khi nhiệt độ tăng, độ tan của oxygen trong nước tinh khiết thay đổi như thế nào?
…………………………………………………………………………………………….
b) Khi áp suất tăng, độ tan của oxygen trong nước tinh khiết thay đổi như thế nào?
…………………………………………………………………………………………….
c) So sánh độ tan của oxygen trong nước tinh khiết và trong nước biển ở:
5oC, 1 atm: ……………………………………………………………
30oC, 4 atm: ……………………………………………………………
Lời giải:
a) Khi nhiệt độ tăng, độ tan của oxygen trong nước tinh khiết giảm dần.
b) Khi áp suất tăng, độ tan của oxygen trong nước tinh khiết giảm dần.
c) So sánh độ tan của oxygen trong nước tinh khiết và trong nước biển ở:
5oC, 1 atm: Độ tan của oxygen trong nước tinh khiết lớn hơn trong nước biển.
30oC, 4 atm: Độ tan của oxygen trong nước tinh khiết lớn hơn trong nước biển.
Xem thêm lời giải Vở thực hành Khoa học tự nhiên 8 sách Kết nối tri thức hay, chi tiết khác:
Bài 5: Định luật bảo toàn khối lượng và phương trình hóa học
Bài 6: Tính theo phương trình hóa học
Xem thêm các chương trình khác:
- Soạn văn 8 Kết nối tri thức (hay nhất)
- Văn mẫu lớp 8 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 8 – Kết nối tri thức
- Bố cục tác phẩm Ngữ văn lớp 8 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn lớp 8 - Kết nối tri thức
- Giải SBT Ngữ văn 8 – Kết nối tri thức
- Giải Vở thực hành Ngữ văn 8 Kết nối tri thức | VTH Ngữ văn 8 Tập 1, Tập 2
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Kết nối tri thức
- Soạn văn 8 Kết nối tri thức (ngắn nhất)
- Giải sgk Toán 8 – Kết nối tri thức
- Lý thuyết Toán 8 – Kết nối tri thức
- Giải sbt Toán 8 – Kết nối tri thức
- Vở thực hành Toán 8 Kết nối tri thức | Giải VTH Toán 8 Tập 1, Tập 2
- Chuyên đề dạy thêm Toán 8 cả 3 sách (2024 có đáp án)
- Bài tập Tiếng Anh 8 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 8 – Global success
- Giải sbt Tiếng Anh 8 - Global Success
- Trọn bộ Từ vựng Tiếng Anh 8 Global success đầy đủ nhất
- Ngữ pháp Tiếng Anh 8 Global success
- Giải sgk Lịch sử 8 – Kết nối tri thức
- Lý thuyết Lịch sử 8 - Kết nối tri thức
- Giải sbt Lịch sử 8 – Kết nối tri thức
- Giải sgk Địa lí 8 – Kết nối tri thức
- Lý thuyết Địa lí 8 - Kết nối tri thức
- Giải sbt Địa lí 8 – Kết nối tri thức
- Giải VTH Địa lí 8 Kết nối tri thức | Vở thực hành Địa lí 8
- Giải sgk Giáo dục công dân 8 – Kết nối tri thức
- Lý thuyết Giáo dục công dân 8 – Kết nối tri thức
- Giải sbt Giáo dục công dân 8 – Kết nối tri thức
- Giải sgk Công nghệ 8 – Kết nối tri thức
- Lý thuyết Công nghệ 8 - Kết nối tri thức
- Giải sbt Công nghệ 8 – Kết nối tri thức
- Giải sgk Tin học 8 – Kết nối tri thức
- Lý thuyết Tin học 8 - Kết nối tri thức
- Giải sbt Tin học 8 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 8 – Kết nối tri thức