Vật lí 11 Bài 14: Dòng điện trong chất điện phân
Với giải bài tập Vật lí lớp 11 Bài 14: Dòng điện trong chất điện phân chi tiết được Giáo viên nhiều năm kinh nghiệm biên soạn bám sát nội dung sách giáo khoa Vật lí 11 giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập môn Vật lí 11 Bài 14. Mời các bạn đón xem:
Mục lục Giải Vật lí 11 Bài 14: Dòng điện trong chất điện phân
Câu hỏi C1 trang 81 Vật lí 11: Để nhận biết môi trường dẫn điện có phải là chất điện phân hay không, ta có thể làm cách nào?
Lời giải:
Để nhận biết môi trường dẫn điện có phải là chất điện phân hay không thì ta cho dòng điện qua môi trường dẫn điện, nếu là chất điện phân thì tại các điện cực có vật chất bám lại hoặc có một số chất thoát ra.
Câu hỏi C2 trang 83 Vật lí 11: Vì sao các định luật Fa-ra-đây có thể áp dụng cả với các chất được giải phóng ở điện cực nhờ phản ứng phụ?
Lời giải:
Các định luật Fa-ra-đây có thể áp dụng cả với các chất được giải phóng ở điện cực nhờ phản ứng phụ vì dòng điện trong chất điện phân tải điện lượng và vật chất bao gồm các chất được giải phóng ở điện cực là do phản ứng phụ sinh ra. Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
m = k.q
k: đương lượng điện hóa của chất được giải phóng ở điện cực.
Câu hỏi C3 trang 83 Vật lí 11:Có thể tính số nguyên tử trong một mol kim loại từ số Fa–ra–đây được không?
Lời giải:
Theo định luật Fa-ra-đây thứ II:
Trong đó:
n là hóa trị của nguyên tố.
A là khối lượng mol của chất được giải phóng ra ở điện cực.
k là đương lượng điện hóa của chất được giải phóng ở điện cực:
Theo định luật Fa-ra-đây thứ nhất ta được:
q = N.e (N là số electron tự do chạy qua bình điện phân)
e = 1,6.10-19C là số điện tích của nguyên tố
Ta suy ra:
Nếu xét 1 mol kim loại có hóa trị là 1 thì ; n = 1 thì số nguyên tử trong 1mol kim loại là:
hạt/mol
Câu hỏi C4 trang 84 Vật lí 11: Tại sao khi mạ điện, muốn lớp mạ đều. Ta phải quay vật cần mạ trong điện phân?
Lời giải:
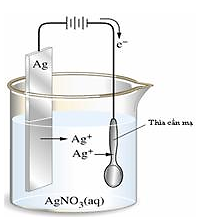
Khi mạ điện, vật cần mạ là catôt, anôt là tấm kim loại để mạ. Nếu ta không quay vật cần mạ trong lúc điện phân thì lượng kim loại bám vào vật cần mạ phía đối diện anôt sẽ nhiều hơn ở các phía khác vì vậy lớp mạ sẽ không đồng đều. Muốn lớp mạ điện đều ta phải quay vật cần mạ trong lúc điện phân.
Bài 1 trang 85 Vật lí 11: Nội dung của thuyết điện li là gì? Anion thường là phần nào của phân tử?
Lời giải:
- Thuyết điện li: Trong dung dịch, các hợp chất hóa học như axit, bazo và muối phân li (một phần hoặc toàn bộ) thành các nguyên tử và nhóm nguyên tử tích điện gọi là ion: ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
- Anion thường là phần ion âm của phần tử thường là gốc axit hoặc nhóm (OH)
- Cation mang điện dương là ion kim loại ion H+ hoặc một số nhóm nguyên tử khác.
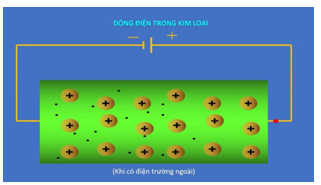
Bài 2 trang 85 Vật lí 11: Dòng điện trong chất điện phân khác dòng điện trong kim loại như thế nào?
Lời giải:
Sự khác nhau dòng điện trong chất điện phân và dòng điện trong kim loại:
|
Dòng điện trong chất điện phân |
Dòng điện trong kim loại |
|
Là dòng chuyển dời có hướng của các ion dương và ion âm |
Là dòng chuyển dời có hướng của các electron tự do |
|
Yếu hơn |
Mạnh hơn |
|
Tải điện lượng và vật chất |
Chỉ tải điện lượng |
Bài 3 trang 85 Vật lí 11: Hãy nói rõ hạt tải điện nào mang dòng điện trên các phần khác nhau của mạch điện có chứa bình điện phân:
a) Dây dẫn và điện cực kim loại.
b) Ở sát bề mặt của hai điện cực.
c) Ở trong lòng chất điện phân.
Lời giải:
Hạt tải điện mang dòng điện trên các phần tử của mạch điện có chứa bình điện phân:
a) Trong phần dây dẫn và các điện cực kim loại: hạt tải điện là các electron tự do.
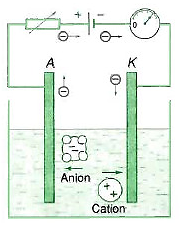
b) Ở sát bề mặt hai điện cực.
+ Sát cực dương: các ion âm (anion)
+ Sát cực âm: các ion dương (cation)
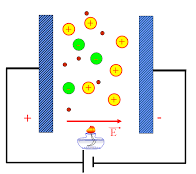
c) Ở trong lòng chất điện phân: dòng chuyển dời có hướng của các ion dương cùng chiều điện trường và ion âm ngược chiều điện trường.
Bài 4 trang 85 Vật lí 11: Chất điện phân thường dẫn điện tốt hơn hay kém hơn kim loại? Tại sao?
Lời giải:
- Chất điện phân thường dẫn điện yếu hơn kim loại.
- Nguyên nhân:
+ Mật độ các ion trong điện phân nhỏ hơn mật độ các electron tự do trong kim loại.
+ Khối lượng và kích thước của các ion trong chất điện phân lớn hơn khối lượng các electron, nên tốc độ chuyển động có hướng của chúng nhỏ hơn electron.
+ Môi trường dung dịch điện phân mất trật tự hơn, nên cản trở mạnh chuyển động có hướng của các ion.
Bài 5 trang 85 Vật lí 11: Hai bể điện phân: bể A để luyện nhôm, bể B để mạ niken. Hỏi bể nào có cực dương tan? Bể nào có suất phản điện?
Lời giải:
- Bể A để luyện nhôm có cực dương bằng than (graphit) nên không có hiện tượng cực dương tan. Mặt khác, bể nào không có cực dương tan thì sẽ đóng vai trò là máy thu và khi đó có suất phản điện ⇒ bể A để luyện nhôm có suất phản điện.
- Bể B để mạ niken có cực dương là niken và chất điện phân NiSO4 thì sẽ có cực dương tan. Khi mới mạ, bề mặt catot và anot còn khác nhau cũng có suất phản điện. Khi lớp niken trên vật cần mạ đã tương đối dày, bản chất hóa học của bề mặt anot và catot giống nhau thì B không còn suất phản điện.
Bài 6 trang 85 Vật lí 11: Phát biểu định luật Fa-ra- đây, công thức Fa-ra-đây và đơn vị dùng trong công thức này.
Lời giải:
- Định luật Fa-ra-đây thứ I
Khối lượng của vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
Công thức: m = kq
Trong đó:
+ k: đương lượng điện hóa của chất được giải phóng ở điện cực (đơn vị kg/C)
- Định luật Fa-ra-đây thứ hai:
Đương lượng điện hóa k của một nguyên tố tỉ lệ với đương lượng gam của nguyên tố đó. Hệ số tỉ lệ là trong đó F là số Fa-ra-đây (F = 96500C/mol):
Công thức:
Trong đó:
+ I là cường độ dòng điện không đổi khi đi qua bình điện (đơn vị A)
+ t là thời gian dòng điện chạy qua bình (đơn vị s)
Bài 7 trang 85 Vật lí 11: Khi điện phân dung dịch H2 SO4 với điện cực bằng graphit, ta thu được khí oxi bay ra ở anot. Có thể dùng công thức Fa-ra-đây để tính khối lượng oxi bay ra được không?
Lời giải:
Khi điện phân dung dịch H2SO4 với điện cực bằng graphit, ta thu được khí oxi bay ra. Trong trường hợp đó có thể dùng công thức Fa-ra-đây để tính khối lượng oxi bay ra.
Công thức:
Bài 8 trang 85 Vật lí 11: Phát biểu nào chính xác?
Dòng điện trong chất điện phân là chuyển động có hướng của:
A. các chất tan trong dung dịch
B. các icon dương trong dung dịch
C. các icon dương và các icon âm dưới tác dụng của điện trường trong dung dịch.
D. các icon dương và icon âm theo chiều điện trường trong dung dịch.
Lời giải:
Dòng điện trong chất điện phân là chuyển động có hướng của các ion dương và các ion âm dưới tác dụng của điện trường trong dung dịch.
Chọn đáp án C
Bài 9 trang 85 Vật lí 11: Phát biểu nào chính xác?
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là:
A. không có thay đổi gì ở bình điện phân.
D. đồng chạy từ anot sang catot.
Lời giải:
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là đồng chạy từ anot sang catot.
CuSO4 → Cu2+ + SO42-
Cu2+ –ve catot, +2e→ Cu
SO42- –ve anot, +2e→ CuSO4 + 2e–
Chọn đáp án D
Bài 10 trang 85 Vật lí 11: Tốc độ chuyển động của ion Na+ và Cl– trong nước có thể tính theo công thức: v = μE trong đó E là cường độ điện trường, μ là độ linh động có giá trị lần lượt là 4,5.10-8 m2/ (V.s). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phần tử NaCl đều phân li thành icon.
Lời giải:
n1 là mật độ hạt tải điện ion Na+; n2 là mật độ hạt tải điện là ion Cl–.
σ là độ dẫn điện; là điện trở suất.
Vì Na+ nhẹ hơn Cl– nên có độ linh động μ+ > μ–;
μ+ = 6,8.10-8 m2/ V.s; μ– = 4,5.10–8 m2/ V.s
Khi phân li, số ion Na+ bằng số ion Cl–. Do đó, theo đề:
n0 là nồng độ của dung dịch NaCl:
n0 = 0,1 mol/l =
=> n1 = n2 = n = n0.NA = 100.6,02.1023
= 6,02.1025 hạt/m3
Tốc độ chuyển động có hướng của các ion trong nước có thể tính theo công thức:
v = μ.E
Mà ta có: ; U = E.I; ; V = S.l nên ta được:
Độ dẫn điện của dung dịch NaCl là:
=> Điện trở suất của dung dịch NaCl:
Đáp án: 0,92 Ωm
Bài 11 trang 85 Vật lí 11: Người ta muốn bóc một lớp đồng dày d = 10 μm trên một bản đồng diện tích S = 1cm2 bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là ρ = 8900 kg/m3.
Lời giải:
Đổi đơn vị: d = 10 μm = 10.10-6 m;
S = 1 cm2 = 10-4 m2.
Khối lượng đồng cần bọc khỏi bản đồng là:
m = V.ρ = S.d.ρ = 10-4.10.10-6.8900.10-3
= 8,9.10-3 g
Mặt khác, theo định luật Fa-ra-đây khối lượng đồng cần bóc khỏi bản đồng trong thời gian t là:
Thời gian cần thiết để bóc được lớp đồng là:
Đáp án: t = 44,73 phút
Video giải Vật lí 11 Bài 14: Dòng điện trong chất điện phân
Xem thêm lời giải bài tập Vật lí lớp 11 hay, chi tiết khác:
Bài 15: Dòng điện trong chất khí
Bài 16: Dòng điện trong chân không
Bài 17: Dòng điện trong chất bán dẫn
Bài 18: Thực hành: khảo sát đặc tính chỉnh lưu của Điôt bán dẫn và đặc tính khuếch đại của tranzito
Xem thêm tài liệu Vật lí lớp 11 hay, chi tiết khác:
Xem thêm các chương trình khác:
- Giải sgk Hóa học 11 | Giải bài tập Hóa học 11 Học kì 1, Học kì 2 (Sách mới)
- Lý thuyết Hóa học 11(sách mới) | Kiến thức trọng tâm Hóa 11
- Giải sbt Hóa học 11 (sách mới) | Sách bài tập Hóa học 11
- Các dạng bài tập Hóa học lớp 11
- Giáo án Hóa học lớp 11 mới nhất
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
