Lý thuyết Dòng điện trong chất điện phân (mới 2023 + Bài Tập) - Vật lí 11
Tóm tắt lý thuyết Vật Lý 11 Bài 14: Dòng điện trong chất điện phân ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Vật Lý 11 Bài 14.
Lý thuyết Vật Lý 11 Bài 14: Dòng điện trong chất điện phân
Bài giảng Vật Lý 11 Bài 14: Dòng điện trong chất điện phân
I. Thuyết điện li
Trong dung dịch, các hợp chất hóa học như axit, bazơ và muối bị phân li (một phần hoặc toàn bộ) thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
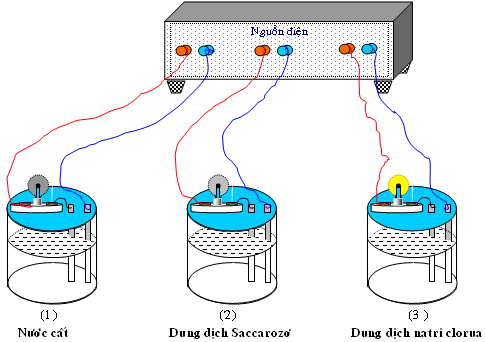
Các ion dương và âm vốn đã tồn tại sẵn trong các phân tử axit, bazo và muối. Chúng liên kết với nhau bằng lực Culong. Khi tan vào dung môi khác thì lực Culong yếu đi và một số phân tử bị chuyển động nhiệt tách thành các ion tự do.
Như vậy: những dung dịch và chất nóng chảy này được gọi là chất điện phân.
II. Bản chất dòng điện trong chất điện phân
- Dòng điện trong lòng chất điện phân là dòng ion dương và ion âm chuyển động có hướng theo hai chiều ngược nhau.
+ Ion dương chạy về phía catot nên gọi là cation.
+ Ion âm chạy về phía anot nên gọi là anion.
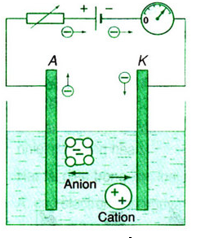
Chiều của các hạt tải điện trong chất điện phân
- Chất điện phân không dẫn điện tốt bằng kim loại. Do mật độ ion trong chất điện phân thường nhỏ hơn mật độ electron tự do trong kim loại, đồng thời khối lượng và kích thước của ion lớn hơn electron tự do nên tốc độ của chuyển động có hướng của chúng nhỏ hơn, môi trường dung dịch mất trật tự nên cản trở chuyển động mạnh.
- Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất đi theo. Tới điện cực chỉ có các electron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân.
III. Các hiện tượng diễn ra ở điện cực. Hiện tượng dương cực tan
Ta xét bình điện phân dung dịch CuSO4 có điện cực bằng đồng.
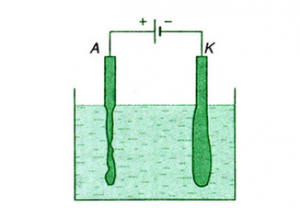
- Khi dòng điện chạy qua, cation Cu2+ chạy về catôt, về nhận electron từ nguồn điện đi tới. Ta có ở các điện cực:
+ Ở catôt: Cu2+ + 2e- → Cu
+ Ở anôt: Cu → Cu2+ + 2e-
- Khi anion (SO4)2- chạy về anôt, nó kéo ion Cu2+ vào dung dịch. Như vậy, đồng ở anôt sẽ tan dần vào trong dung dịch.
Kết luận: Hiện tượng dương cực tan xảy ra khi các anion đi tới anot kéo các ion kim loại của điện cực vào trong dung dịch.
IV. Các định luật Fa-ra-đây
1. Định luật Fa-ra-đây thứ nhất
Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện trường chạy qua bình đó: m = k.q
Trong đó k gọi là đương lượng điện hóa của chất được giải phóng ở điện cực.
2. Định luật Fa-ra-đây thứ hai
Đương lượng điện hóa k của một nguyên tố tỉ lệ với đương lượng gam của nguyên tố đó. Hệ số tỉ lệ là trong đó F gọi là số Fa-ra-đây.
Kết hợp hai định luật Fa-ra-đây, ta được công thức Fa-ra-đây:
Trong đó:
+ F = 96500 C/mol
+ A là khối lượng mol (g/mol)
+ n là hóa trị
+ m là khối lượng chất được giải phóng ở điện cực (g)
+ I là cường độ dòng điện (A)
+ t là thời gian dòng điện chạy qua (s)
V. Ứng dụng của hiện tượng điện phân
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống như luyện nhôm, tinh luyện đồng, điều chế clo, xút, mạ điện, đúc điện…
1. Luyện nhôm
Công nghệ luyện nhôm chủ yếu dựa vào hiện tượng điện phân quặng nhôm nóng chảy.
+ Quặng nhôm phổ biến là bôxit giàu nhôm ôxit Al2O3. Nhiệt độ nóng chảy của Al2O3 rất cao nên người ta pha thêm vào quặng Na3AlF6 để hạ nhiệt nóng chảy xuống còn 950oC. Bể điện phân có cực dương là quặng nhôm nóng chảy, cực âm bằng than, chất điện phân là muối nhôm nóng chảy, dòng điện chạy qua khoảng 104A.

Công nghiệp luyện nhôm
2. Mạ điện
Bể điện phân lúc này gọi là bể mạ có anot là một tấm kim loại để mạ, catot là vật cần mạ.
Chất điện phân thường là dung dịch muối kim loại để mạ (nếu mạ niken ta dùng NiSO4 tan trong nước,…) thêm một số chất phụ gia để lớp mạ bám chắc, bền đẹp hơn. Dòng điện qua bể mạ được chọn một cách thích hợp để đảm bảo chất lượng của lớp mạ.


Mạ điện
Trắc nghiệm Vật lí 11 Bài 14: Dòng điện trong chất điện phân
Câu 1. Hạt tải điện trong chất điện phân là
A. ion dương và ion âm.
B. electron tự do.
C. ion âm và electron.
D. ion dương và electron tự do.
Đáp án: A
Giải thích:
Dòng điện trong chất điện phân là dòng ion dương và dòng ion âm chuyển động có hướng theo hai chiều ngược nhau dưới tác dụng của điện trường.
Hạt tải điện trong chất điện phân là ion dương và ion âm.
Câu 2. Bản chất dòng điện trong chất điện phân là
A. dòng ion dương và dòng electron dịch chuyển ngược chiều điện trường.
B. dòng electron chuyển động hỗn loạn.
C. dòng ion dương và dòng ion âm chuyển động có hướng theo hai chiều ngược nhau.
D. dòng ion dương và dòng ion âm chuyển động cùng chiều nhau.
Đáp án: C
Giải thích: Dòng điện trong chất điện phân là dòng ion dương và dòng ion âm chuyển động có hướng theo hai chiều ngược nhau dưới tác dụng của điện trường.
Câu 3. Câu nào sau đây là không đúng khi nói về dòng điện trong chất điện phân.
A. Chất điện phân dẫn điện không tốt bằng kim loại.
B. Chất điện phân dẫn điện tốt hơn kim loại.
C. Mật độ hạt tải điện tự do trong chất điện phân nhỏ hơn trong kim loại, môi trường dung dịch rất mất trật tự.
D. Khối lượng và kích thước ion lớn hơn của electron.
Đáp án: B
Giải thích:
Dòng điện trong chất điện phân dẫn điện không tốt bằng kim loại do: mật độ electron tự do trong chất điện phân nhỏ hơn trong kim loại, môi trường dung dịch rất mất trật tự và khối lượng, kích thước ion lớn hơn của electron.
Câu 4. Trong các chất sau, chất nào là chất điện phân?
A. Nước nguyên chất.
B. Dung dịch NaOH.
C. Ca.
D. CO2.
Đáp án: B
Giải thích:
Trong dung dịch, các hợp chất hóa học như axit, bazơ và muối bị phân li (một phần hoặc toàn bộ) thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
Trong các chất trên thì chất điện phân là dung dịch NaOH (trong dung dịch NaOH phân li thành ion Na+ và ion OH-).
Câu 5. Trong các chất sau, chất nào không phải là chất điện phân?
A. Nước nguyên chất.
B. Dung dịch NaOH.
C. Dung dịch CuSO4.
D. Dung dịch NaCl.
Đáp án: A
Giải thích:
Trong dung dịch, các hợp chất hóa học như axit, bazơ và muối bị phân li (một phần hoặc toàn bộ) thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
Các chất điện phân là dung dịch NaOH, CuSO4, NaCl.
Nước nguyên chất không phải là chất điện phân.
Câu 6. Khối lượng chất giải phóng ở điện cực của bình điện phân được xác định bằng biểu thức nào sau đây?
A.
B.
C.
D.
Đáp án: C
Giải thích: Khối lượng chất giải phóng ở điện cực của bình điện phân được xác định bởi biểu thức:
Câu 7. Đơn vị của hằng số Fa - ra - đây là
A. C.mol.
B. C/mol.
C. N.
D. F.
Đáp án: B
Giải thích:
Hằng số Fa-ra-đây là F = 96494 C/mol (thường lấy là 96500 C/mol).
Đơn vị của hằng số Fa - ra - đây là: C/mol.
Câu 8. Đơn vị của đương lượng điện hóa là
A. kg/C.
B. C/mol.
C. N/m.
D. N.
Đáp án: B
Giải thích: Đơn vị của đương lượng điện hóa là: kg/C.
Câu 9. Câu nào sau đây là đúng khi nói về khối lượng chất được giải phóng ở điện cực của bình điện phân?
A. Khối lượng chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
B. Khối lượng chất giải phóng ở điện cực của bình điện phân tỉ lệ với khối lượng dung dịch trong bình.
C. Khối lượng chất giải phóng ở điện cực của bình điện phân tỉ lệ với thể tích của dung dịch trong bình.
D. Khối lượng chất giải phóng ở điện cực của bình điện phân tỉ lệ với khối lượng chất điện phân.
Đáp án: A
Giải thích: Định luật Fa – ra – đây thứ nhất: khối lượng chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó m = k.q.
Câu 10. Khối lượng chất giải phóng ở điện cực của bình điện phân tỉ lệ với
A. khối lượng dung dịch trong bình.
B. khối lượng chất điện phân.
C. điện lượng chuyển qua bình.
D. thể tích của dung dịch trong bình.
Đáp án: C
Giải thích: Định luật Fa – ra – đây thứ nhất: Khối lượng chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó m = k.q.
Xem thêm các chương trình khác:
- Giải sgk Hóa học 11 | Giải bài tập Hóa học 11 Học kì 1, Học kì 2 (Sách mới)
- Lý thuyết Hóa học 11(sách mới) | Kiến thức trọng tâm Hóa 11
- Giải sbt Hóa học 11 (sách mới) | Sách bài tập Hóa học 11
- Các dạng bài tập Hóa học lớp 11
- Giáo án Hóa học lớp 11 mới nhất
- Tóm tắt tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 11 (hay nhất) | Để học tốt Ngữ Văn 11 (sách mới)
- Soạn văn 11 (ngắn nhất) | Để học tốt Ngữ văn 11 (sách mới)
- Tác giả tác phẩm Ngữ văn 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Văn mẫu 11 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Toán 11 | Giải bài tập Toán 11 Học kì 1, Học kì 2 (sách mới)
- Các dạng bài tập Toán lớp 11
- Lý thuyết Toán lớp 11 (sách mới) | Kiến thức trọng tâm Toán 11
- Giáo án Toán lớp 11 mới nhất
- Bài tập Toán lớp 11 mới nhất
- Chuyên đề Toán lớp 11 mới nhất
- Giải sgk Tiếng Anh 11 (thí điểm)
- Giải sgk Tiếng Anh 11 | Giải bài tập Tiếng anh 11 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 11 (sách mới) | Sách bài tập Tiếng Anh 11
- Giải sbt Tiếng Anh 11 (thí điểm)
- Giải sgk Lịch sử 11 | Giải bài tập Lịch sử 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch Sử 11(sách mới) | Kiến thức trọng tâm Lịch Sử 11
- Giải Tập bản đồ Lịch sử 11
- Giải sgk Sinh học 11 | Giải bài tập Sinh học 11 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Sinh học 11 (sách mới) | Kiến thức trọng tâm Sinh 11
- Giải sgk Giáo dục công dân 11
- Lý thuyết Giáo dục công dân 11
- Lý thuyết Địa Lí 11 (sách mới) | Kiến thức trọng tâm Địa lí 11
- Giải Tập bản đồ Địa Lí 11
- Giải sgk Giáo dục quốc phòng - an ninh 11
