Sách bài tập Hóa 11 Bài 3 (Kết nối tri thức): Ôn tập chương 1
Với giải sách bài tập Hóa 11 Bài 3: Ôn tập chương 1 sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa 11 Bài 3.
Giải SBT Hóa 11 Bài 3: Ôn tập chương 1
Bài 3.1 trang 12 SBT Hóa 11: Cho phản ứng hoá học sau:
CH3COOH(l)+CH3OH(l)⇌CH3COOCH3(l)+H2O(l)
Biểu thức hằng số cân bằng của phản ứng trên là
A. KC=[CH3COOCH3][H2O][CH3COOH][CH3OH],
B. KC=[CH3COOCH3][CH3COOH][CH3OH].
C. KC=[CH3COOH][CH3OH][CH3COOCH3][H2O].
D. KC=[CH3COOH][CH3OH][CH3COOCH3].
Lời giải:
Đáp án đúng là: A
Hằng số cân bằng của phản ứng là KC=[CH3COOCH3][H2O][CH3COOH][CH3OH]
Bài 3.2 trang 12 SBT Hóa 11: Cho phản ứng hoá học sau: 3Fe(s)+4H2O(g)⇌Fe3O4(
Biểu thức hằng số cân bằng của phản ứng trên là
A.
B.
C. .
D. .
Lời giải:
Đáp án đúng là: B
Hằng số cân bằng của phản ứng là
Bài 3.3 trang 12 SBT Hóa 11: Cho phản ứng hoá học sau:
Nhận xét nào sau đây không đúng?
A. Nếu tăng nhiệt độ thì cân bằng trên chuyển dịch theo chiều nghịch.
B. Nếu tăng áp suất thì cân bằng trên chuyển dịch theo chiều nghịch.
C. Hằng số cân bằng của phản ứng trên chỉ phụ thuộc vào nhiệt độ.
D. Phản ứng thuận là phản ứng toả nhiệt.
Lời giải:
Đáp án đúng là: B
Tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm áp suất, tức là giảm số mol khí. Vậy cân bằng phải chuyển dịch theo chiều thuận.
Bài 3.4 trang 13 SBT Hóa 11: Cho cân bằng hoá học sau: .
Ở ToC, nồng độ các chất ở trạng thái cân bằng như sau:
và .
Hằng số cân bằng của phản ứng tại ToC là
A. 1,276.10-2.
B. 4,375.10-2.
C. 78,36.
D. 22,85.
Lời giải:
Đáp án đúng là: A
Hằng số cân bằng của phản ứng
A. FeCl3.
B. KCl.
C. Na2CO3.
D. Na2SO4.
Lời giải:
Đáp án đúng là: A
pH < 7 ứng với môi trường acid, muối FeCl3 là muối chứa cation kim loại trung bình.
A. H2SO4.
B. HCl.
C. NH3.
D. NaOH.
Lời giải:
Đáp án đúng là: D
pH càng cao, tính base càng mạnh. Vậy với cùng một nồng độ, dung dịch có pH cao nhất là NaOH.
Bài 3.7 trang 13 SBT Hóa 11: Cho phản ứng thuận nghịch sau:
Ở 430oC, nồng độ các chất ở trạng thái cân bằng là: [H2] = [I2] = 0,107 mol/L; [HI] = 0,786 mol/L.
a) Tính hằng số cân bằng (Kc) của phản ứng ở 430oC.
b) Nếu cho 2 mol H2 và 2 mol I2 vào bình kín dung tích 10 lít, giữ bình ở 430oC thì nồng độ các chất ở trạng thái cân bằng là bao nhiêu?
Lời giải:
a) Hằng số cân bằng của phản ứng là
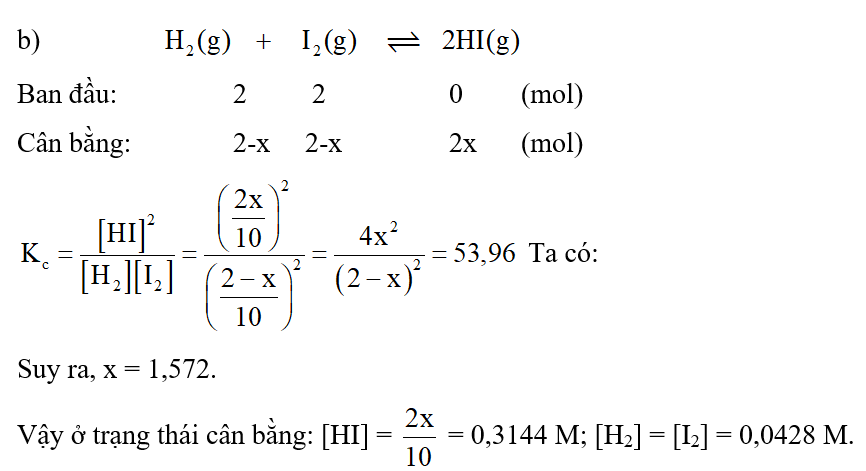
Lời giải:
Phương trình phản ứng:
Phản ứng thuận: H2O là acid, CH3-NH2 là base, phản ứng nghịch CH3-NH3+ là acid, OH- là base.
Dung dịch CH3NH2 có pH > 7, môi trường base.
Lời giải:
Phương trình điện li của các acid:
Nồng độ H+ trong dung dịch H2SO4 > HCl > CH3COOH.
pH (H2SO4) < pH (HCl) < pH (CH3COOH).
a) 5 mL dung dịch A và 10 mL dung dịch B.
b) 5 mL dung dịch B vào 10 mL dung dịch A.
c) 10 mL dung dịch B vào 10 mL dung dịch A.
Lời giải:
Phản ứng xảy ra khi trộn các dung dịch:
NaOH + HCl → NaCl + H2O
a) Sau khi phản ứng, số mol NaOH dư là: 5.10-3.0,1 = 5.10-4 (mol)
pH = 12,52.
b) Sau phản ứng, số mol HCl dư: 5.10-3.0,1 = 5.10-4 (mol)
pH = 1,48.
c) Sau phản ứng, dung dịch chỉ có NaCl, pH = 7.
Lời giải:
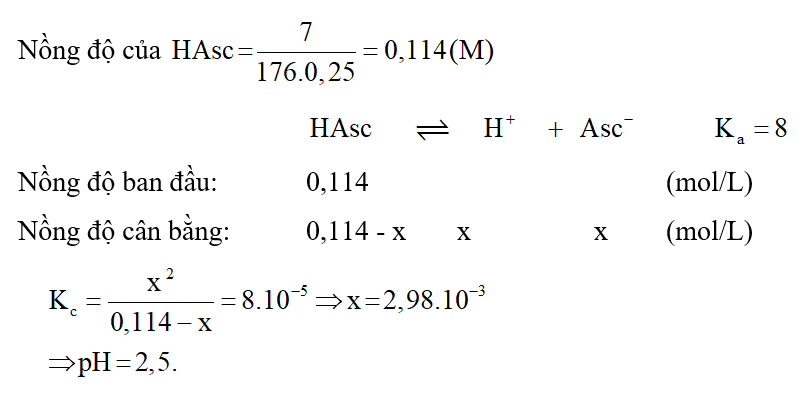
Lời giải:
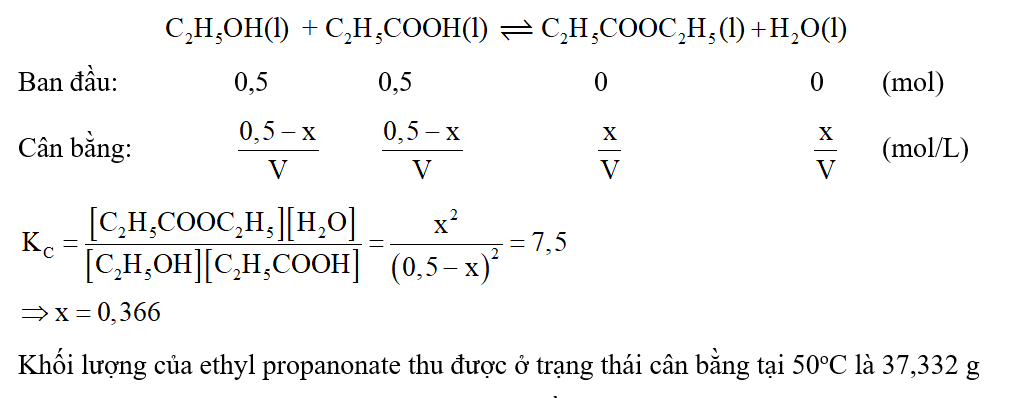
Bài 3.13 trang 14 SBT Hóa 11: Cho cân bằng hoá học sau:
a) Xác định số mol các chất ở trạng thái cân bằng.
b) Tính hằng số cân bằng của phản ứng ở nhiệt độ trên.
c) Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều nào?
Lời giải:
a)
Ban đầu: 1,0 3,0 (mol)
Phản ứng: 0,2 0,6 0,4 (mol)
Cân bằng: 0,8 2,4 0,4 (mol)
Nồng độ: 0,08 0,24 0,04 (mol)
b)
c) Nếu tăng nhiệt độ của bình phản ứng: cân bằng chuyển dịch theo chiều thu nhiệt tức là theo chiều nghịch, Kc giảm.
b) Trong dung dịch nước ion CH3COO- nhận proton của nước. Viết phương trình thuỷ phân và cho biết môi trường của dung dịch CH3COONa.
c) Cho 10 mL dung dịch NaOH 0,1 M vào 10 mL dung dịch CH3COOH 0,2 M thu được 20 mL dung dịch A. Tính pH của dung dịch A.
Lời giải:
a) Phương trình phân li xảy ra như sau:
b)
Phương trình thủy phân của ion CH3COO-:
CH3COO- + H2O ⇌ CH3COOH + OH-
Dung dịch CH3COONa có môi trường base.
c) Phản ứng :
Ban đầu: 2.10-3 1.10-3 (mol)
Phản ứng: 1.10-3 0 1.10-3 (mol)
Sau phản ứng: 1.10-3 1.10-3 (mol)
Nồng độ: 0,05 0,05 (mol/L)
Xét cân bằng hóa học sau:
Ban đầu: 0,05 0,05 0 (mol/L)
Cân bằng: 0,05 - x 0,05 + x x (mol/L)
.
Bài 3.15 trang 14 SBT Hóa 11: Một học sinh cân 1,062 g NaOH rắn rồi pha thành 250 mL dung dịch A.
a) Tính nồng độ CM của dung dịch A.
c) Nêu một số nguyên nhân dẫn đến việc sai khác nồng độ dung dịch A trong câu a và b.
Lời giải:
Số mol NaOH = 0,02655 mol.
a) CM của dung dịch A = 0,1062 M
b) Phản ứng chuẩn độ: HCl + NaOH → NaCl + H2O
Nồng độ dung dịch NaOH =
c) Một số nguyên nhân dẫn đến việc sai khác nồng độ dung dịch A: NaOH hút ẩm trong không khí, hấp thụ một lượng nhỏ khí CO2 trong không khí.
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Kết nối tri thức - hay nhất
- Văn mẫu lớp 11 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 11 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 11 - Kết nối tri thức
- Giải SBT Ngữ văn 11 – Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 11 – Kết nối tri thức
- Giải Chuyên đề học tập Ngữ văn 11 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Kết nối tri thức
- Soạn văn 11 Kết nối tri thức (ngắn nhất)
- Giải sgk Toán 11 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 11 – Kết nối tri thức
- Lý thuyết Toán 11 - Kết nối tri thức
- Giải sbt Toán 11 – Kết nối tri thức
- Bài tập Tiếng Anh 11 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 11 – Global success
- Giải sbt Tiếng Anh 11 - Global Success
- Trọn bộ Từ vựng Tiếng Anh 11 Global success đầy đủ nhất
- Ngữ pháp Tiếng Anh 11 Global success
- Giải sgk Vật lí 11 – Kết nối tri thức
- Lý thuyết Vật lí 11 – Kết nối tri thức
- Giải sbt Vật lí 11 – Kết nối tri thức
- Giải Chuyên đề học tập Vật lí 11 – Kết nối tri thức
- Chuyên đề dạy thêm Vật lí 11 cả 3 sách (2024 có đáp án)
- Giải sgk Sinh học 11 – Kết nối tri thức
- Lý thuyết Sinh học 11 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 11 – Kết nối tri thức
- Giải sbt Sinh học 11 – Kết nối tri thức
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Kết nối tri thức
- Lý thuyết Kinh tế pháp luật 11 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 11 – Kết nối tri thức
- Giải sgk Lịch sử 11 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 11 – Kết nối tri thức
- Lý thuyết Lịch sử 11 - Kết nối tri thức
- Giải sbt Lịch sử 11 – Kết nối tri thức
- Giải sgk Địa lí 11 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 11 – Kết nối tri thức
- Lý thuyết Địa lí 11 - Kết nối tri thức
- Giải sbt Địa lí 11 – Kết nối tri thức
- Giải sgk Công nghệ 11 – Kết nối tri thức
- Lý thuyết Công nghệ 11 - Kết nối tri thức
- Giải sbt Công nghệ 11 – Kết nối tri thức
- Giải sgk Tin học 11 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 11 – Kết nối tri thức
- Lý thuyết Tin học 11 - Kết nối tri thức
- Giải sbt Tin học 11 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng an ninh 11 – Kết nối tri thức
- Lý thuyết Giáo dục quốc phòng 11 – Kết nối tri thức
- Giải sbt Giáo dục quốc phòng 11 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 11 – Kết nối tri thức
