Phản ứng dưới đây có thể được thực hiện để điều chế khí chlorine trong phòng thí nghiệm
Lời giải bài 3 trang 114 Hóa học 10 sách Cánh diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải Hóa học 10 Cánh diều Bài 18: Hydrogen halide và hydrohalic acid
Bài 3 trang 114 Hóa học 10: a) Phản ứng dưới đây có thể được thực hiện để điều chế khí chlorine trong phòng thí nghiệm
4HCl + MnO2 Cl2 + MnCl2 + 2H2O
Cho biết khí chlorine thu được có thể lẫn với chất nào. Chỉ ra chất khử và chất oxi hóa trong phản ứng trên.
b) Hãy dự đoán, hydroiodic acid có phản ứng được với manganese(IV) oxide không. Giải thích.
Trả lời:
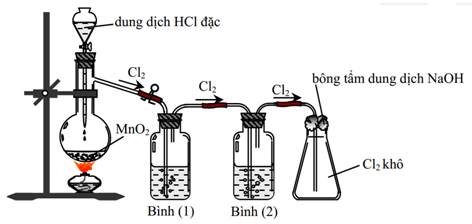
a) Khí chlorine có thể bị lẫn khí HCl và hơi nước. Dẫn khí tạo thành qua bình đựng dung dịch NaCl để giữ lại HCl. Dẫn khí qua bình đựng dung dịch H2SO4 đặc để giữ hơi nước. Khí chlorine thu được cuối cùng là tinh khiết.
Chất khử: HCl (số oxi hóa của Cl tăng từ -1 lên 0)
Chất oxi hóa: MnO2 (số oxi hóa của Mn giảm từ +4 xuống +2)
b) Hydroiodic acid (HI) có phản ứng được với mangan(IV) oxide (MnO2). Vì tính khử của I- lớn hơn Cl-
Chất khử: HI (số oxi hóa của I tăng từ -1 lên 0)
Chất oxi hóa: MnO2 (số oxi hóa của Mn giảm từ +4 xuống +2)
Xem thêm các bài giải sách giáo khoa Hóa học 10 bộ sách Cánh diều hay, chi tiết khác:
Câu hỏi 1 trang 109 Hóa học 10: Giải thích tại sao xu hướng phân cực của các phân tử HX giảm dần từ HF đến HI.
Câu hỏi 2 trang 109 Hóa học 10: Dựa vào bảng 18.1, hãy cho biết khí hydrogen halide nào sẽ hóa lỏng trước tiên khi nhiệt độ được hạ xuống thấp dần.
Câu hỏi 3 trang 111 Hóa học 10: Phản ứng của sodium chloride rắn, hay của sodium iodide rắn với sulfuric acid đặc là phản ứng oxi hóa – khử? Vì sao?
Luyện tập 1 trang 111 Hóa học 10: Có thể điều chế được hydrogen bromide từ phản ứng giữa potassium bromide với sulfuric acid đặc, đun nóng không? Vì sao?
Vận dụng trang 112 Hóa học 10: Vật dụng bằng kim loại đồng dễ bị phủ bởi lớp copper(II) oxide.
Thực hành trang 113 Hóa học 10: Nhận biết các dung dịch Có bốn bình nhỏ được đậy bằng nút có ống nhỏ giọt...
Bài 1 trang 114 Hóa học 10: Hãy giải thích vì sao nhiệt độ sôi của hydrogen bromide cao hơn nhiệt độ sôi của hydrogen chloride.
Bài 2 trang 114 Hóa học 10: Quan sát hình bên, nếu bơm từ từ cho đến hết lượng nước trong xi-lanh vào bong bóng chứa khí hydrogen chloride thì hiện tượng gì sẽ xảy ra. Giải thích.
Bài 3 trang 114 Hóa học 10: a) Phản ứng dưới đây có thể được thực hiện để điều chế khí chlorine trong phòng thí nghiệm
Bài 4 trang 114 Hóa học 10: Dung dịch hydrobromic acid không màu, để lâu trong không khí thì chuyển sang màu vàng nâu do phản ứng với oxygen trong không khí.
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 2: Thành phần của nguyên tử
Bài 4: Mô hình nguyên tử và orbital nguyên tử
Bài 5: Lớp, phân lớp và cấu hình electron
Xem thêm tài liệu Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Cánh Diều
- Tác giả tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Bố cục tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Soạn văn lớp 10 (ngắn nhất) – Cánh Diều
- Giải sbt Ngữ văn lớp 10 – Cánh Diều
- Văn mẫu lớp 10 – Cánh Diều
- Giải Chuyên đề học tập Ngữ văn 10 – Cánh diều
- Giải sgk Toán 10 – Cánh Diều
- Giải Chuyên đề Toán 10 – Cánh Diều
- Lý thuyết Toán 10 – Cánh Diều
- Giải sbt Toán 10 – Cánh Diều
- Chuyên đề dạy thêm Toán 10 Cánh diều (2024 có đáp án)
- Giải sgk Tiếng Anh 10 – Explore new worlds
- Giải sgk Tiếng Anh 10 – ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 10 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 i-learn Smart World
- Giải sbt Tiếng Anh 10 - iLearn Smart World
- Giải sgk Vật lí 10 – Cánh Diều
- Giải sbt Vật lí 10 – Cánh Diều
- Lý thuyết Vật lí 10 – Cánh Diều
- Giải Chuyên đề Vật lí 10 – Cánh Diều
- Giải sgk Sinh học 10 – Cánh Diều
- Giải sbt Sinh học 10 – Cánh Diều
- Lý thuyết Sinh học 10 – Cánh Diều
- Giải Chuyên đề Sinh học 10 – Cánh diều
- Giải sgk Lịch sử 10 – Cánh Diều
- Giải sbt Lịch sử 10 – Cánh Diều
- Giải Chuyên đề Lịch sử 10 – Cánh Diều
- Lý thuyết Lịch sử 10 – Cánh diều
- Giải sgk Địa lí 10 – Cánh Diều
- Lý thuyết Địa Lí 10 – Cánh Diều
- Giải sbt Địa lí 10 – Cánh Diều
- Giải Chuyên đề Địa lí 10 – Cánh Diều
- Lý thuyết Công nghệ 10 – Cánh Diều
- Giải sgk Công nghệ 10 – Cánh Diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải Chuyên đề Kinh tế pháp luật 10 – Cánh diều
- Lý thuyết KTPL 10 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 10 – Cánh Diều
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Cánh diều
- Giải sbt Giáo dục quốc phòng - an ninh 10 – Cánh Diều
- Giải sgk Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sbt Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sgk Tin học 10 – Cánh Diều
- Giải sbt Tin học 10 – Cánh Diều
- Giải Chuyên đề Tin học 10 – Cánh diều
- Lý thuyết Tin học 10 - Cánh diều
- Giải sgk Giáo dục thể chất 10 – Cánh Diều
