Giải Hóa 10 Bài 16 - Cánh diều: Tốc độ phản ứng hóa học
Với giải bài tập Hóa 10 Bài 16: Tốc độ phản ứng hóa học sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 10 Bài 16.
Giải bài tập Hóa lớp 10 Bài 16: Tốc độ phản ứng hóa học
Video giải bài tập Hóa lớp 10 Bài 16: Tốc độ phản ứng hóa học
Trả lời:
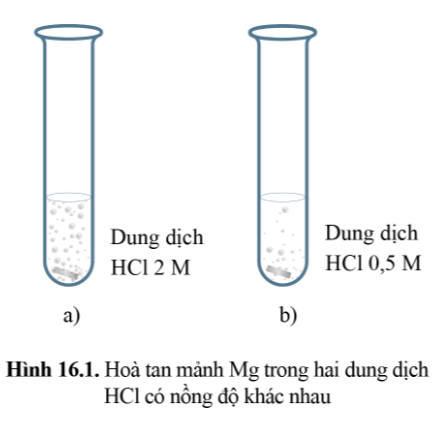
Mảnh Mg ở thí nghiệm (a) sẽ tan hết trước, do ở thí nghiệm (a) nồng độ HCl là 2M lớn hơn nồng độ HCl ở thí nghiệm (b).
I. Khái niệm tốc độ phản ứng, tốc độ trung bình của phản ứng
1. Khái niệm tốc độ phản ứng
Trả lời:
Trong cùng một khoảng thời gian lượng HCl và Mg bị mất đi ở thí nghiệm (a) là nhanh hơn so với thí nghiệm (b).
⇒ Lượng MgCl2 tạo thành ở thí nghiệm (a) cũng tăng lên nhanh hơn.
Coi thể tích của dung dịch là không đổi trong suốt quá trình của phản ứng
⇒ Nồng độ của MgCl2 ở thí nghiệm (a) tăng lên nhanh hơn.
Trả lời:
Tốc độ của phản ứng (1) ở (thí nghiệm (a)) là nhanh hơn so với tốc độ của phản ứng ở (thí nghiệm (b)).
2. Tốc độ trung bình của phản ứng
Trả lời:
Tốc độ trung bình của phản ứng:
ΔC = C2 – C1 ; Δt = t2 – t1
Trong đó C1, C2 là nồng độ của một chất tại thời điểm tương ứng t1 và t2.
Các chất tham gia có nồng độ giảm theo thời gian ⇒ C2 < C1 ⇒ ΔC < 0
Vậy để tốc độ phản ứng nhận giá trị dương cần phải thêm dấu trừ trong biểu thức (3) khi tính tốc độ trung bình của phản ứng theo các chất tham gia phản ứng.
Trả lời:
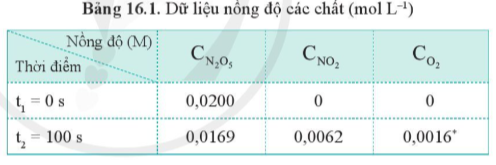
Nồng độ ban đầu của O2 (C1) là 0, nồng độ sau 100s (C2) là 0,0016M.
Δt = 100 s – 0 s = 100 s. Vậy tốc độ trung bình của phản ứng trong 100 s đầu tiên là:
= 1,6.10-5 (M.s-1).
Trả lời:
Từ bảng 6.1, không thể tính được tốc độ trung bình của phản ứng sau 50 giây vì chưa biết nồng độ của các chất (C2) tại t2 = 50 s
Trả lời:
Sắp xếp tốc độ các phản ứng sau theo chiều tăng dần:
(2) phản ứng gỉ sắt < (1) phản ứng than cháy trong không khí < (3) phản ứng nổ của khí bình gas.
II. Định luật tác dụng khối lượng
Trả lời:
Hiện tượng:
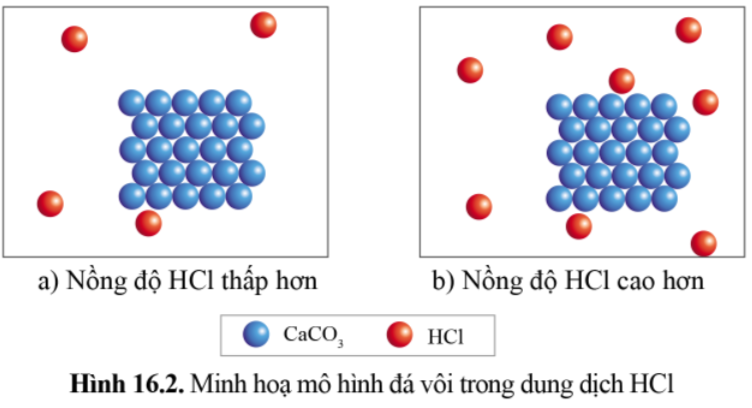
Mẩu đá vôi ở ống nghiệm (b) tan nhanh hơn mẩu đá vôi ở ống nghiệm (a); đồng thời khí thoát ra ở ống nghiệm (b) cũng nhanh hơn khí thoát ra ở ống nghiệm (a).
Phương trình hóa học của phản ứng:
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + H2O (l) + CO2 (g)
Nhận xét:
Nồng độ HCl càng lớn thì tốc độ của phản ứng càng lớn.
Trả lời:
Bơm N2 hoặc CO2 vào túi đựng thực phẩm trước khi đóng gói nhằm mục đích đẩy bớt oxygen ra ngoài (làm giảm nồng độ oxygen trong túi) ⇒ Giảm tốc độ phản ứng oxi hóa thực phẩm của oxygen cũng như sự hoạt động của vi khuẩn ⇒ Hạn chế sự ôi thiu thực phẩm.
Trả lời:
Biểu thức (5) v = k.
Nếu nồng độ của chất A và B đều bằng 1M thì ta có: v = k.1.1 hay v = k
Như vậy hằng số tốc độ phản ứng có giá trị đúng bằng tốc độ phản ứng.
Trả lời:
Phản ứng (6): H2 (g) + I2 (g) → 2HI (g)
Tốc độ của phản ứng (6): v = k.
Nếu nồng độ H2 tăng gấp đôi thì v’ = k. = 2.v
⇒ Nếu nồng độ H2 tăng gấp đôi thì tốc độ của phản ứng tăng gấp đôi.
III. Các yếu tố ảnh hưởng đến tốc độ phản ứng, hệ số nhiệt độ vant’t hoff (γ)
1. Ảnh hưởng của nồng độ
Trả lời:
Theo định luật tác dụng khối lượng, tốc độ của phản ứng H2(g) với I2(g) là:
v = k.
Khi nồng độ của H2(g) cũng như I2(g) đều tăng lên gấp đôi ta có:
v’ = k. = 4.v
Vậy tốc độ của phản ứng tăng lên 4 lần.
Vận dụng 3 trang 93 Hóa học 10: Hãy giải thích các hiện tượng dưới đây.
a) Khi ở nơi đông người trong không gian kín, ta cảm thấy khó thở và phải thở nhanh hơn.
b) Tàn đóm đỏ bùng lên khi cho vào bình oxygen nguyên chất.
c) Bệnh nhân suy hô hấp cần thở oxygen thay vì không khí (chứa 21% thể tích oxygen).
Trả lời:
a) Khi ở nơi đông người trong không gian kín, ta cảm thấy khó thở và phải thở nhanh hơn.
Vì: Oxygen duy trì sự hô hấp, khi ở nơi đông người trong không gian kín nồng độ oxygen giảm đi nhanh vì phải cung cấp cho nhiều người ⇒ Con người bị thiếu oxygen nên cảm thấy khó thở và phải thở nhanh hơn để lấy oxygen.
b) Oxygen duy trì sự cháy mà trong bình khí oxygen nguyên chất, nồng độ oxygen lớn hơn ngoài không khí.
⇒ Tốc độ phản ứng cháy xảy ra nhanh hơn, mãnh liệt hơn.
⇒ Tàn đóm đỏ bùng cháy.
c) Bệnh nhân suy hô hấp cần thở oxygen thay vì không khí do: bệnh nhân suy hô hấp khó khăn trong việc tự thở, dẫn đến thiếu oxygen cung cấp cho hoạt động của cơ thể. Trong bình khí nén oxygen, nồng độ oxygen cao hơn nồng độ oxygen có trong không khí giúp bệnh nhân thở dễ dàng hơn, cung cấp đủ oxygen cho các tế bào, giúp duy trì sự sống.
2. Ảnh hưởng của áp suất
3. Ảnh hưởng của diện tích bề mặt
Trả lời:
Hiện tượng: Mẩu đá vôi B (đã được tán nhỏ thành bột) tan trong dung dịch HCl nhanh hơn mẩu đá vôi A, đồng thời khí thoát ra ở ống nghiệm chứa mẩu B (đã được tán nhỏ thành bột) cũng nhanh hơn.
Phương trình hóa học của phản ứng:
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + H2O (l) + CO2 (g)
Nhận xét: Diện tích bề mặt càng lớn, tốc độ phản ứng càng lớn.
Trả lời:
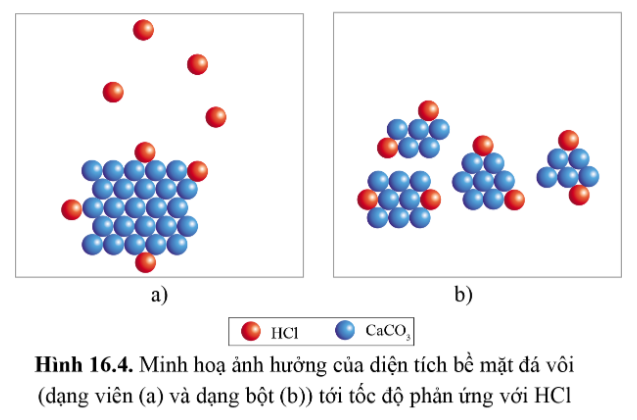
Khi diện tích bề mặt đá vôi tăng lên (đá vôi dạng bột) thì số lượng va chạm của CaCO3 với HCl trong cùng một đơn vị thời gian sẽ lớn hơn, số lượng va chạm hiệu quả cũng cao hơn, từ đó tốc độ phản ứng nhanh hơn.
Vận dụng 4 trang 94 Hóa học 10: Giải thích vì sao thanh củi chẻ nhỏ hơn thì sẽ cháy nhanh hơn.
Trả lời:
Thanh củi chẻ nhỏ hơn thì diện tích bề mặt tiếp xúc của củi với oxygen không khí sẽ lớn hơn làm cho củi sẽ cháy nhanh hơn.
4. Ảnh hưởng của nhiệt độ
Trả lời:
Hiện tượng: Ở ống nghiệm được đun nóng bằng đèn cồn đinh sắt tan nhanh hơn, đồng thời khí thoát ra nhanh hơn.
Phương trình hóa học của phản ứng:
Fe(s) + H2SO4 (aq) → FeSO4 (aq) + H2(g)
Nhận xét: Nhiệt độ càng cao, tốc độ phản ứng càng lớn.
Câu hỏi 8 trang 95 Hóa học 10: Vì sao đinh sắt trong thí nghiệm bên phải được tẩy sạch gỉ và dầu mỡ?
Trả lời:
Vì khi đinh sắt bị bao quanh bởi lớp gỉ và dầu mỡ (lẫn tạp chất) sẽ làm kết quả thí nghiệm không chính xác.
Trả lời:
Dựa vào tốc độ thoát khí nhanh hay chậm để so sánh tốc độ phản ứng trong hai thí nghiệm này.
Trả lời:
⇔ = 23 = 8
Vậy với phản ứng có γ = 2, nếu nhiệt độ tăng từ 20oC lên 50oC thì tốc độ phản ứng tăng 8 lần.
5. Ảnh hưởng của chất xúc tác
Trả lời:
- Rót khoảng 2 ml nước oxi già (dung dịch H2O2 3%) vào một ống nghiệm.
Hiện tượng: Xuất hiện lăn tăn bọt khí.
Nhận xét: Dung dịch H2O2 3% ở điều kiện bình thường phân hủy rất chậm tạo bọt khí O2 thoát ra. Theo phương trình:
2H2O2(aq) → O2(g) + 2H2O(l)
- Thêm một lượng nhỏ bột MnO2 (màu đen, dùng làm chất xúc tác) vào ống nghiệm.
Hiện tượng: Bọt khí thoát ra mãnh liệt, khi kết thúc thí nghiệm màu đen của MnO2 ban đầu vẫn giữ nguyên.
Nhận xét: Phản ứng xảy ra nhanh hơn do thêm xúc tác MnO2, sau phản ứng MnO2 không bị biến đổi.
2H2O2(aq) O2(g) + 2H2O(l)
Kết luận: Chất xúc tác MnO2 làm tăng tốc độ phân hủy H2O2.
Trả lời:
Enzyme amylase và lipase có trong nước bọt là chất xúc tác đẩy nhanh quá trình tiêu hóa tinh bột và chất béo.
Khi nhai kĩ thức ăn được chia nhỏ hơn nhằm tăng diện tích tiếp xúc giữa thức ăn với các enzyme, khiến các phản ứng trong quá trình tiêu hóa chất béo và tinh bột xảy ra nhanh hơn, hiệu quả hơn.
Bài tập (trang 98)
Trả lời:
Đáp án đúng là: C
Áp dụng mối liên hệ của hệ số Van’t Hoff với tốc độ và nhiệt độ ta có:
Trong đó giá trị γ = 2 – 4
Với γ = 2 ⇒ = 4
Vậy tốc độ quá trình thủy phân collagen thành gelatin sẽ tăng lên ít nhất 4 lần khi sử dụng nồi áp suất thay cho nồi thường.
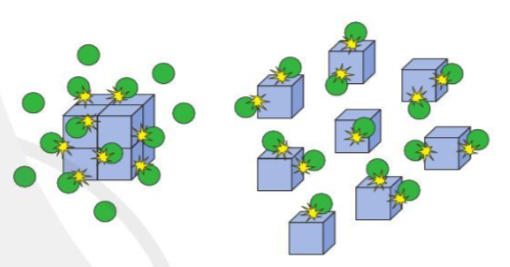
Trả lời:
Hình ảnh bên minh họa ảnh hưởng của diện tích tiếp xúc tới tốc độ phản ứng.
Giả sử khối lập phương là chất X, quả cầu màu xanh là chất Y.
Khi chất X được chia nhỏ, số va chạm của chất X và chất Y (trong cùng một đơn vị thời gian) sẽ lớn hơn, số va chạm hiệu quả cũng tăng lên, từ đó tốc độ phản ứng tăng.
Trả lời:
Phương trình hóa học của phản ứng:
Fe(s) + 2HCl(aq) → FeCl2(aq) + H2(g)
Để làm tăng tốc độ điều chế khí H2 ta có thể:
- Tăng nồng độ dung dịch HCl.
- Đun nóng ống nghiệm chứa hỗn hợp Fe và HCl
- Dùng sắt bột và khuấy nhẹ trong quá trình phản ứng.
Bài 4* trang 98 Hóa học 10: Cùng một lượng kim loại Zn phản ứng với cùng một thể tích dung dịch H2SO4 1M, nhưng ở hai nhiệt độ khác nhau.
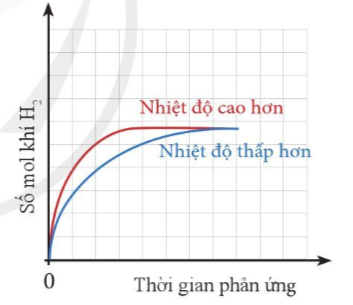
Thể tích khí H2 sinh ra ở mỗi thí nghiệm theo thời gian được biểu diễn ở đồ thị bên.
a) Giải thích vì sao đồ thị màu đỏ ban đầu cao hơn đồ thị màu xanh.
b) Vì sao sau một thời gian, hai đường đồ thị lại chụm lại với nhau?
Trả lời:
a) Đồ thị màu đỏ ban đầu cao hơn đồ thị màu xanh do: Nhiệt độ càng cao, tốc độ phản ứng càng lớn, khí thoát ra càng nhiều.
b) Sau một thời gian, hai đồ thị lại chụm lại với nhau do phản ứng đã dừng lại (một hoặc cả hai các chất tham gia phản ứng hết). Do cùng lượng kim loại và H2SO4 cùng thể tích, nồng độ nên lượng khí thu được là như nhau ở cả 2 trường hợp.
Bài 5* trang 98 Hóa học 10: Phản ứng A → sản phẩm được thực hiện trong bình kín. Nồng độ của A tại các thời điểm t = 0; t = 1 phút; t = 2 phút lần lượt là 0,1563 M; 0,1496 M; 0,1431 M.
a) Tính tốc độ trung bình của phản ứng trong phút thứ nhất và từ phút thứ nhất tới hết phút thứ hai.
b) Vì sao hai giá trị tốc độ tính được không bằng nhau.
Trả lời:
a) Tốc độ trung bình của phản ứng trong phút thứ nhất là
= = 1,12.10-4 (M.s-1)
Tốc độ trung bình của phản ứng từ phút thứ nhất tới hết phút thứ hai là
= = 1,08.10-4 (M.s-1)
b) Đa số các phản ứng hóa học có nồng độ giảm dần theo thời gian.
Nồng độ của chất phản ứng càng lớn thì tốc độ phản ứng càng lớn. Càng về sau nồng độ của chất A càng giảm nên tốc độ của phản ứng cũng giảm dần.
Lý thuyết Tốc độ phản ứng hóa học
I. Khái niệm tốc độ phản ứng, tốc độ trung bình của phản ứng
1. Khái niệm tốc độ phản ứng
- Thí nghiệm: Cho hai mảnh Zn có cùng khối lượng vào hai bình chứa cùng thể tích dung dịch H2SO4 loãng, dư, nồng độ dung dịch ở mỗi bình lần lượt là 0,5M và 1M.

Hình 16.1. Thí nghiệm Zn tác dụng với H2SO4 loãng
+ Phản ứng xảy ra trong thí nghiệm cho Zn vào dung dịch H2SO4 loãng, ở hai nồng độ khác nhau như sau:
Zn(s) + H2SO4(aq) ZnSO4(aq) + H2(g)
+ Hiện tượng: bọt khí H2 thoát ra ở thí nghiệm (b) nhanh hơn so với thí nghiệm (a) đã chứng tỏ lượng H2SO4 bị mất đi do phản ứng với Zn ở thí nghiệm (b) nhanh hơn ở thí nghiệm (a).
Tốc độ phản ứng giữa Zn với dung dịch H2SO4 ở các nồng độ khác nhau là khác nhau.
+ Trong hai thí nghiệm trên, coi thể tích của dung dịch là không đổi trong suốt quá trình phản ứng. Trong cùng một khoảng thời gian, độ giảm nồng độ H2SO4 trong thí nghiệm (b) là nhanh hơn so với trong thí nghiệm (a).
Có thể dựa theo sự thay đổi nồng độ của chất trong phản ứng trong một đơn vị thời gian để đánh giá mức độ nhanh, chậm của phản ứng.
Kết luận:
- Khái niệm: Tốc độ phản ứng của một phản ứng hóa học là đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
- Tốc độ phản ứng được kí hiệu là v, có đơn vị là (đơn vị nồng độ) (đơn vị thời gian)-1
Ví dụ: mol L-1 s-1 (hay M s-1), ...
2. Tốc độ trung bình của phản ứng
- Tốc độ trung bình của phản ứng (![]() ) là tốc độ tính trung bình trong một khoảng thời gian phản ứng.
) là tốc độ tính trung bình trong một khoảng thời gian phản ứng.
- Cho phản ứng tổng quát:
aA + bB mM + nN (1)
Tốc độ phản ứng (1) được tính dựa theo sự thay đổi nồng độ của một chất bất kì trong phản ứng theo quy ước sau:
![]() (2)
(2)
Trong đó: ΔC = C2 – C1, Δt = t2 – t1 lần lượt là biến thiên nồng độ và biến thiên thời gian tương ứng. C1, C2 là nồng độ của một chất tại thời điểm tương ứng t1 và t2 (với t2 > t1).
Ví dụ: Cho phản ứng phân hủy N2O5:
2N2O5(g) 4NO2(g) + O2(g) (3)
Nồng độ của mỗi chất trong phản ứng (3) tại thời điểm t1 = 0 và t2 = 50s được cho trong bảng sau:
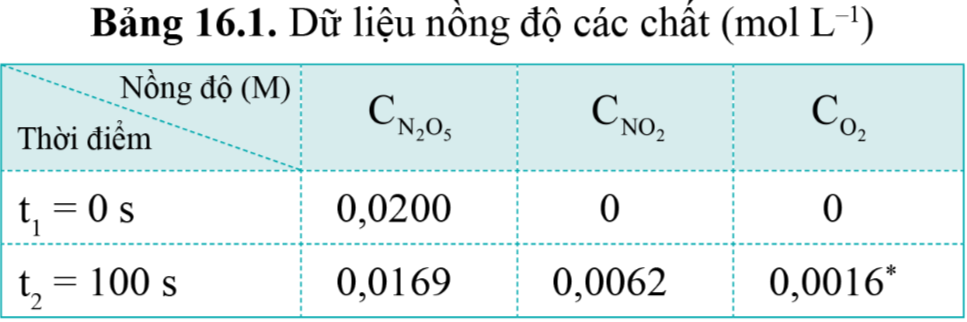
Bảng 16.1. Dữ liệu nồng độ các chất (mol L-1)
Tốc độ trung bình của phản ứng (3) có thể được tính theo biến thiên nồng độ chất phản ứng hoặc sản phẩm:
+ Tính theo nồng độ N2O5
Nồng độ của N2O5 ban đầu (C1) là 0,0200M, sau 50 s (C2) là 0,0045M
Vậy tốc độ trung bình của phản ứng trong 50s đầu tiên là:
![]() = 1,55,10-5 (M s-1)
= 1,55,10-5 (M s-1)
+ Tính theo O2
Nồng độ của O2 ban đầu (C1) là 0M, sau 50 s (C2) là 0,000775M
Vậy tốc độ trung bình của phản ứng trong 50s đầu tiên là:
= 1,55,10-5 (M s-1)
II. Định luật tác dụng khối lượng
- Thí nghiệm: Cho hai mảnh Zn có cùng khối lượng vào hai bình chứa cùng thể tích dung dịch H2SO4 loãng, dư, nồng độ dung dịch ở mỗi bình lần lượt là 0,5M và 1M.
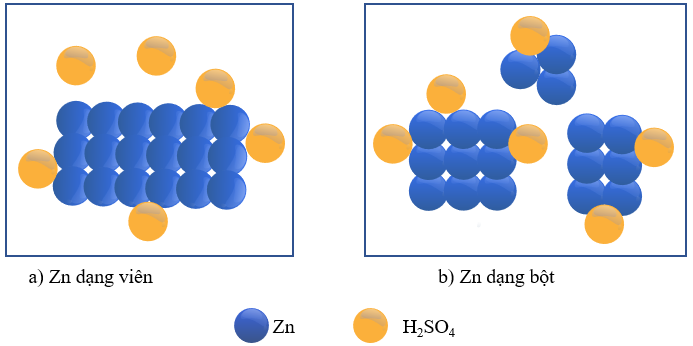
Hình 16.2. Minh họa mô hình Zn trong dung dịch H2SO4 loãng
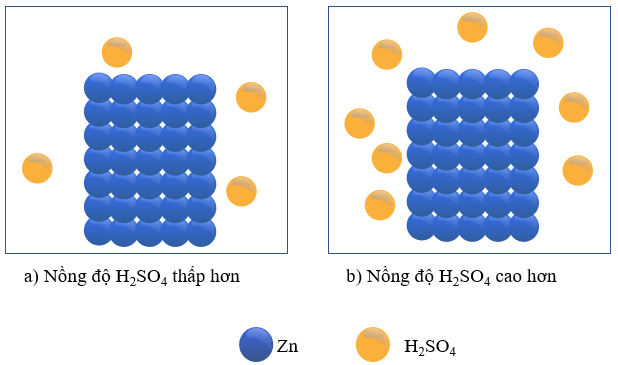
- Giải thích: Để phản ứng xảy ra, cần phải có sự va chạm giữa H2SO4 và Zn. Nồng độ của H2SO4 ở bình (b) lớn gấp đôi nồng độ H2SO4 ở bình (a), do vậy số va chạm của H2SO4 với Zn trong bình (b) sẽ nhiều hơn, dẫn đến tốc độ phản ứng ở bình (b) là lớn hơn.
- Kết luận: Khi nồng độ các chất tham gia phản ứng càng lớn thì tốc độ phản ứng càng lớn.
- Giải thích: Để phản ứng xảy ra, các phân tử phản ứng phải va chạm với nhau, nồng độ càng lớn thì số lượng va chạm càng nhiều (trong cùng một đơn vị thời gian, một đơn vị thể tích) nên tốc độ phản ứng càng lớn.
- Định luật tác dụng khối lượng áp dụng cho các phản ứng đơn giản, biểu thị sự phụ thuộc tốc độ phản ứng theo nồng độ các chất phản ứng.
Lưu ý: Phản ứng đơn giản là phản ứng chỉ diễn ra qua một giai đoạn duy nhất, chất phản ứng tạo thành sản phẩm không qua một chất trung gian nào khác.
- Cho phản ứng tổng quát: aA + bB sản phẩm
+ Tốc độ phản ứng được tính như sau: v = k(4)
+ Trong đó: CA, CB là nồng độ mol. L-1 tương ứng của chất A và B; k là hằng số tốc độ phản ứng mà giá trị của nó chỉ phụ thuộc vào nhiệt độ và bản chất các chất tham gia phản ứng.
- Định luật tác dụng khối lượng: Tốc độ phản ứng tỉ lệ thuận với tích nồng độ các chất tham gia phản ứng với số mũ thích hợp.
® Hằng số tốc độ phản ứng càng lớn thì tốc độ phản ứng càng lớn.
- Hằng số tốc độ phản ứng có giá trị đúng bằng tốc độ phản ứng khi nồng độ các chất phản ứng bằng nhau và bằng 1M. Đây chính là ý nghĩa của hằng số tốc độ phản ứng.
Ví dụ: Phản ứng của N2 và H2 là phản ứng đơn giản:
N2(g) + 3H2(g) 2NH3(g) (5)
+ Theo định luật tác dụng khối lượng, tốc độ của phản ứng (5) được viết dưới dạng:
v = k
+ Ở một nhiệt độ không đổi, tốc độ phản ứng (5) tỉ lệ với nồng độ N2 và H2.
Lưu ý: Tốc độ phản ứng tính theo định luật tác dụng khối lượng là tốc độ tức thời của phản ứng tại một thời điểm, khác với tốc độ trung bình của phản ứng trong một khoảng thời gian như đã nêu trên.
III. Các yếu tố ảnh hưởng tới tốc độ phản ứng, hệ số nhiệt độ Van’t Hoff
1. Ảnh hưởng của nồng độ
- Nồng độ các chất phản ứng càng lớn, tốc độ phản ứng càng lớn.
Ví dụ: Phản ứng của H2 và I2 như sau:
H2(g) + I2(g) 2HI(g) (6)
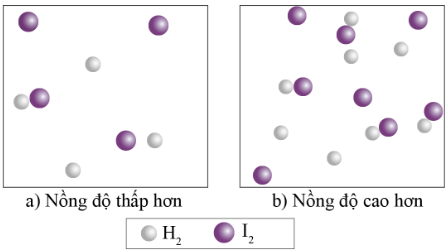
Hình 16.3. Ảnh hưởng của nồng độ các chất phản ứng tới tốc độ phản ứng
+ Giải thích: Khi nồng độ của H2 và I2 tăng lên trong một đơn vị thể tích, các phân tử này cũng sẽ nhiều hơn, dẫn đến số lượng va chạm giữa chúng (trong cùng một đơn vị thời gian) tăng lên. Vì vậy tốc độ phản ứng tăng lên khi nồng độ các chất tăng.
2. Ảnh hưởng của áp suất
- Áp suất của các chất phản ứng ở thể khí càng lớn, tốc độ phản ứng càng lớn.
- Giải thích: Đối với các chất khí, nồng độ của chất khí tỉ lệ với áp suất của nó. Do vậy, khi áp suất chất tham gia phản ứng ở thể khí tăng lên, sẽ làm nồng độ chất khí tăng lên, từ đó làm tốc độ phản ứng tăng.
Ví dụ: Phản ứng tổng hợp NH3 từ N2 và H2 được thực hiện ở áp suất rất cao từ 200 – 300 atm để tăng tốc độ phản ứng.
3. Ảnh hưởng của diện tích bề mặt
- Thí nghiệm: Dùng hai mẫu Zn có cùng khối lượng, trong đó một mẫu dạng hạt còn một mẫu dạng bột. Cho hai mẫu đó cùng tác dụng với hai thể tích bằng nhau dung dịch H2SO4 loãng, dư, cùng nồng độ.
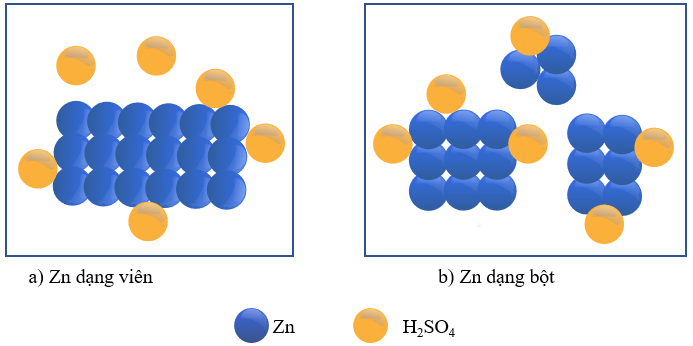
Hình 16.4. Ảnh hưởng của diện tích bề mặt tới tốc độ phản ứng
- Diện tích bề mặt càng lớn, tốc độ phản ứng càng lớn.
- Giải thích: Khi diện tích bề mặt tăng lên, dẫn đến số lượng va chạm giữa các chất phản ứng tăng lên (trong cùng một đơn vị thời gian) tăng lên. Vì vậy tốc độ phản ứng tăng lên khi nồng độ các chất tăng.
- Ảnh hưởng của diện tích bề mặt tới tốc độ phản ứng trong thực tế: thanh củi chẻ nhỏ hơn thì sẽ cháy nhanh hơn, than tổ ong có nhiều lỗ sẽ cháy nhanh hơn, ...
4. Ảnh hưởng của nhiệt độ
- Nhiệt độ càng cao, tốc độ phản ứng càng lớn. Với đa số các phản ứng, khi nhiệt độ tăng 10oC thì tốc độ phản ứng tăng từ 2 đến 4 lần. Giá trị g = 2 ÷ 4 này được gọi là hệ số nhiệt độ Van’t Hoff.
- Mối liên hệ của hệ số nhiệt độ Van’t Hoff tới tốc độ và nhiệt độ như sau:
Trong đó, v2 và v1 là tốc độ phản ứng ở nhiệt độ T2 và T1 tương ứng.
- Ảnh hưởng của nhiệt độ tới tốc độ phản ứng trong thực tế: Nước nhanh sôi hơn khi được đun ở nhiệt độ cao; thức ăn bị chậm ôi, thiu khi được để trong tủ lạnh, ...
5. Ảnh hưởng của chất xúc tác
- Chất xúc tác là chất làm tăng tốc độ phản ứng, nhưng không bị thay đổi cả về lượng và chất sau phản ứng.
Ví dụ 1: Khi đun nóng, KClO3 bị phân hủy tương đối chậm theo phương trình:
3KClO3(s) 3KCl(s) + 3O2(g)
Tuy nhiên tốc độ phản ứng phân hủy này sẽ nhanh hơn rất nhiều khi có mặt chất xúc tác MnO2. Kết thúc thí nghiệm trên, màu đen của MnO2 ban đầu vẫn giữ nguyên vì MnO2 không bị biến đổi sau phản ứng phân hủy KClO3.
- Ảnh hưởng của nhiệt độ tới tốc độ phản ứng trong thực tế:
+ Phản ứng tổng hợp NH3 từ N2 và H2 cần sử dụng chất xúc tác là sắt kim loại được trộn thêm Al2O3, K2O, ... để làm tăng tốc độ phản ứng, phản ứng không có chất xúc tác sẽ diễn ra rất chậm.
+ Các enzyme trong cơ thể là những chất xúc tác sinh học thúc đẩy các phản ứng sinh hóa phức tạp trong cơ thể chúng ta. Ví dụ enzyme amylase có trong nước ngọt giúp thủy phân tinh bột thành đường.
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 17: Nguyên tố và đơn chất halogen
Bài 18: Hydrogen halide và hydrohalic acid
Bài 2: Thành phần của nguyên tử
Xem thêm tài liệu Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Cánh Diều
- Tác giả tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Bố cục tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Soạn văn lớp 10 (ngắn nhất) – Cánh Diều
- Giải sbt Ngữ văn lớp 10 – Cánh Diều
- Văn mẫu lớp 10 – Cánh Diều
- Giải Chuyên đề học tập Ngữ văn 10 – Cánh diều
- Giải sgk Toán 10 – Cánh Diều
- Giải Chuyên đề Toán 10 – Cánh Diều
- Lý thuyết Toán 10 – Cánh Diều
- Giải sbt Toán 10 – Cánh Diều
- Chuyên đề dạy thêm Toán 10 Cánh diều (2024 có đáp án)
- Giải sgk Tiếng Anh 10 – Explore new worlds
- Giải sgk Tiếng Anh 10 – ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 10 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 i-learn Smart World
- Giải sbt Tiếng Anh 10 - iLearn Smart World
- Giải sgk Vật lí 10 – Cánh Diều
- Giải sbt Vật lí 10 – Cánh Diều
- Lý thuyết Vật lí 10 – Cánh Diều
- Giải Chuyên đề Vật lí 10 – Cánh Diều
- Giải sgk Sinh học 10 – Cánh Diều
- Giải sbt Sinh học 10 – Cánh Diều
- Lý thuyết Sinh học 10 – Cánh Diều
- Giải Chuyên đề Sinh học 10 – Cánh diều
- Giải sgk Lịch sử 10 – Cánh Diều
- Giải sbt Lịch sử 10 – Cánh Diều
- Giải Chuyên đề Lịch sử 10 – Cánh Diều
- Lý thuyết Lịch sử 10 – Cánh diều
- Giải sgk Địa lí 10 – Cánh Diều
- Lý thuyết Địa Lí 10 – Cánh Diều
- Giải sbt Địa lí 10 – Cánh Diều
- Giải Chuyên đề Địa lí 10 – Cánh Diều
- Lý thuyết Công nghệ 10 – Cánh Diều
- Giải sgk Công nghệ 10 – Cánh Diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải Chuyên đề Kinh tế pháp luật 10 – Cánh diều
- Lý thuyết KTPL 10 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 10 – Cánh Diều
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Cánh diều
- Giải sbt Giáo dục quốc phòng - an ninh 10 – Cánh Diều
- Giải sgk Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sbt Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sgk Tin học 10 – Cánh Diều
- Giải sbt Tin học 10 – Cánh Diều
- Giải Chuyên đề Tin học 10 – Cánh diều
- Lý thuyết Tin học 10 - Cánh diều
- Giải sgk Giáo dục thể chất 10 – Cánh Diều