TOP 15 câu Trắc nghiệm Hydrogen halide và hydrohalic acid (có đáp án) - Hoá 10 Cánh diều
Bộ 15 bài tập trắc nghiệm Hóa học lớp 10 Bài 18: Hydrogen halide và hydrohalic acid có đáp án đầy đủ các mức độ sách Cánh diều giúp học sinh ôn luyện trắc nghiệm Hóa học 10 Bài 18.
Chỉ 150k mua trọn bộ Trắc nghiệm Hóa lớp 10 Cánh diều bản word (cả năm) có đáp án chi tiết:
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận tài liệu.
Xem thử tài liệu tại đây: Link tài liệu
Trắc nghiệm Hóa học 10 Bài 18: Hydrogen halide và hydrohalic acid - Cánh diều
Câu 1. Hydrogen halide là
A. đơn chất halogen (X2)
B. hợp chất gồm nguyên tố halogen và nguyên tố hydrogen (HX)
C. hợp chất gồm nguyên tố chlorine và nguyên tố hydrogen (HCl)
D. hợp chất gồm nguyên tố halogen, nguyên tố hydrogen và nguyên tố oxygen (HXO)
Đáp án: B
Giải thích:
Hydrogen halide là hợp chất gồm nguyên tố halogen và nguyên tố hydrogen (HX).
Câu 2. Hydrogen halide là
A. đơn chất
B. hợp chất ion
C. hợp chất cộng hóa trị không cực
D. hợp chất cộng hóa trị phân cực
Đáp án: D
Giải thích:
Hydrogen halide là hợp chất cộng hóa trị phân cực do sự chênh lệch độ âm điện giữa nguyên tử H và nguyên tử halogen.
H?− : X?+
Câu 3. Xu hướng phân cực giảm từ HF đến HI là do
A. khối lượng phân tử tăng dần từ HF đến HI
B. bán kính nguyên tử halogen tăng dần từ F đến I
C. tính oxi hóa giảm dần từ F2 đến I2
D. độ âm điện giảm dần từ F đến I
Đáp án: D
Giải thích:
Xu hướng phân cực giảm từ HF đến HI là do độ âm điện giảm dần từ F đến I làm cho sự chênh lệch độ âm điện giữa H và halogen giảm dần ⇒ Độ phân cực H – X giảm dần từ HF đến HI.
Câu 4. Phân tử nào dưới đây có nhiệt độ sôi cao bất thường?
A. HCl
B. HF
C. HI
D. HBr
Đáp án: B
Giải thích:
Trong dãy hydrogen halide, nhiệt độ sôi tăng dần từ HCl đến HI. Riêng HF có nhiệt độ sôi cao bất thường do các phân tử HF tạo liên kết hydrogen với nhau.
![]()
Câu 5. Hydrohalic acid có tính acid mạnh nhất là
A. HCl
B. HF
C. HI
D. HBr
Đáp án: C
Giải thích:
Trong dãy hydrohalic acid, tính acid tăng dần từ HF đến HI.
Vậy HI có tính acid mạnh nhất.
Câu 6. Nguyên nhân chủ yếu làm tăng độ mạnh của các acid theo dãy từ HF đến HI là do
A. sự tăng khối lượng phân tử từ HF đến HI
B. sự giảm độ phân cực của liên kết từ HF đến HI
C. sự giảm độ bền liên kết từ HF đến HI
D. sự tăng kích thước từ HF đến HI
Đáp án: C
Giải thích:
Nguyên nhân chủ yếu làm tăng độ mạnh của các acid theo dãy từ HF đến HI là do sự giảm độ bền liên kết từ HF đến HI.
Câu 7. Khi phản ứng với sulfuric acid đặc thì:
(1) Ion Cl− thể hiện tính khử.
(2) Ion Br− thể hiện tính khử và sulfur trong H2SO4 từ số oxi hóa +6 về số oxi hóa +4 trong SO2.
(3) Ion I− thể hiện tính khử và sulfur trong H2SO4 từ số oxi hóa +6 về số oxi hóa −4 trong H2S.
Khẳng định đúng là
A. (1)
B. (1), (2) và (3)
C. (2) và (3)
D. (1) và (2)
Đáp án: C
Giải thích:
Khi phản ứng với sulfuric acid đặc thì:
(1) Ion Cl− thể hiện tính khử. ⇒ sai. Vì ion Cl− không thể hiện tính khử.
(2) Ion Br− thể hiện tính khử và sulfur trong H2SO4 từ số oxi hóa +6 về số oxi hóa +4 trong SO2. ⇒ đúng.
(3) Ion I− thể hiện tính khử và sulfur trong H2SO4 từ số oxi hóa +6 về số oxi hóa −4 trong H2S. ⇒ đúng.
Câu 8. Cho phản ứng: NaCl (s) + H2SO4 (l)
Sản phẩm thu được là
A. NaHSO3 và HCl
B. NaHSO4, Cl2, S và H2O
C. NaHSO4 và HCl
D. NaHSO4, Cl2, SO2 và H2O
Đáp án: C
Giải thích:
NaCl (s) + H2SO4 (l) NaHSO4 (s) + HCl (g)
Câu 9. Khi cho NaBr (s) tác dụng với H2SO4 đặc, đun nóng. Hiện tượng xảy ra là
A. tạo khí có mùi hắc
B. tạo khí có mùi trứng thối
C. tạo khí có mùi hắc, hơi bay ra có màu nâu đỏ
D. Không hiện tượng
Đáp án: C
Giải thích:
2NaBr (s) + 3H2SO4 (l) 2NaHSO4 (s) + Br2 (g) + SO2 (g) + 2H2O (g)
Phản ứng tạo ra khí SO2 có mùi hắc, hơi Br2 có màu nâu đỏ.
Câu 10. Trong các ion halide X−, ion có tính khử mạnh nhất là
A. F−
B. I−
C. Br−
D. Cl−
Đáp án: A
Giải thích:
Trong các ion halide X−, tính khử tăng từ Cl− đến I− (F− không thể hiện tính khử)
⇒ ion có tính khử mạnh nhất là I−
Câu 11. Ứng dụng nào dưới đây không phải là ứng dụng của hydrogen chloride?
A. Khắc chữ lên thủy tinh
B. Sản xuất vinyl chloride cung cấp cho ngành nhựa
C. Phục vụ sản xuất dược phẩm, thuốc nhuộm
D. Tẩy rửa gỉ sét bám trên bề mặt thép
Đáp án: A
Giải thích:
Khắc chữ lên thủy tinh là ứng dụng của hydrogen fluoride (HF) theo phản ứng:
SiO2 (s) + 4HF (aq) ⟶ SiF4 (g) + 2H2O (l)
Câu 12. Thuốc thử để nhận biết các ion halide X− là
A. nước
B. quỳ tím
C. dung dịch AgNO3
D. sung dịch Ba(OH)2
Đáp án: C
Giải thích:
Thuốc thử để nhận biết các ion halide X− là dung dịch silver nitrate AgNO3.
- Khi X- là F- thì không thấy hiện tượng xảy ra.
- Khi X- là Cl- thì xuất hiện kết tủa màu trắng silver chloride (AgCl)
- Khi X- là Br- thì xuất hiện kết tủa màu vàng nhạt sliver bromide (AgBr)
- Khi X- là I- thì xuất hiện kết tủa màu vàng silver iodide (AgI)
Câu 13. Nhỏ từ từ vài giọt dung dịch silver nitrate vào ống nghiệm chứa dung dịch hydrochloride acid, ta thấy
A. không có hiện tượng xảy ra
B. xuất hiện kết tủa trắng
C. xuất hiện kết tủa vàng nhạt
D. xuất hiện kết tủa vàng
Đáp án: B
Giải thích:
AgNO3 (aq) + HCl (aq) ⟶ AgCl (s) + NaNO3 (aq)
AgCl (s) là kết tủa có màu trắng.
Câu 14. Nếu bơm từ từ cho đến hết lượng nước trong xi lanh vào bong bóng chứa khí hydrogen chloride thì hiện tượng xảy ra là
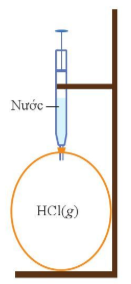
A. Bong bóng xẹp vào
B. Bong bóng phồng to hơn
C. Bong bóng đổi màu
D. Không có hiện tượng
Đáp án: A
Giải thích:
Vì khí hydrogen chloride tan nhiều trong nước tạo thành dung dịch hydrochloride acid.
⇒ Khi bơm nước vào, khí hydrogen chloride bị hòa tan hết.
⇒ Bong bóng xẹp vào.
Câu 15. Nhỏ vài giọt dung dịch silver nitrate vào ống nghiệm chứa dung dịch muối sodium halide thì thấy không có hiện tượng xảy ra. Công thức của muối đó là
A. NaCl
B. NaF
C. NaBr
D. NaI
Đáp án: B
Giải thích:
AgNO3 (aq) + NaF (aq) ⟶ Không xảy ra phản ứng.
Do đó, không có hiện tượng xảy ra.
Các câu hỏi trắc nghiệm Hóa học lớp 10 sách Cánh diều có đáp án, chọn lọc khác:
Trắc nghiệm Bài 2. Thành phần của nguyên tử
Trắc nghiệm Bài 3. Nguyên tố hóa học
Trắc nghiệm Bài 4: Mô hình nguyên tử và orbital nguyên tử
Trắc nghiệm Bài 5: Mô hình nguyên tử và orbital nguyên tử
Trắc nghiệm Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Xem thêm các chương trình khác:
- Trắc nghiệm Toán lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Hóa học lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Địa Lí lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Công nghệ lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Giáo Dục Quốc Phòng lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Vật Lí lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Lịch sử lớp 10 có đáp án - Kết nối tri thức
- Trắc nghiệm Sinh học lớp 10 có đáp án – Kết nối tri thức
- Trắc nghiệm Tin học lớp 10 có đáp án - Kết nối tri thức
- Trắc nghiệm Kinh tế pháp luật lớp 10 có đáp án - Kết nối tri thức
- Trắc nghiệm Tiếng Anh lớp 10 có đáp án - Global Success Kết nối tri thức
- Trắc nghiệm Toán lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm Địa Lí lớp 10 có đáp án – Chân trời sáng tạo
- Trắc nghiệm GDTC lớp 10 có đáp án – Chân trời sáng tạo
