Giải Hóa 11 Bài 8 (Cánh diều): Hợp chất hữu cơ và hoá học hữu cơ
Với giải bài tập Hóa 11 Bài 8: Hợp chất hữu cơ và hoá học hữu cơ sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 11 Bài 8.
Giải Hóa 11 Bài 8: Hợp chất hữu cơ và hoá học hữu cơ
Cho biết một số ứng dụng của chất hữu cơ trong đời sống.
Lời giải:
- Trong số các chất trên, chất hữu cơ là saccharose (C12H22O11); celullose ((C6H10O5)n); aspirin (hay acetylsalicylic acid, C9H8O4); propane (C3H8). Chất vô cơ là calcium sulfate (CaSO4); silicon dioxide (SiO2).
- Hợp chất hữu cơ có nhiều ứng dụng quan trọng trong cuộc sống như làm nhiên liệu; nguyên liệu sản xuất; dung môi …
I. Hợp chất hữu cơ và hoá học hữu cơ
II. Đặc điểm chung của các hợp chất hữu cơ
Lời giải:
Do các nguyên tố C, H, O, N, P có độ âm điện khác nhau không nhiều nên liên kết giữa nguyên tử của các nguyên tố này với nhau lại là liên kết cộng hoá trị.
CH3 – CH2 – CH2 – CH3 (1)
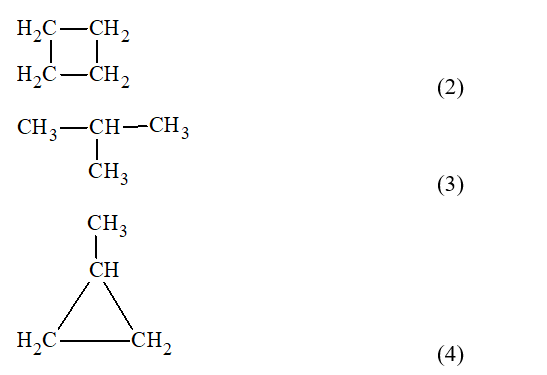
Hãy chỉ ra chất nào có mạch carbon hở không phân nhánh, chất nào có mạch carbon hở phân nhánh và chất nào có mạch vòng.
Lời giải:
- Chất có mạch carbon hở không phân nhánh là (1);
- Chất có mạch carbon hở phân nhánh là (3);
- Chất có mạch vòng là (2) và (4).
Lời giải:
Ta có:
|
Chất |
C2H6 |
H2O |
LiF |
|
Nhiệt độ sôi |
-88,5 oC |
100 oC |
1 676 oC |
Giải thích:
+ LiF là hợp chất ion; C2H6 và H2O là hợp chất cộng hoá trị do đó LiF có nhiệt độ sôi lớn nhất.
+ Trong hai hợp chất C2H6 và H2O thì chỉ có H2O tạo được liên kết hydrogen, do đó nhiệt độ sôi của H2O cao hơn của C2H6.
Lời giải:
Người ta thường dùng acetone để loại bỏ vết sơn móng tay hay vết mực bút bi dây trên áo. Acetone là hợp chất hữu cơ.
Không thể dùng nước để rửa các vết màu này. Do các vết màu này là các hợp chất hữu cơ ít tan trong nước nhưng lại tan tốt trong các dung môi hữu cơ.
Câu hỏi 3 trang 52 Hoá học 11: Cho phản ứng đốt cháy 1 mol ethanol (C2H6O):
C2H6O(l) + 3O2(g) 2CO2(g) + 3H2O(g)
Lời giải:
nên phản ứng là toả nhiệt.
Nhiệt lượng toả ra là 1 300 kJ nên dễ dàng thấy được phản ứng trên xảy ra thuận lợi. Hay ethanol dễ cháy, khi cháy toả nhiều nhiệt.
III. Phân loại các hợp chất hữu cơ
Lời giải:
- Hydrocarbon là những hợp chất hữu cơ trong phân tử chỉ chứa carbon và hydrogen. Vậy các hydrocarbon là: (1); (4).
- Khi thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nguyên tử hay nhóm nguyên tử khác thì thu được dẫn xuất hydrocarbon. Vậy dẫn xuất hydrocarbon là: (2); (3); (5); (6).
IV. Nhóm chức
Lời giải:
- Nhóm – CHO có trong thành phần của những chất trên đã làm cho chúng có tính chất giống nhau.
A. chỉ thể hiện các tính chất hoá học đặc trưng của alcohol.
B. chỉ thể hiện các tính chất hoá học đặc trưng của aldehyde.
C. thể hiện các tính chất hoá học đặc trưng của cả alcohol và aldehyde.
D. không thể hiện tính chất hoá học đặc trưng của cả alcohol và aldehyde.
Lời giải:
Đáp án đúng là: C
Nhóm chức gây ra tính chất hoá học đặc trưng của hợp chất hữu cơ. Do đó một hợp chất hữu cơ X chứa đồng thời hai nhóm chức alcohol và aldehyde. Khi đó, hợp chất X sẽ thể hiện các tính chất hoá học đặc trưng của cả alcohol và aldehyde.
Lời giải:
Phổ IR này là của hợp chất CH3CH2CH2COOH (B).
Trong đó, tín hiệu 1 712 cm-1 là tín hiệu đặc trưng của liên kết C = O; tín hiệu 2 971 cm-1, 2 860 cm-1, 2 668 cm-1 là tín hiệu đặc trưng của liên kết O – H trong nhóm – COOH.
Bài tập (trang 56)
Bài 1 trang 56 Hoá học 11: Trong các chất dưới đây, chất nào là chất vô cơ, chất nào là chất hữu cơ?
CH3C ≡ CCH2NH2 (7).
Lời giải:
Hợp chất vô cơ: CaCO3 (1); CO (2);
Hợp chất hữu cơ: CH3COONa (3); C6H5CH3 (4); CH3CH2CH2CN (5); CH3CH2SCH3 (6); CH3C ≡ CCH2NH2 (7).
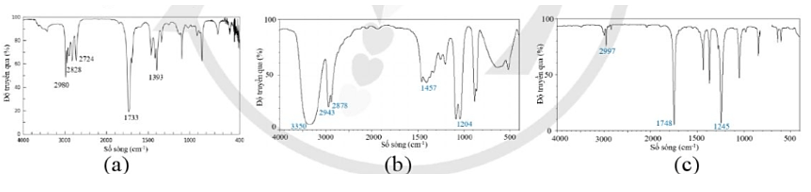
Lời giải:
Ta có:
(1) – (b): Do tín hiệu 3 350 cm-1 là tín hiệu đặc trưng của nhóm – OH ancol;
(2) – (a): Do tín hiệu 1 733 cm-1 là tín hiệu đặc trưng của nhóm C = O; các tín hiệu 2 724 cm-1; 2 828 cm-1 là tín hiệu đặc trưng của liên kết C – H trong nhóm – CHO.
Còn lại: (3) – c.
Bài 3* trang 56 Hoá học 11: Cho phản ứng:
a) Có những nhóm chức nào trong phân tử mỗi chất hữu cơ ở phản ứng trên?
Lời giải:
a) Trong hợp chất 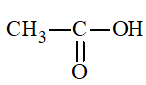
Trong hợp chất CH3CH2OH có nhóm chức – OH.
Trong hợp chất 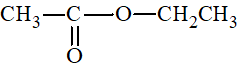
b) Có thể sử dụng phổ hồng ngoại để xác định chất đó là CH3COOCH2CH3 hay CH3COOH hoặc CH3CH2OH. Do mỗi chất này có các nhóm chức khác nhau mà mỗi liên kết trong phân tử hợp chất hữu cơ hấp thụ một vài bức xạ hồng ngoại đặc trưng cho liên kết đó.
Lý thuyết Hợp chất hữu cơ và hoá học hữu cơ
I. Hợp chất hữu cơ và hóa học hữu cơ
-Hợp chất hữu cơ là hợp chất của carbon trừ một số hợp chất như CO, CO2, muối carbonate, các cyanide, carbide,..
-Ngành hóa học nghiên cứu về các hợp chất hữu cơ được gọi là hóa học hữu cơ.
II. Đặc điểm chung của các hợp chất hữu cơ
1.Thành phần nguyên tố
-Ngoài carbon, trong thành phần của hợp chất hữu cơ thường có thêm các nguyên tố khác như: hydrogen, oxygen, nitrogen, phosphorus, các nguyên tố halogen,…
2. Đặc điểm cấu tạo
-Các nguyên tử trong phân tử hợp chất hữu cơ chủ yếu liên kết bằng liên kết cộng hóa trị.
3. Tính chất vật lý
-Đa số hợp chất hữu cơ ít tan trong nước nhưng tan tốt trong dung môi hữu cơ.
-Các hợp chất hữu cơ thường có nhiệt độ nóng chảy và nhiệt độ sôi thấp (dễ bay hơi).
4. Tính chất hóa học
-Phản ứng của hợp chất hữu cơ thường xảy ra chậm và theo nhiều hướng kahcs nhau, tạo thành hỗn hợp các sản phẩm.
-Các hợp chất hữu cơ thường kém bền nhiệt và dễ cháy.
III. Phân loại
-Các hợp chất hữu cơ thường được chia thành 2 nhóm lớn: hydrocarbon và dẫn xuất của hydrocarbon.
-Hydrocarbon: những hợp chất hữu cơ trong phân tử chỉ chứa carbon và hydrogen.
-Dẫn xuất hydrocarbon: thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nguyên tử hay nhóm nguyên tử khác.
IV. Nhóm chức
1. Khái niệm
-Nhóm chức là nguyên tử hay nhóm nguyên tử gây ra những tính chất hóa học đặc trưng của hợp chất hữu cơ.
-Một số loại nhóm chức:-OH; -CHO; -COOH; C=O;…
2. Xác định nhóm chức bằng phổ hồng ngoại
-Có thể xác định được nhóm chức trong phân tử hợp chất hữu cơ dựa vào tín hiệu hấp thụ đặc trưng trên phổ hồng ngoại của nó.
Sơ đồ tư duy Hợp chất hữu cơ và hoá học hữu cơ
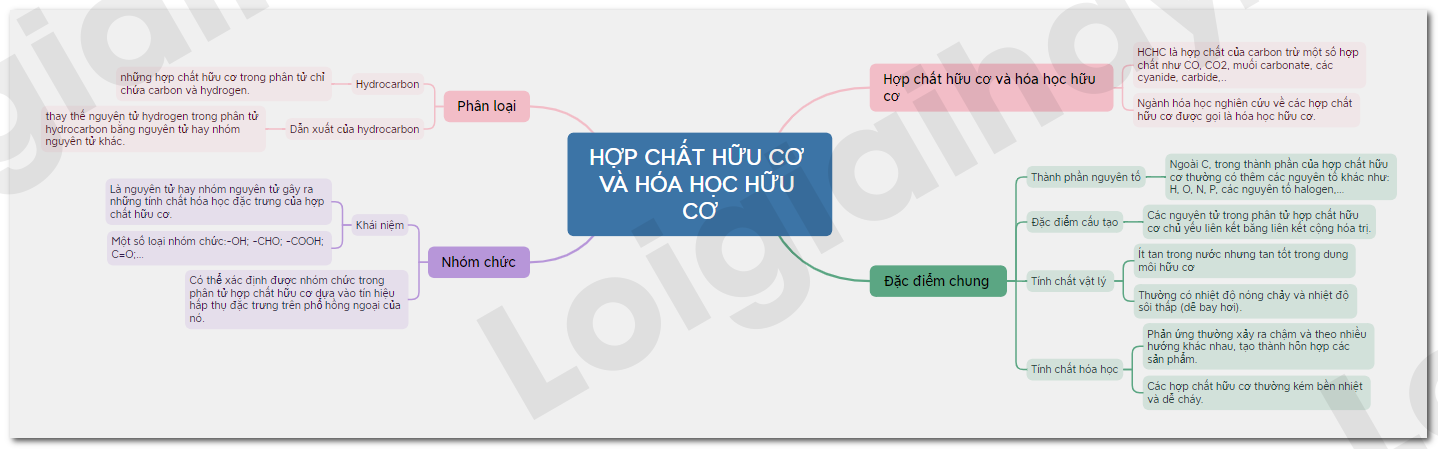
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Bài 6: Sulfur và sulfur dioxide
Bài 7: Sulfuric acid và muối sulfate
Bài 9: Phương pháp tách biệt và tinh chế hợp chất hữu cơ
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Cánh diều (hay nhất)
- Văn mẫu lớp 11 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 11 – Cánh diều
- Tác giả tác phẩm Ngữ văn 11 - Cánh diều
- Giải SBT Ngữ văn 11 – Cánh diều
- Bố cục tác phẩm Ngữ văn 11 – Cánh diều
- Giải Chuyên đề học tập Ngữ văn 11 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Cánh diều
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 – Cánh diều
- Giải Chuyên đề học tập Toán 11 – Cánh diều
- Lý thuyết Toán 11 - Cánh diều
- Giải sbt Toán 11 – Cánh diều
- Giải sgk Tiếng Anh 11 – ilearn Smart World
- Giải sbt Tiếng Anh 11 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 11 ilearn Smart World đầy đủ nhất
- Giải sgk Vật lí 11 – Cánh diều
- Lý thuyết Vật lí 11 – Cánh diều
- Giải sbt Vật lí 11 – Cánh diều
- Giải Chuyên đề học tập Vật lí 11 – Cánh diều
- Giải sgk Sinh học 11 – Cánh diều
- Lý thuyết Sinh học 11 – Cánh diều
- Giải Chuyên đề học tập Sinh học 11 – Cánh diều
- Giải sbt Sinh học 11 – Cánh diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Cánh diều
- Lý thuyết Kinh tế pháp luật 11 – Cánh diều
- Giải sbt Kinh tế pháp luật 11 – Cánh diều
- Giải sgk Lịch sử 11 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 11 – Cánh diều
- Lý thuyết Lịch sử 11 - Cánh diều
- Giải sbt Lịch sử 11 – Cánh diều
- Giải sgk Địa lí 11 – Cánh diều
- Giải Chuyên đề học tập Địa lí 11 – Cánh diều
- Lý thuyết Địa lí 11 - Cánh diều
- Giải sbt Địa lí 11 – Cánh diều
- Giải sgk Công nghệ 11 – Cánh diều
- Lý thuyết Công nghệ 11 - Cánh diều
- Giải sbt Công nghệ 11 – Cánh diều
- Giải sgk Tin học 11 – Cánh diều
- Giải Chuyên đề học tập Tin học 11 – Cánh diều
- Lý thuyết Tin học 11 - Cánh diều
- Giải sbt Tin học 11 – Cánh diều
- Giải sgk Giáo dục quốc phòng an ninh 11 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 11 – Cánh diều
- Giải sbt Giáo dục quốc phòng 11 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 – Cánh diều