Giải Hóa 11 Bài 15 (Cánh diều): Dẫn xuất halogen
Với giải bài tập Hóa 11 Bài 15: Dẫn xuất halogen sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 11 Bài 15.
Giải Hóa 11 Bài 15: Dẫn xuất halogen
Lời giải:
Nhờ có sự phân cực của liên kết C – X, dẫn xuất halogen dễ tham gia vào nhiều phản ứng hoá học. Hai loại phản ứng hoá học quan trọng nhất của dẫn xuất halogen là phản ứng thế nguyên tử halogen và phản ứng tách hydrogen halide.
Dẫn xuất halogen có nhiều ứng dụng trong đời sống, công nghiệp hoá chất và y học.
- Các dẫn xuất halogen như chloroform (CHCl3), carbon tetrachloride (CCl4), methylene dichloride (CH2Cl2), … là những chất lỏng dễ bay hơi, hoà tan được nhiều chất hữu cơ nên chúng được sử dụng là dung môi trong phòng thí nghiệm và công nghiệp.
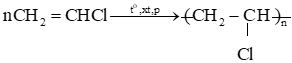
- Một số dẫn xuất halogen được sử dụng làm monomer trong tổng hợp các polymer. Ví dụ, từ vinyl chloride tổng hợp được poly(vinyl chloride) (nhựa PVC) để làm ống nước, vỏ bọc dây điện, vải giả da, … Từ 2 – chlorobuta – 1,3 – diene tổng hợp ra poly(2 – chlorobuta – 1,3 – diene) ứng dụng trong sản xuất cao su chloroprene để chế tạo ống, băng tải cao su chịu nhiệt dùng trong khai thác mỏ; các sản phẩm đúc, con dấu, vòng đệm, … Trùng hợp tetrafluoroethylene thu được polytetrafluoroethylene hay teflon được ứng dụng trong sản xuất chảo chống dính, vật liệu cách điện, các ống chịu hoá chất, bình phản ứng …
- Dẫn xuất halogen còn được sử dụng để tổng hợp alcohol, ether, … hoặc các chất cơ nguyên tố.
- Dẫn xuất halogen có hoạt tính sinh học đa dạng. Ví dụ, chloroform, ethyl chloride, halothane được sử dụng làm chất gây mê trong y học. Ethyl chloride được dùng làm chất giảm đau tạm thời cho các chấn thương nhỏ trong thể thao. Methyl bromide là một chất khử trùng, tiêu diệt nhiều loại dịch hại như nhện, ve, nấm, côn trùng … Các chất như 2,4 – dichlorophenoxyacetic acid (2,4 – D) và 2,4,5 – trichlorophenoxyacetic acid (2,4,5 – T) ở nồng độ thấp (vài phần triệu) có tác dụng kích thích sinh trưởng thực vật nhưng ở nồng độ cao có tác dụng diệt cây cỏ nên được dùng làm chất diệt cỏ, phát quang rừng rậm …
- Các hợp chất chỉ chứa chlorine, fluorine và carbon trong phân tử được gọi chung là các hợp chất CFC hay freon trước đây được sử dụng trong công nghệ làm lạnh (điều hoà, tủ lạnh) nhưng do các chất này có thể phá huỷ tầng ozone nên hiện nay các hợp chất CFC này đã được thay thế bằng các hợp chất HFC (tức hydrofluorocarbon).
Lời giải:
|
Hydrocarbon |
Dẫn xuất halogen tương ứng |
|
CH4 |
CH3Cl; CH2Cl2; CHCl3; CCl4; CH3Br; CHI3 … |
|
CH3 – CH3 |
CH3CH2Cl; CH2Br – CH2Br, … |
|
CH2 = CH2 |
CH2 = CHCl; CF2 = CF2, … |
|
C6H6 |
C6H5Br; C6H5Cl … |
I. Khái niệm đồng phân và danh pháp
Lời giải:
Các đồng phân cấu tạo có cùng công thức phân tử là C4H9Cl:
(1) CH3 – CH2 – CH2 – CH2 – Cl: 1 – chlorobutane.
(2) CH3 – CHCl – CH2 – CH3: 2 – chlorobutane.
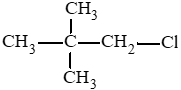
(3) 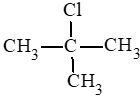
(4) 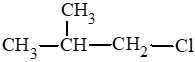
Đồng phân mạch carbon: (1) và (4); (2) và (3).
Đồng phân vị trí nhóm chức: (1) và (2); (3) và (4).
Lời giải:
CH3 – CH2 – CH2 – CH2 – CH2Cl: 1 – chloropentane.
CH3 – CHCl – CH2 – CH2 – CH3: 2 – chloropentane.
CH3 – CH2 – CHCl – CH2 – CH3: 3 – chloropentane.
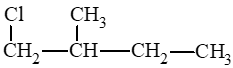
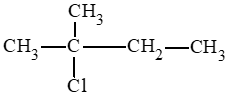
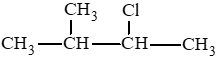
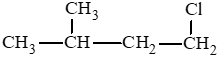
Lời giải:
Ta có dự đoán sau:
|
Chất |
CH3F |
CH3Cl |
CH3Br |
CH3I |
|
tosôi |
-78 oC |
-24 oC |
4 oC |
42 oC |
Giải thích dự đoán: Với các dẫn xuất halogen cùng gốc alkyl nhiệt độ sôi tăng theo chiều tăng của nguyên tử khối halogen.
Lời giải:
|
Liên kết |
C – C |
C – H |
C – Cl |
|
Hiệu độ âm điện |
0 |
0,35 |
0,96 |
Nhận xét: độ phân cực của liên kết tăng dần theo thứ tự: C – C, C – H, C – Cl.
II. Tính chất vật lí
Lời giải:
Ta có dự đoán sau:
|
Chất |
CH3F |
CH3Cl |
CH3Br |
CH3I |
|
tosôi |
-78 oC |
-24 oC |
4 oC |
42 oC |
Giải thích dự đoán: Với các dẫn xuất halogen cùng gốc alkyl nhiệt độ sôi tăng theo chiều tăng của nguyên tử khối halogen.
III. Tính chất hoá học
Lời giải:
|
Liên kết |
C – C |
C – H |
C – Cl |
|
Hiệu độ âm điện |
0 |
0,35 |
0,96 |
Nhận xét: độ phân cực của liên kết tăng dần theo thứ tự: C – C, C – H, C – Cl.
Lời giải:
Ban đầu hỗn hợp tách thành hai lớp do dẫn xuất halogen không tan trong nước. Trong đó, dẫn xuất halogen ở lớp dưới do nặng hơn nước.
Sau phản ứng thêm tiếp AgNO3 vào ống nghiệm thấy có kết tủa xuất hiện do:
Ag+ + X- → AgX (với X: Cl, Br, I).
Lời giải:
Các phương trình hoá học xảy ra:
CH3Cl + NaOH CH3OH + NaCl
CH3CHClCH3 + NaOH CH3CH(OH)CH3 + NaCl
C6H5CH2Br + NaOH C6H5CH2OH + NaBr
CH2 = CHCH2Cl + NaOH CH2 = CHCH2OH + NaCl.
Câu hỏi 4 trang 103 Hóa học 11: Trong thí nghiệm Thuỷ phân dẫn xuất halogen, cho biết:
Lời giải:
a) Cho nước vào ống nghiệm chứa dẫn xuất halogen sau đó thử phần nước bằng dung dịch silver nitrate nhằm mục đích rửa ion halide, kiểm tra nước rửa còn ion halide hay không.
b) Cần acid hoá dung dịch sau khi thuỷ phân bằng dung dịch HNO3 trước khi cho dung dịch AgNO3 để tránh sinh ra kết tủa Ag2O làm sai lệch kết quả thí nghiệm. Cụ thể, nếu còn base dư có thêm phản ứng:
AgNO3 + NaOH → AgOH + NaNO3
2AgOH (không bền) → Ag2O + H2O.
Không thể thay thế dung dịch HNO3 bằng các dung dịch H2SO4 hay HCl vì các acid này đều tạo kết tủa với AgNO3, làm sai lệch kết quả thí nghiệm.
Lời giải:
Các phương trình hoá học xảy ra:
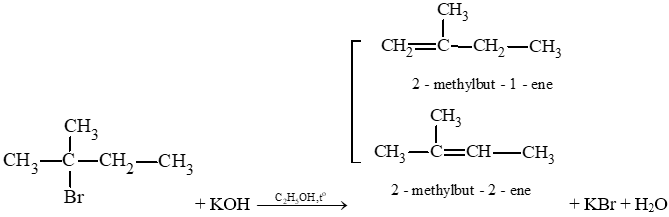
a) CH3 – CHCl – CH3 + KOH CH2 = CH – CH3 + KCl + H2O
Các sản phẩm sinh ra: propene, potassium chloride, nước.
b)
IV: Ứng dụng của dẫn xuất halogen
Câu hỏi 5 trang 104 Hóa học 11: Trình bày một số ứng dụng trong thực tiễn của dẫn xuất halogen.
Lời giải:
Một số ứng dụng trong thực tiễn của dẫn xuất halogen:
- Các dẫn xuất halogen như chloroform (CHCl3), carbon tetrachloride (CCl4), methylene dichloride (CH2Cl2), … được sử dụng là dung môi trong phòng thí nghiệm và công nghiệp.
- Một số dẫn xuất halogen được sử dụng làm monomer trong tổng hợp các polymer.
- Dẫn xuất halogen còn được sử dụng để tổng hợp alcohol, ether, … hoặc các chất cơ nguyên tố.
- Dẫn xuất halogen có hoạt tính sinh học đa dạng. Ví dụ, chloroform, ethyl chloride, halothane được sử dụng làm chất gây mê trong y học. Ethyl chloride được dùng làm chất giảm đau tạm thời cho các chấn thương nhỏ trong thể thao….
Lời giải:
Chất diệt cỏ, chất kích thích tăng trưởng 2,4 – D và 2,4,5 – T là các chất hoá học, có đặc tính khó phân huỷ, tồn dư lâu trong môi trường và có tác hại đến sức khoẻ con người, do đó không nên lạm dụng các chất này.
Lời giải:
Các hợp chất chỉ chứa chlorine, fluorine và carbon trong phân tử được gọi chung là các hợp chất CFC hay freon trước đây được sử dụng trong công nghệ làm lạnh (điều hoà, tủ lạnh) nhưng do các chất này có thể phá huỷ tầng ozone nên hiện nay các hợp chất CFC này đã được thay thế bằng các hợp chất HFC (tức hydrofluorocarbon).
Bài tập (trang 106)
a) Gọi tên các chất trên theo danh pháp thay thế.
b) Viết phương trình hoá học của phản ứng điều chế các chất trên từ hydrocarbon tương ứng.
Lời giải:
|
Dẫn xuất halogen |
a) Danh pháp thay thế |
b) PTHH điều chế |
|
CH3Cl |
chloromethane |
CH4 + Cl2 CH3Cl + HCl |
|
CH3CH2Cl |
chloroethane |
CH3CH3 + Cl2 CH3CH2Cl + HCl |
|
C6H5Br |
bromobenzene |
C6H6 + Br2 C6H5Br + HBr |
|
CHCl3 |
1,1,1 - trichloromethane |
CH4 + 3Cl2 CHCl3 + 3HCl |
|
CH2BrCH2Br |
1,2 - dibromoethane |
CH2 = CH2 + Br2 → CH2BrCH2Br |
Lời giải:
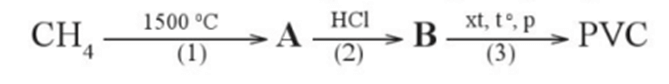
2CH4 CH ≡ CH + 3H2
CH ≡ CH + HCl CH2 = CHCl
Sơ đồ được hoàn thành:
CH4 CH ≡ CH CH2 = CHCl PVC.
Bài 3 trang 106 Hóa học 11: Ethyl chloride hoá lỏng được sử dụng làm thuốc xịt có tác dụng giảm đau tạm thời khi chơi thể thao.
Khi xịt thuốc vào chỗ đau thì người ta cảm giác nóng hay lạnh?
b) Viết phương trình hoá học của phản ứng điều chế ethyl chloride từ ethane.
Lời giải:
a) Quá trình C2H5Cl(l) ⇌ C2H5Cl(g) có > 0 nên quá trình này thu nhiệt. Do đó, khi xịt thuốc vào chỗ đau thì người ta có cảm giác lạnh.
b) Phương trình hoá học điều chế:
CH3CH3 + Cl2 CH3CH2Cl + HCl.
Lý thuyết Dẫn xuất halogen
I. Khái niệm, đồng phân và danh pháp
1. Khái niệm
- Khi thay thế nguyên tử hydrogen của phân tử hydrocarbon bằng nguyên tử halogen được dẫn xuất halogen của hydrocarbon.
2. Đồng phân
- Đồng phân mạch carbon và đồng phân vị trí nhóm chức.
3. Danh pháp
- Tên thay thế của dẫn xuất halogen được gọi như sau:
Số chỉ vị trí nhóm thế-tên nhóm thế+tên mạch chính
- Một số dẫn xuất halogen được gọi theo tên thông thường.
II. Tính chất vật lý
- Chất có phân tử khối nhỏ (CH3F, CH3Cl, CH3Br) ở thể khí, các chất có phân tử khối lớn hơn thường ở thể lỏng.
- Hầu như không tan trong nước.
III. Tính chất hóa học
1. Phản ứng thế nguyên tử halogen bằng nhóm –OH
![]()
- Phản ứng này còn được gọi là phản ứng thủy phân dẫn xuất halogen.
2. Phản ứng tách hydrogen halide

- Quy tắc Zaitsev: trong phản ứng tách HX ra khỏi dẫn xuất halogen, nguyên tử X ưu tiên tách ra cùng với nguyên tử H ở nguyên C bên cạnh có bậc cao hơn, tạo ra sản phẩm chính.
IV. Ứng dụng của dẫn xuất halogen
Dẫn xuất halogen có nhiều ứng dụng trong đời sống, công nghiệp hóa chất và y học.
- Có thể được sử dụng làm dung môi.
- Một số dẫn xuất halogen được sử dụng để tổng hợp polymer.
- Được sử dụng để tổng hợp alcohol, ether,…
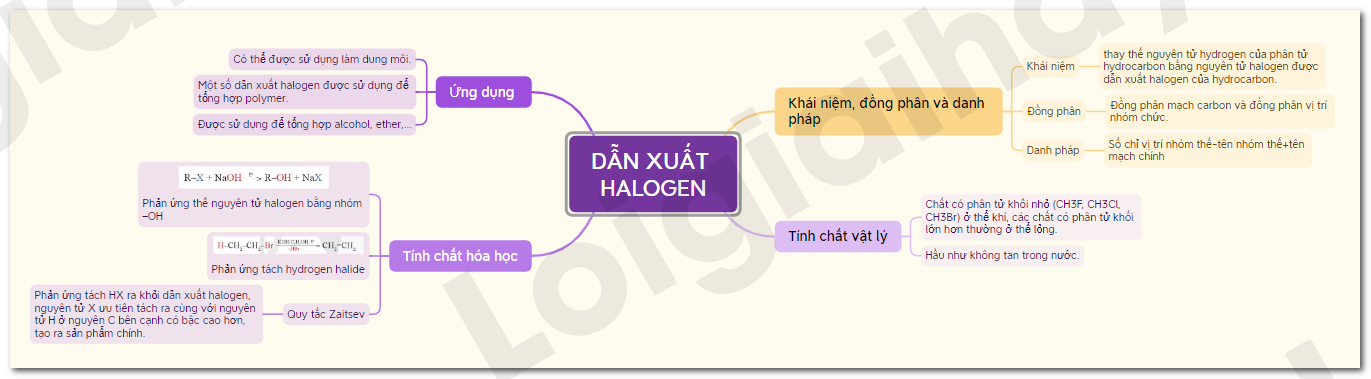
Sơ đồ tư duy Dẫn xuất halogen
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Cánh diều (hay nhất)
- Văn mẫu lớp 11 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 11 – Cánh diều
- Tác giả tác phẩm Ngữ văn 11 - Cánh diều
- Giải SBT Ngữ văn 11 – Cánh diều
- Bố cục tác phẩm Ngữ văn 11 – Cánh diều
- Giải Chuyên đề học tập Ngữ văn 11 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Cánh diều
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 – Cánh diều
- Giải Chuyên đề học tập Toán 11 – Cánh diều
- Lý thuyết Toán 11 - Cánh diều
- Giải sbt Toán 11 – Cánh diều
- Giải sgk Tiếng Anh 11 – ilearn Smart World
- Giải sbt Tiếng Anh 11 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 11 ilearn Smart World đầy đủ nhất
- Giải sgk Vật lí 11 – Cánh diều
- Lý thuyết Vật lí 11 – Cánh diều
- Giải sbt Vật lí 11 – Cánh diều
- Giải Chuyên đề học tập Vật lí 11 – Cánh diều
- Giải sgk Sinh học 11 – Cánh diều
- Lý thuyết Sinh học 11 – Cánh diều
- Giải Chuyên đề học tập Sinh học 11 – Cánh diều
- Giải sbt Sinh học 11 – Cánh diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Cánh diều
- Lý thuyết Kinh tế pháp luật 11 – Cánh diều
- Giải sbt Kinh tế pháp luật 11 – Cánh diều
- Giải sgk Lịch sử 11 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 11 – Cánh diều
- Lý thuyết Lịch sử 11 - Cánh diều
- Giải sbt Lịch sử 11 – Cánh diều
- Giải sgk Địa lí 11 – Cánh diều
- Giải Chuyên đề học tập Địa lí 11 – Cánh diều
- Lý thuyết Địa lí 11 - Cánh diều
- Giải sbt Địa lí 11 – Cánh diều
- Giải sgk Công nghệ 11 – Cánh diều
- Lý thuyết Công nghệ 11 - Cánh diều
- Giải sbt Công nghệ 11 – Cánh diều
- Giải sgk Tin học 11 – Cánh diều
- Giải Chuyên đề học tập Tin học 11 – Cánh diều
- Lý thuyết Tin học 11 - Cánh diều
- Giải sbt Tin học 11 – Cánh diều
- Giải sgk Giáo dục quốc phòng an ninh 11 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 11 – Cánh diều
- Giải sbt Giáo dục quốc phòng 11 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 – Cánh diều