Lý thuyết Thế điện cực và nguồn điện hoá học – Hóa lớp 12 Kết nối tri thức
Với lý thuyết Hóa lớp 12 Bài 15: Thế điện cực và nguồn điện hoá học chi tiết, ngắn gọn và bài tập tự luyện có lời giải chi tiết sách Kết nối tri thức sẽ giúp học sinh nắm vững kiến thức trọng tâm để học tốt môn Hóa 12.
Lý thuyết Hóa 12 Bài 15: Thế điện cực và nguồn điện hoá học- Kết nối tri thức
A. Lý thuyết Thế điện cực và nguồn điện hoá học
I. Cặp oxi hóa – khử
- Xét một quá trình có ion kim loại Mn+ đóng vai trò là chất oxi hóa và một quá trình kim loại M đóng vai trò là chất khử như sau:
Mn+ + ne → M
M →Mn+ + ne
- Trong trường hợp trên, chất oxi hóa (dạng oxi hóa) Mn+và chất khử (dạng khử). M thuộc cùng một nguyên tố kim loại. Quá trình trên được viết gọn như sau:
Mn+ + ne →←\vboxto.5ex\vss M
Dạng oxi hóa Dạng khử
- Dạng oxi hóa và dạng khử của cùng một nguyên tố kim loại tạo nên cặp oxi hóa – khử của kim loại đó.
II. Thế điện cực chuẩn
1. Điện cực
Ứng với mỗi cặp oxi hóa – khử có thể thiết lập một điện cực, tại đó tồn tại cân bằng giữa dạng oxi hóa và dạng khử.
2. Thế điện cực chuẩn
Thế điện cực của cặp oxi hóa – khử của kim loại trong điều kiện chuẩn (nồng độ ion kim loại trong dung dịch là 1M, nhiệt độ 25oC) được gọi là thế điện cực chuẩn của kim loại, kí hiệu là Eooxh/kh
Đơn vị thường sử dụng của thế điện cực là volt (V)
- Giá trị thế điện cực chuẩn càng nhỏ thì dạng khử có tính khử càng mạnh, dạng oxi hóa có tính oxi hóa càng yếu
- Giá trị thế điện cực chuẩn càng lớn thì dạng khử có tính khử càng yếu, dạng oxi hóa có tính oxi hóa càng mạnh.
3. Ý nghĩa của thế điện cực chuẩn
a) So sánh tính khử, tính oxi hóa giữa các cặp oxi hóa – khử
Giữa hai cặp oxi hóa – khử, cặp có giá trị thế điện cực chuẩn nhỏ hơn thì dạng khử có tính khử mạnh hơn, còn dạng oxi hóa có tính oxi hóa yếu hơn và ngược lại.
Trên cơ sở so sánh giá trị thế điện cực chuẩn, các cặp oxi hóa – khử Mn+/M được sắp xếp thành dãy theo chiều tăng dần thế điện cực chuẩn, thường gọi là dãy điện hóa của kim loại
b) Dự đoán chiều phản ứng giữa hai cặp oxi hóa – khử
- Chiều của phản ứng giữa hai cặp oxi hóa – khử có thể dự đoán được từ việc so sánh giá trị thế điện cực chuẩn
- Chất khử của cặp oxi hóa – khử có thế điện cực nhỏ hơn tác dụng với chất oxi hóa cặp oxi hóa – khử có thế điện cực lớn hơn, tạo ra dạng oxi hóa và dạng khử tương ứng
- Chất khử của cặp oxi hóa – khử đứng trước tác dụng với chất oxi hóa của cặp oxi hóa – khử đứng sau, tạo ra dạng oxi hóa và dạng khử tương ứng.
Hai cách dự đoán trên được minh họa thông qua quy tắc α
III. Pin điện hóa
1. Phản ứng oxi hóa – khử và dòng điện
Phản ứng oxi hóa – khử luôn kèm theo sự chuyển electron từ chất khử sang chất oxi hóa. Nếu các quá trình oxi hóa, quá trình lhử xảy ra trên hai điện cực và electron được truyền từ chất khử sang chất oxi hóa qua dây dẫn thì năng lượng của phản ứng hóa học sẽ chuyển thành năng lượng điện.
2. Pin Galvani
- Pin Galvani là pin điện hóa có cấu tạo gồm hai điện cực, mỗi điện cực ứng với một cặp oxi hóa – khử và thường nối với nhau qua cầu muối.
- Sức điện động của pin đo ở điều kiện chuẩn gọi là sức điện động chuẩn. Sức điện động chuẩn có thể xác định dựa vào thế điện cực chuẩn của các cặp oxi hóa – khử tương ứng: Eopin=Eocathode−Eoanode
IV. Một số loại pin khác
Acquy là nguồn điện được sử dụng phổ biến trong các phương tiện giao thông, thiết bị lưu điện, phát điện.
- Pin nhiên liệu: hoạt động dựa trên phản ứng oxi hóa – khử giữa nhiên liệu và chất oxi hóa. Pin nhiên liệu phổ biến hiện nay là pin hydrogen. Ưu điểm của pin nhiên liệu là nhiên liệu được bổ sung liên tục nên thời gian hoạt động của pin không bị hạn chế. Nhược điểm của pin nhiên liệu là công nghiệp chưa được phổ biến và giá thành cao.
- Pin mặt trời bao gồm nhiều tế bào quang điện làm biến đổi năng lượng ánh sáng thành năng lượng điện. Ưu điểm tạo được nguồn năng lượng xanh, thân thiện với môi trường, chi phí không quá cao, sử dụng lâu dài tuy nhiên, pin mặt trời cần được lắp đặt trên không gian rộng để pin tiếp xúc trực tiếp với ánh sáng mặt trời. Loại pin này khó di chuyển.
B. Trắc nghiệm Thế điện cực và nguồn điện hoá học
Đang cập nhật …
C. Sơ đồ tư duy Thế điện cực và nguồn điện hoá học
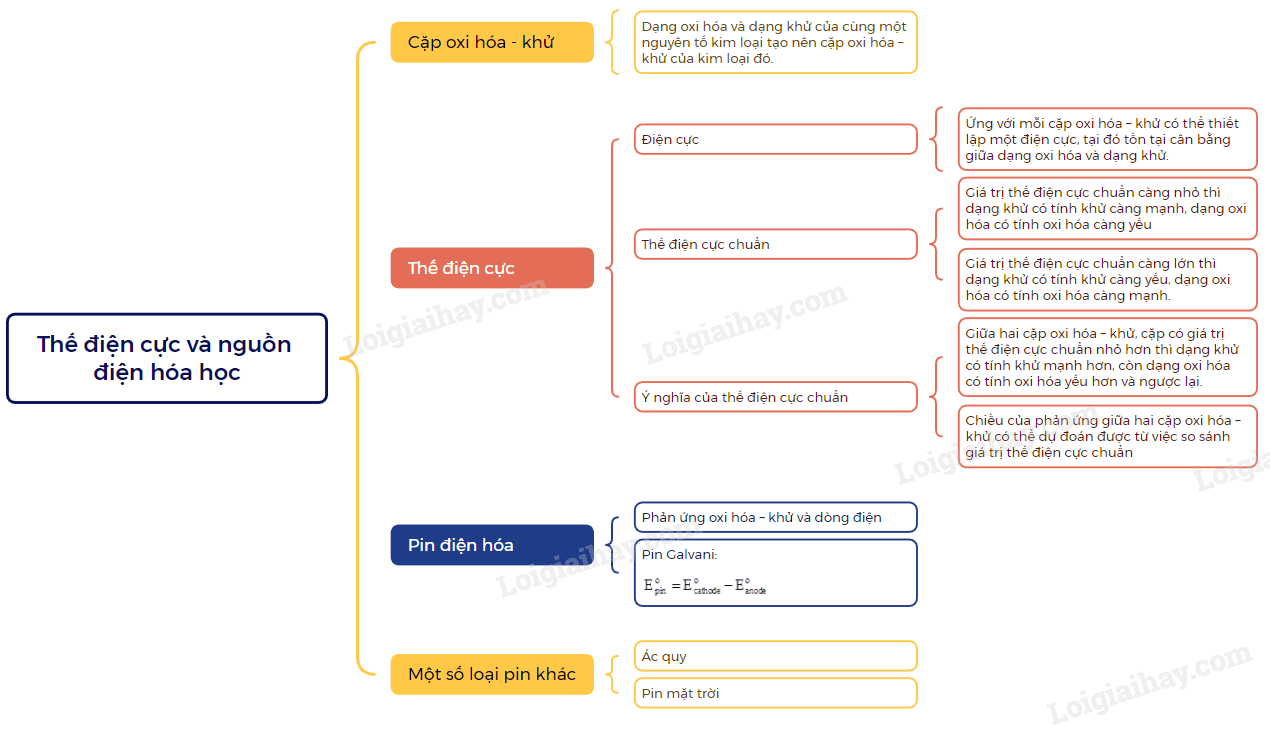
Xem thêm các chương trình khác:
- Soạn văn 12 Kết nối tri thức (hay nhất)
- Văn mẫu 12 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 12 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 12 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 12 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 12 – Kết nối tri thức
- Giải sgk Toán 12 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 12 – Kết nối tri thức
- Lý thuyết Toán 12 – Kết nối tri thức
- Giải sbt Toán 12 – Kết nối tri thức
- Bài tập Tiếng Anh 12 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 12 - Global success
- Trọn bộ Từ vựng Tiếng Anh 12 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 12 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 12 – Global Success
- Giải sgk Vật lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Vật lí 12 – Kết nối tri thức
- Lý thuyết Vật lí 12 – Kết nối tri thức
- Giải sbt Vật lí 12 – Kết nối tri thức
- Giải sgk Sinh học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 12 – Kết nối tri thức
- Lý thuyết Sinh học 12 – Kết nối tri thức
- Giải sbt Sinh học 12 – Kết nối tri thức
- Giải sgk Lịch sử 12 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 12 – Kết nối tri thức
- Giải sbt Lịch sử 12 – Kết nối tri thức
- Giải sgk Địa lí 12 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 12 – Kết nối tri thức
- Giải sbt Địa lí 12 – Kết nối tri thức
- Giải sgk Tin học 12 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 12 – Kết nối tri thức
- Giải sbt Tin học 12 – Kết nối tri thức
- Lý thuyết Tin học 12 - Kết nối tri thức
- Giải sgk Công nghệ 12 – Kết nối tri thức
- Giải sgk Kinh tế pháp luật 12 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 12 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng 12 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 12 – Kết nối tri thức
