Lý thuyết Hóa 10 Bài 24: Sơ lược về hợp chất có oxi của clo
Tóm tắt lý thuyết Hóa 10 Bài 24: Sơ lược về hợp chất có oxi của clo ngắn gọn, chi tiết sẽ giúp học sinh nắm vững kiến thức trọng tâm Hóa 10 Bài 24.
Lý thuyết Hóa 10 Bài 24: Sơ lược về hợp chất có oxi của clo
Bài giảng Hóa 10 Bài 24: Sơ lược về hợp chất có oxi của clo
I. Nước Gia –ven
- Thành phần: Nước gia – ven là dung dịch hỗn hợp muối NaCl và NaClO (natri hipoclorit).

Hình 1: Nước Gia – ven (Javel)
- Tính chất:
+ Muối NaClO có tính oxi hóa mạnh.
+ NaClO là muối của axit yếu (yếu hơn axit cacbonic), trong không khí nó tác dụng dần với CO2 tạo ra HClO không bền. Phương trình hóa học:
NaClO + CO2 + H2O → NaHCO3 + HClO
Cả NaClO và HClO đều có tính oxi hóa mạnh.
- Điều chế:
+ Trong phòng thí nghiệm, nước gia – ven được điều chế bằng cách cho khí clo tác dụng với NaOH loãng ở điều kiện thường:
Cl2 + 2NaOH → NaCl + NaClO + H2O
+ Trong công nghiệp, nước gia – ven được điều chế bằng cách điện phân dung dịch muối ăn, nồng độ từ 15% - 20%, trong thùng điện phân không có màng ngăn:
2NaCl + 2H2O → 2NaOH + Cl2 + H2
Do không có màng ngăn nên Cl2 tác dụng với NaOH tạo thành nước gia – ven:
Cl2 + 2NaOH → NaCl + NaClO + H2O
- Ứng dụng: Muối NaClO có tính oxi hóa rất mạnh, do đó nước Gia – ven có tính tẩy màu và sát trùng, dùng để tẩy trắng vải, sợi, giấy và dùng để tẩy uế chuồng trại chăn nuôi, nhà vệ sinh.
II. Clorua vôi
Clorua vôi là chất bột màu trắng, xốp.

Hình 2: Clorua vôi
- Công thức:
Công thức phân tử của clorua vôi là CaOCl2 và có công thức cấu tạo là:
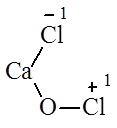
⇒ Clorua vôi là muối hỗn tạp do là muối của kim loại Ca với hai loại gốc axit là Cl- và ClO-.
- Tính chất:
+ Clorua vôi có tính oxi hóa mạnh, tương tự nước gia -ven.
+ Trong không khí, clorua vôi tác dụng dần với CO2 và hơi nước giải phóng HClO. Phương trình hóa học:
2CaOCl2 + CO2 + H2O → CaCO3 + CaCl2 + 2HClO
- Điều chế: Cho clo tác dụng với vôi tôi hoặc sữa vôi ở 30oC:
Cl2 + Ca(OH)2 CaOCl2 + H2O
- Ứng dụng:
+ Clorua vôi có tính oxi hóa mạnh nên dùng tẩy trắng vải, sợi, giấy.
+ So với nước gia – ven, clorua vôi rẻ tiền hơn, hàm lượng hipoclorit cao hơn nên được dùng để tẩy uế hố rác, cống rãnh, chồng trại chăn nuôi …
+ Một lượng lớn clorua vôi được dùng để tinh chế dầu mỏ. Do có khả năng tác dụng với các chất hữu cơ, clorua vôi được dùng để xử lý chất độc, bảo vệ môi trường.
Xem thêm các bài tổng hợp lý thuyết Hóa học lớp 10 đầy đủ, chi tiết khác:
Lý thuyết Bài 25: Flo – brom – iot
Lý thuyết Bài 26: Luyện tập nhóm halogen
Lý thuyết Bài 32: Hiđro sunfua – lưu huỳnh đioxit – lưu huỳnh trioxit
Xem thêm các chương trình khác:
- Giải sgk Vật Lí 10 | Giải bài tập Vật lí 10 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Vật Lí 10
- Tóm tắt tác phẩm Ngữ văn 10
- Soạn văn 10 (hay nhất) | Để học tốt Ngữ Văn 10 (sách mới)
- Soạn văn 10 (ngắn nhất) | Để học tốt Ngữ văn 10 (sách mới)
- Văn mẫu lớp 10 (cả ba sách) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Lịch sử 10 | Giải bài tập Lịch sử 10 Học kì 1, Học kì 2 (sách mới)
