Lý thuyết Khoa học tự nhiên 7 Bài 2. Nguyên tử - Kết nối tri thức
Tóm tắt lý thuyết Khoa học tự nhiên lớp 7 Bài 2. Nguyên tử ngắn gọn, chi tiết sách Kết nối tri thức sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Khoa học tự nhiên 7.
Lý thuyết Khoa học tự nhiên 7 Bài 2. Nguyên tử
I. Quan niệm ban đầu về nguyên tử
- Theo Đê – mô – crit: sự tồn tại của một loại hạt vô cùng nhỏ (được gọi là nguyên tử) tạo nên sự đa dạng của vạn vật. Khởi nguồn của quan niệm nguyên tử là sự chia nhỏ một vật sẽ đến một giới hạn “không thể phân chia được”.
- Theo Đan – tơn: Có các đơn vị chất tối thiểu (được gọi là nguyên tử) để các chất tác dụng vừa đủ với nhau theo các lượng xác định.
II. Mô hình nguyên tử của Rơ-dơ-pho – Bo
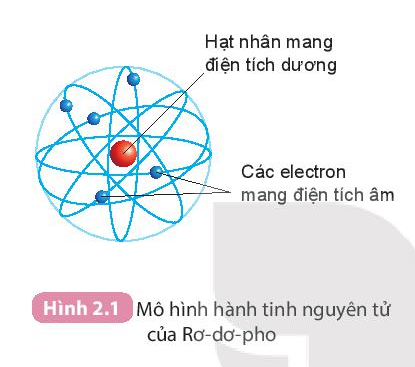
- Rơ-dơ-pho (E.Rutherford) (1871 – 1937), nhà vật lí người Niu-di-lân (New ZeaLand) đã đề xuất mô hình nguyên tử như sau:
+ Nguyên tử có cấu tạo rỗng.
+ Nguyên tử gồm: Hạt nhân ở tâm mang điện tích dương và các electron mang điện tích âm.
+ Các electron chuyển động xung quanh hạt nhân như các hành tinh quay xung quanh Mặt Trời.
- Bo (N. Bohr) (1885 – 1962), nhà vật lí người Đan Mạch, đã hoàn thiện mô hình nguyên tử của Rơ-dơ-pho như sau:
+ Các electron chuyển động xung quanh hạt nhân theo từng lớp khác nhau.
+ Lớp electron trong cùng chứa tối đa 2 electron và bị hạt nhân hút mạnh nhất.
+ Các lớp electron khác chứa tối đa 8 electron hoặc nhiều hơn và bị hạt nhân hút yếu hơn.
Ví dụ:
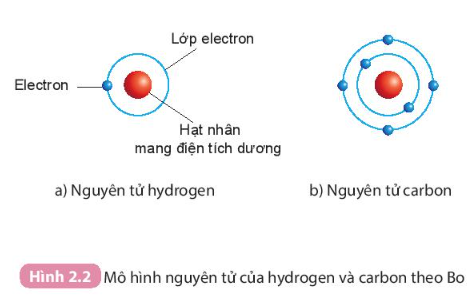
Theo mô hình nguyên tử của Bo
- Nguyên tử carbon gồm:
+ Hạt nhân ở tâm mang điện tích dương.
+ Có 6 electron chuyển động xung quanh hạt nhân và được sắp xếp thành hai lớp:
Lớp thứ nhất (lớp trong cùng gần hạt nhân nhất) có 2 electron.
Lớp thứ hai có 4 electron.
Mở rộng: Lịch sử tìm ra các hạt tạo nên nguyên tử
- Bằng các thí nghiệm vật lí, Tôm-xơn (J.J.Thomson) (1856-1940), nhà vật lí người Anh, đã xác định được electron, kí hiệu là e, là một thành phần tạo nên nguyên tử và mang điện tích âm.
- Qua thí nghiệm bắn phá lá vàng, Rơ-dơ-pho đã xác định được nguyên tử có cấu tạo rỗng và có hạt nhân ở tâm.
- Bằng cách bắn phá các hạt nhân nguyên tử, Rơ-dơ-pho đã tìm ra hạt proton mang điện tích dương và Chat-uých (J.Chadwick) đã tìm ra hạt neutron không mang điện, đó là các hạt tạo nên hạt nhân nguyên tử.
III. Cấu tạo nguyên tử
1. Hạt nhân nguyên tử
- Nguyên tử có kích thước vô cùng nhỏ, chỉ khoảng một phần mười tỉ mét. Kích thước của hạt nhân còn nhỏ hơn nữa và chỉ bằng khoảng một phần mười ngàn kích thước của nguyên tử.
- Hạt nhân nguyên tử được tạo thành từ các hạt proton và neutron.
+ Hạt proton kí hiệu là p. Mỗi hạt proton mang một đơn vị điện tích dương, quy ước là +1.
+ Hạt neutron khí hiệu n. Hạt neutron không mang điện.
- Số đơn vị điện tích hạt nhân, kí hiệu là Z, bằng tổng số proton có trong hạt nhân.
Ví dụ:
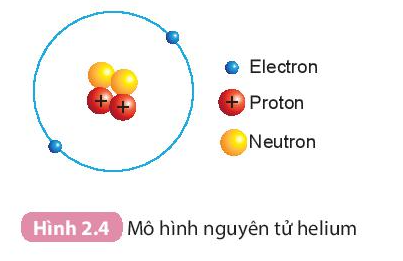
- Hạt nhân nguyên tử helium có 2p, 2n.
- Helium có 2 proton trong hạt nhân ⇒ Số đơn vị điện tích hạt nhân của helium bằng 2.
2. Vỏ nguyên tử
- Vỏ nguyên tử được cấu tạo nên bởi các electron, kí hiệu là e.
- Mỗi electron mang một đơn vị điện tích âm, quy ước là -1.
- Các electron được sắp xếp thành từng lớp:
+ Lớp thứ nhất (trong cùng, gần hạt nhân nhất) có tối đa 2 electron;
+ Lớp thứ hai có tối đa 8 electron…
- Các electron sắp xếp vào các lớp theo thứ tự từ trong ra ngoài cho đến hết.
- Các electron lớp ngoài cùng quyết định tính chất hóa học của nguyên tử.
Ví dụ:
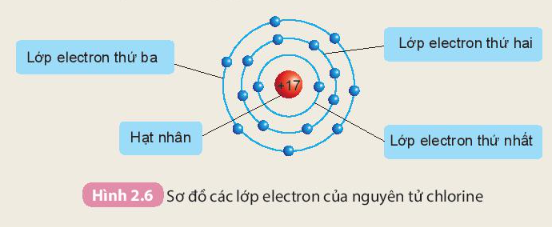
Nguyên tử chlorine có 17 electron
- Các electron sắp xếp thành từng lớp theo thứ tự từ trong ra ngoài cho đến hết:
+ Lớp electron thứ nhất ở trong cùng, gần hạt nhân nhất có 2 electron.
+ Lớp electron thứ hai ở bên ngoài lớp thứ nhất có 8 electron.
+ Lớp electron thứ ba ở ngoài cùng có 7 electron.
Kết luận:
- Nguyên tử là hạt vô cùng nhỏ tạo nên các chất.
- Nguyên tử gồm hạt nhân mang điện tích dương và vỏ nguyên tử mang điện tích âm.
- Nguyên tử trung hòa và điện nên tổng số hạt proton bằng tổng số hạt electron.
IV. Khối lượng nguyên tử
- Khối lượng nguyên tử bằng tổng khối lượng của các hạt proton, neutron trong hạt nhân và các hạt electron ở vỏ nguyên tử.
- Khối lượng nguyên tử vô cùng nhỏ, để thuận tiện cho việc sử dụng, người ta dùng đơn vị khối lượng nguyên tử, viết tắt là amu.
- Khối lượng 1 proton ≈ khối lượng 1 neutron ≈ 1 amu.
Khối lượng 1 electron ≈ 0,00055 amu nhỏ hơn rất nhiều so với khối lượng của proton và neutron.
⇒ Coi khối lượng hạt nhân nguyên tử là khối lượng của nguyên tử.
Ví dụ: Nguyên tử đồng có 29 proton, 29 electron, 35 neutron
Coi khối lượng hạt nhân nguyên tử là khối lượng của nguyên tử.
⇒ Khối lượng của nguyên tử đồng là 29.1amu + 35.1 amu = 64 amu
Xem thêm tóm tắt lý thuyết Khoa học tự nhiên 7 sách Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 3: Nguyên tố hóa học
Lý thuyết Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Lý thuyết Bài 5: Phân tử - Đơn chất - Hợp chất
Xem thêm các chương trình khác:
- Giải sgk Toán 7 – Kết nối tri thức
- Giải sbt Toán 7 – Kết nối tri thức
- Lý thuyết Toán 7 – Kết nối tri thức
- Giải VTH Toán 7 – Kết nối tri thức
- Chuyên đề dạy thêm Toán 7 cả 3 sách (2024 có đáp án)
- Giải sgk Lịch sử 7 – Kết nối tri thức
- Lý thuyết Lịch Sử 7 – Kết nối tri thức
- Giải sbt Lịch sử 7 – Kết nối tri thức
- Giải VTH Lịch sử 7 – Kết nối tri thức
- Soạn văn lớp 7 (hay nhất) – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn lớp 7 – Kết nối tri thức
- Soạn văn lớp 7 (ngắn nhất) – Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn lớp 7 – Kết nối tri thức
- Bố cục tác phẩm Ngữ văn lớp 7 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn lớp 7 – Kết nối tri thức
- Văn mẫu lớp 7 – Kết nối tri thức
- Giải VTH Ngữ văn lớp 7 – Kết nối tri thức
- Giải sgk Địa Lí 7 – Kết nối tri thức
- Lý thuyết Địa Lí 7 – Kết nối tri thức
- Giải sbt Địa lí 7 – Kết nối tri thức
- Giải VTH Địa lí 7 – Kết nối tri thức
- Giải sgk Tiếng Anh 7 Global Success – Kết nối tri thức
- Giải sbt Tiếng Anh 7 Global Success - Kết nối tri thức
- Bài tập Tiếng Anh 7 Global success theo Unit có đáp án
- Trọn bộ Từ vựng Tiếng Anh 7 Global success đầy đủ nhất
- Ngữ pháp Tiếng Anh 7 Global success
- Giải sgk Giáo dục công dân 7 – Kết nối tri thức
- Lý thuyết GDCD 7 – Kết nối tri thức
- Giải sbt Giáo dục công dân 7 – Kết nối tri thức
- Giải vth Giáo dục công dân 7 – Kết nối tri thức
- Giải sbt Hoạt động trải nghiệm lớp 7 - KNTT
- Giải sgk Hoạt động trải nghiệm 7 - KNTT
- Giải sgk Công nghệ 7 – Kết nối tri thức
- Lý thuyết Công nghệ 7 – Kết nối tri thức
- Giải sbt Công nghệ 7 – Kết nối tri thức
- Giải VTH Công nghệ 7 – KNTT
- Giải sgk Tin học 7 – Kết nối tri thức
- Lý thuyết Tin học 7 – Kết nối tri thức
- Giải sbt Tin học 7 – Kết nối tri thức
- Giải VTH Tin học 7 – Kết nối tri thức
- Giải sgk Giáo dục thể chất 7 – Kết nối tri thức
- Giải sgk Âm nhạc 7 – Kết nối tri thức
