Giáo án điện tử Lớp, phân lớp electron | Bài giảng PPT Hóa 10 Cánh diều
Với Giáo án PPT Lớp, phân lớp electron Hóa 10 sách Cánh diều sẽ giúp thầy cô dễ dàng biên soạn và giảng dạy bằng giáo án điện tử hay POWERPOINT Lớp, phân lớp electron.
Chỉ 400k mua trọn bộ Giáo án Hóa 10 Cánh diều bản PPT (cả năm) đẹp mắt (Chỉ 40k cho 1 bài giảng bất kì):
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận giáo án.
Xem thử tài liệu tại đây: Link tài liệu




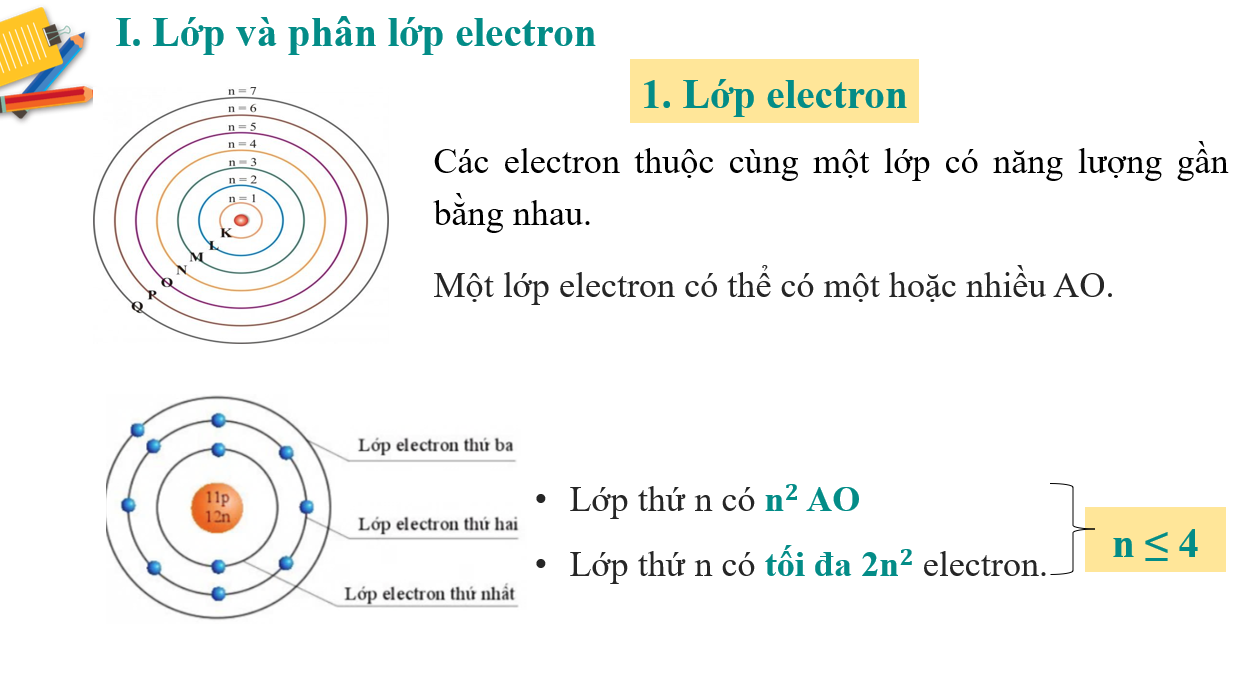
Tài liệu có 33 trang, trên đây trình bày tóm tắt 5 trang của Giáo án POWERPOINT Lớp, phân lớp electron Hóa 10 Cánh diều.
Giáo án Hóa 10 Bài 5 (Cánh diều): Lớp, phân lớp và cấu hình electron (3 tiết)
I. MỤC TIÊU
1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm lớp, phân lớp electron và mối quan hệ về số lượng phân lớp trong một lớp. Liên hệ được về số lượng AO trong một phân lớp, trong một lớp.
- Viết được cấu hình electron nguyên tử theo lớp, phân lớp electron và theo ô orbital khi biết số hiệu nguyên tử Z của 20 nguyên tố đầu tiên trong bảng tuần hoàn.
- Dựa vào đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, dự đoán được tính chất hóa học cơ bản (kim loại hay phi kim) của nguyên tố tương ứng.
2) Năng lực
a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/ nhóm, trách nhiệm của bản thân, đề xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học:
+ Trình bày được khái niệm lớp, phân lớp electron và mối quan hệ về số lượng phân lớp trong một lớp. Liên hệ được về số lượng AO trong một phân lớp, trong một lớp.
+ Viết được cấu hình electron nguyên tử theo lớp, phân lớp electron và theo ô orbital khi biết số hiệu nguyên tử Z của 20 nguyên tố đầu tiên trong bảng tuần hoàn.
+ Dựa vào đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, dự đoán được tính chất hóa học cơ bản (kim loại hay phi kim) của nguyên tố tương ứng.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: Thông qua hoạt động khai thác vốn kiến thức, kĩ năng đã học và thảo luận nội dung mới trong SGK, HS khám phá và thu nhận được kiến thức mới về lớp, phân lớp, cấu hình electron.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên.
3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Giáo viên: Sưu tầm hình ảnh có nội dung liên quan đến bài học, thiết kế phiếu học tập.
- Học sinh: Đọc lại các kiến thức có liên quan về cấu tạo nguyên tử.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: HS hoạt động cá nhân, xác định nhiệm vụ học tập: Nhận biết sự phân bố electron vào các lớp và thứ tự phân bố electron vào lớp vỏ nguyên tử.
c) Sản phẩm: Câu trả lời của HS.
d) Tổ chức thực hiện:
- GV sử dụng hình 5.1 trong SGK hoặc có thể sử dụng kết quả của bài học trước, yêu cầu HS trả lời các câu hỏi:
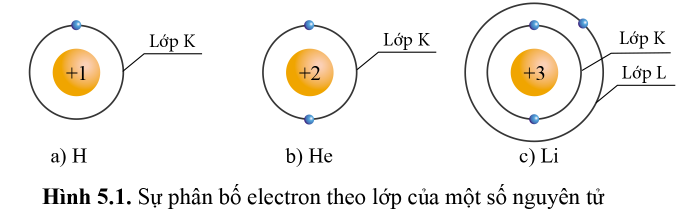
(1) Số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là bao nhiêu?
(2) Thứ tự phân bố electron vào lớp vỏ nguyên tử như thế nào?
(3) Số electron tối đa trong mỗi lớp là bao nhiêu?
Đáp án:
(1) Số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là 2.
(2) Thứ tự phân bố electron vào lớp vỏ nguyên tử: Các electron sẽ được phân bố lần lượt vào các lớp theo chiều từ gần hạt nhân ra ngoài.
(3) Mỗi lớp có số electron đối đa xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ 2 có tối đa 8 electron,…
- GV gọi một số HS trả lời, sau đó nhận xét và bổ sung kiến thức cần thiết. GV đặt vấn đề để HS nhận thấy ở lớp vỏ nguyên tử ngoài khái niệm lớp electron còn xuất hiện khái niệm phân lớp electron.
………………………………………….
………………………………………….
………………………………………….
Giáo án Hóa 10 Bài 5 (Cánh diều): Lớp, phân lớp và cấu hình electron (3 tiết)
I. MỤC TIÊU
1) Kiến thức
Học xong bài này, học sinh có thể:
- Trình bày được khái niệm lớp, phân lớp electron và mối quan hệ về số lượng phân lớp trong một lớp. Liên hệ được về số lượng AO trong một phân lớp, trong một lớp.
- Viết được cấu hình electron nguyên tử theo lớp, phân lớp electron và theo ô orbital khi biết số hiệu nguyên tử Z của 20 nguyên tố đầu tiên trong bảng tuần hoàn.
- Dựa vào đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, dự đoán được tính chất hóa học cơ bản (kim loại hay phi kim) của nguyên tố tương ứng.
2) Năng lực
a) Năng lực chung
- Năng lực tự chủ và tự học: học sinh xác định đúng đắn động cơ, thái độ học tập, tự đánh giá và điều chỉnh được kế hoạch học tập; tự nhận ra được những sai sót và khắc phục.
- Năng lực giao tiếp: tiếp thu kiến thức, trao đổi học hỏi bạn bè thông qua việc thực hiện nhiệm vụ các hoạt động cặp đôi, nhóm; có thái độ tôn trọng, lắng nghe, có phản ứng tích cực trong giao tiếp.
- Năng lực hợp tác: học sinh xác định được nhiệm vụ của tổ/ nhóm, trách nhiệm của bản thân, đề xuất được những ý kiến đóng góp, góp phần hoàn thành nhiệm vụ học tập.
b) Năng lực chuyên biệt
- Năng lực nhận thức hóa học:
+ Trình bày được khái niệm lớp, phân lớp electron và mối quan hệ về số lượng phân lớp trong một lớp. Liên hệ được về số lượng AO trong một phân lớp, trong một lớp.
+ Viết được cấu hình electron nguyên tử theo lớp, phân lớp electron và theo ô orbital khi biết số hiệu nguyên tử Z của 20 nguyên tố đầu tiên trong bảng tuần hoàn.
+ Dựa vào đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, dự đoán được tính chất hóa học cơ bản (kim loại hay phi kim) của nguyên tố tương ứng.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học: Thông qua hoạt động khai thác vốn kiến thức, kĩ năng đã học và thảo luận nội dung mới trong SGK, HS khám phá và thu nhận được kiến thức mới về lớp, phân lớp, cấu hình electron.
- Năng lực vận dụng kiến thức, kỹ năng đã học: giải thích được các hiện tượng hóa học xảy ra trong tự nhiên.
3) Phẩm chất
- Yêu nước: nhận biết được vẻ đẹp của tự nhiên, của đất nước thông qua bộ môn Hóa học.
- Trách nhiệm: nghiêm túc thực hiện các nhiệm vụ học tập được giao đúng tiến độ.
- Trung thực: thành thật trong việc thu thập các tài liệu, viết báo cáo và các bài tập.
- Chăm chỉ: tích cực trong các hoạt động cá nhân, tập thể.
- Nhân ái: quan tâm, giúp đỡ, chia sẻ những khó khăn trong việc thực hiện nhiệm vụ học tập.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Giáo viên: Sưu tầm hình ảnh có nội dung liên quan đến bài học, thiết kế phiếu học tập.
- Học sinh: Đọc lại các kiến thức có liên quan về cấu tạo nguyên tử.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG
a) Mục tiêu: Tạo tình huống có vấn đề và tâm lý hứng thú cho HS khi bắt đầu bài học mới.
b) Nội dung: HS hoạt động cá nhân, xác định nhiệm vụ học tập: Nhận biết sự phân bố electron vào các lớp và thứ tự phân bố electron vào lớp vỏ nguyên tử.
c) Sản phẩm: Câu trả lời của HS.
d) Tổ chức thực hiện:
- GV sử dụng hình 5.1 trong SGK hoặc có thể sử dụng kết quả của bài học trước, yêu cầu HS trả lời các câu hỏi:

(1) Số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là bao nhiêu?
(2) Thứ tự phân bố electron vào lớp vỏ nguyên tử như thế nào?
(3) Số electron tối đa trong mỗi lớp là bao nhiêu?
Đáp án:
(1) Số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z ≥ 2 là 2.
(2) Thứ tự phân bố electron vào lớp vỏ nguyên tử: Các electron sẽ được phân bố lần lượt vào các lớp theo chiều từ gần hạt nhân ra ngoài.
(3) Mỗi lớp có số electron đối đa xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ 2 có tối đa 8 electron,…
- GV gọi một số HS trả lời, sau đó nhận xét và bổ sung kiến thức cần thiết. GV đặt vấn đề để HS nhận thấy ở lớp vỏ nguyên tử ngoài khái niệm lớp electron còn xuất hiện khái niệm phân lớp electron.
………………………………………….
………………………………………….
………………………………………….
Xem thêm các chương trình khác:
- Giáo án Toán 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Hóa 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Vật lí 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Sinh học 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Lịch sử 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Địa lí 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Tin học 10 Kết nối tri thức năm 2023 (mới nhất)
- Giáo án Kinh tế pháp luật 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Chuyên đề KTPL 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Công nghệ 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án Tiếng Anh 10 Global Success năm 2024 (mới nhất)
- Giáo án Giáo dục quốc phòng 10 Kết nối tri thức năm 2024 (mới nhất)
- Giáo án PPT Tiếng Anh 10 Global success
- Giáo án PPT Toán 10 Kết nối tri thức
- Giáo án PPT Vật lí 10 Kết nối tri thức
- Giáo án PPT Hóa 10 Kết nối tri thức
- Giáo án Ngữ Văn 10 Kết nối tri thức (mới nhất)
- Giáo án Toán 10 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Hóa 10 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Vật lí 10 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Sinh học 10 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Lịch sử 10 Chân trời sáng tạo năm 2024 (mới nhất)
- Giáo án Tiếng Anh 10 Friends Global năm 2024 (mới nhất)
- Giáo án Ngữ Văn 10 Chân trời sáng tạo (mới nhất)
