Giải KHTN 9 Bài 19 (Kết nối tri thức): Dãy hoạt động hoá học
Với giải bài tập Khoa học tự nhiên 9 Bài 19: Dãy hoạt động hoá học sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập KHTN 9 Bài 19.
Giải KHTN 9 Bài 19: Dãy hoạt động hoá học
Trả lời:
Nhận thấy:
Khả năng tham gia phản ứng hoá học của các kim loại khác nhau là khác nhau.
Khả năng phản ứng của các kim loại giảm dần theo thứ tự: sắt, đồng, bạc, vàng …
I. Xây dựng dãy hoạt động hoá học
Hoạt động trang 92, 93 KHTN 9: Sắp xếp mức độ hoạt động hoá học của: Na, Fe, H, Cu, Ag
1. Khảo sát phản ứng của các kim loại Na, Fe, Cu với nước
(Phản ứng của kim loại natri với nước xem Hình 18.5, Bài 18).
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
Dựa vào khả năng phản ứng với nước, có thể chia các kim loại natri, đồng và sắt thành mấy nhóm? So sánh mức độ hoạt động hoá học của các nhóm kim loại này.
2. Khảo sát phản ứng của kim loại Fe, Cu với dung dịch acid
Chuẩn bị: đinh sắt, dây đồng, hai ống nghiệm đựng cùng một lượng dung dịch HCl cùng nồng độ.
Tiến hành: Cho đinh sắt, dây đồng vào từng ống nghiệm riêng biệt đựng dung dịch HCl.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
a) Hãy cho biết kim loại nào phản ứng được với dung dịch HCl (đẩy được hydrogen ra khỏi acid).
b) So sánh mức độ hoạt động hoá học của sắt, đồng với hydrogen.
c) So sánh mức độ hoạt động hoá học của sắt với đồng.
3. So sánh mức độ hoạt động hoá học của kim loại Ag và Cu
Chuẩn bị: dây đồng, dung dịch AgNO3 2%; ống nghiệm, panh.
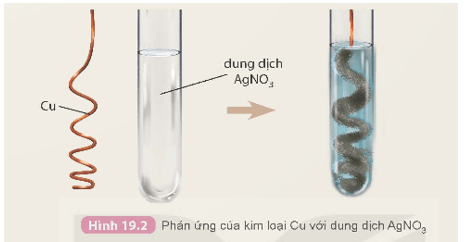
Tiến hành: Dùng panh kẹp dây đồng đã được uốn thành hình lò xo đưa vào ống nghiệm chứa dung dịch AgNO3 2%.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
a) Mô tả hiện tượng và viết phương trình hoá học của phản ứng xảy ra.
b) So sánh mức độ hoạt động của kim loại đồng và bạc. Giải thích.
c) Qua ba thí nghiệm ở trên, hãy sắp xếp mức độ hoạt động hoá học của các kim loại Na, Fe, Cu, Ag và H thành dãy theo chiều giảm dần.
Trả lời:
1. Khảo sát phản ứng của các kim loại Na, Fe, Cu với nước
Dựa vào khả năng phản ứng với nước, có thể chia các kim loại natri, đồng và sắt thành hai nhóm:
+ Nhóm 1: Phản ứng được với nước ở điều kiện thường: natri.
+ Nhóm 2: Không phản ứng được với nước ở điều kiện thường: đồng và sắt.
So sánh: Mức độ hoạt động hoá học của nhóm 1 mạnh hơn nhóm 2.
2. Khảo sát phản ứng của kim loại Fe, Cu với dung dịch acid
a) Kim loại Fe phản ứng được với dung dịch HCl (đẩy được hydrogen ra khỏi acid).
b) Mức độ hoạt động của sắt mạnh hơn hydrogen; mức độ hoạt động của đồng yếu hơn hydrogen.
c) Mức độ hoạt động hoá học của sắt mạnh hơn đồng.
3. So sánh mức độ hoạt động hoá học của kim loại Ag và Cu
a) Hiện tượng:
- Có lớp kim loại trắng bạc bám ngoài dây đồng.
- Dung dịch chuyển dần từ không màu sang màu xanh.
Phương trình hoá học:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
b) Mức độ hoá học của đồng mạnh hơn bạc. Do đồng đẩy được bạc ra khỏi muối.
c) Mức độ hoạt động hoá học của các kim loại và H giảm dần theo thứ tự:
Na, Fe, H, Cu, Ag.
II. Ý nghĩa dãy hoạt động hoá học
Hoạt động trang 93 KHTN 9: Tìm hiểu về ý nghĩa dãy hoạt động hoá học
Trình bày về ý nghĩa dãy hoạt động hoá học theo gợi ý sau:
2. Kim loại đứng trước H phản ứng với dung dịch acid (H2SO4 loãng, HCl, …) tạo thành sản phẩm gì?
3. Nêu khái quát về vị trí trong dãy hoạt động của:
- Kim loại hoạt động hoá học mạnh;
- Kim loại hoạt động hoá học trung bình;
- Kim loại hoạt động hoá học yếu.
Trả lời:
1. Kim loại hoạt động hoá học mạnh như K, Na, Ca phản ứng với nước ở điều kiện thường tạo thành hydroxide và khí hydrogen.
2. Kim loại đứng trước H phản ứng với dung dịch acid (H2SO4 loãng, HCl, …) tạo thành muối và khí hydrogen.
3. Khái quát vị trí:
- Kim loại hoạt động hoá học mạnh đứng đầu dãy hoạt động hoá học của kim loại (bao gồm từ K đến Al).
- Kim loại hoạt động hoá học trung bình đứng giữa dãy hoạt động hoá học của kim loại (bao gồm từ sau Al đến trước H);
- Kim loại hoạt động hoá học yếu đứng sau H (đứng cuối) trong dãy hoạt động hoá học của kim loại.
2. Cho viên kẽm vào ống nghiệm chứa dung dịch AgNO3.
3. Rót vào ba cốc thuỷ tinh loại 100 mL, mỗi cốc 25 mL nước cất. Cho vào mỗi cốc một mẩu kim loại trong số ba kim loại sau: Cu, Fe, Ca.
Trả lời:
Dự đoán:
1. Thí nghiệm 1:
Hiện tượng:
- Ống nghiệm chứa Mg và ống nghiệm chứa Zn có sủi bọt khí, kim loại trong ống nghiệm tan dần.
- Ống nghiệm chứa Ag không có hiện tượng gì.
Phương trình hoá học:
Mg + H2SO4 loãng → MgSO4 + H2
Zn + H2SO4 loãng → ZnSO4 + H2
Ag + H2SO4 loãng → không phản ứng
2. Thí nghiệm 2:
- Hiện tượng: Viên kẽm tan dần, có lớp kim loại trắng sáng bám ngoài viên kẽm.
- Phương trình hoá học:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
3. Thí nghiệm 3:
- Hiện tượng:
+ Chỉ có cốc cho Ca có phản ứng hoá học xảy ra. Ca tan dần, có khí thoát ra.
+ Hai cốc còn lại không có hiện tượng gì xuất hiện.
- Phương trình hoá học:
Ca + 2H2O → Ca(OH)2 + H2
Trả lời:
- Các kim loại hoạt động mạnh như K, Na, Ca, … tác dụng với nước ở điều kiện thường, giải phóng khí hydrogen.
- Kim loại đứng trước H có thể tác dụng với dung dịch acid, giải phóng khí hydrogen.
- Kim loại đứng trước (trừ K, Na, Ca, …) có thể đẩy kim loại đứng sau ra khỏi dung dịch muối.
Xem thêm lời giải bài tập Khoa học tự nhiên lớp 9 Kết nối tri thức hay, chi tiết khác:
Bài 20: Tách kim loại và việc sử dụng hợp kim
Bài 21: Sự khác nhau cơ bản giữa phi kim và kim loại
Xem thêm các chương trình khác:
- Soạn văn 9 Kết nối tri thức (hay nhất)
- Văn mẫu 9 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 9 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 9 - Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 9 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn 9 – Kết nối tri thức
- Soạn văn 9 Kết nối tri thức (ngắn nhất)
- Giải sgk Toán 9 – Kết nối tri thức
- Lý thuyết Toán 9 – Kết nối tri thức
- Giải sbt Toán 9 – Kết nối tri thức
- Bài tập Tiếng Anh 9 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 9 - Global success
- Trọn bộ Từ vựng Tiếng Anh 9 Global success đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh 9 Global success đầy đủ nhất
- Giải sbt Tiếng Anh 9 – Global Success
- Giải sgk Lịch sử 9 – Kết nối tri thức
- Giải sbt Lịch sử 9 – Kết nối tri thức
- Giải sgk Địa lí 9 – Kết nối tri thức
- Giải sbt Địa lí 9 – Kết nối tri thức
- Giải sgk Tin học 9 – Kết nối tri thức
- Giải sbt Tin học 9 – Kết nối tri thức
- Giải sgk Công nghệ 9 – Kết nối tri thức
- Giải sgk Giáo dục công dân 9 – Kết nối tri thức
- Giải sbt Giáo dục công dân 9 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 9 – Kết nối tri thức