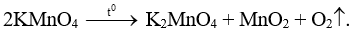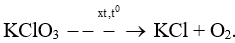Sách bài tập KHTN 8 Bài 5 (Cánh diều): Tính theo phương trình hóa học
Với giải sách bài tập Khoa học tự nhiên 8 Bài 5: Tính theo phương trình hóa học sách Cánh diều hay nhất, ngắn gọn sẽ giúp học sinh dễ dàng làm bài tập trong SBT KHTN 8 Bài 5.
Giải SBT KHTN 8 Bài 5: Tính theo phương trình hóa học
A. 0,68 gam. B. 0,64 gam. C. 0,16 gam. D. 0,32 gam.
Lời giải:
Đáp án đúng là: D
Phương trình hóa học: 4P + 5O2 2P2O5
Theo đề bài:
Theo phương trình hóa học: Cứ 4 mol P phản ứng với 5 mol O2,
Do đó 0,04 mol P phản ứng với 0,05 mol O2.
Vậy số mol O2 còn dư là 0,06 – 0,05 = 0,01 (mol).
Khối lượng O2 dư là 0,01 ´ 32 = 0,32 (gam)
A. 2,2400 lít. B. 2,4790 lít. C. 1,2395 lít. D. 4,5980 lít.
Lời giải:
Đáp án đúng là: C
Phương trình hoá học: Mg + 2HCl → MgCl2 + H2
Theo bài ra:
Theo phương trình hoá học, cứ 1 mol Mg phản ứng với 2 mol HCl;
Do đó cứ 0,2 mol Mg phản ứng với 0,4 mol HCl.
Vậy Mg dư, HCl hết, số mol khí tính theo HCl.
Đem nhiệt phân hoàn toàn 7,9 gam potassium permanganate thu được khối lượng khí O2 là
A. 0,2 gam. B. 1,6 gam. C. 0,4 gam. D. 0,8 gam.
Lời giải:
Đáp án đúng là: D
Theo phương trình hoá học cứ 2 mol KMnO4 phản ứng sinh ra 1 mol O2.
Vậy cứ 0,05 mol KMnO4 phản ứng sinh ra 0,025 mol O2.
Khối lượng khí O2 là: 0,25 × 32 = 0,8 gam.
a) Hoàn thành phương trình hóa học của phản ứng trên.
A. 54,73%. B. 60,00%. C. 90,00%. D. 70,00%.
Lời giải:
a) 2KClO3 2KCl + 3O2.
b) Đáp án đúng là: B
Theo phương trình hoá học cứ 2 mol KClO3 phản ứng thu được 3 mol O2.
Vậy 0,3 mol KClO3 phản ứng thu được 0,45 mol O2.
Hiệu suất phản ứng là:
A. 21,6 và 40,8. B. 91,8 và 12,15. C. 40,8 và 21,6. D. 12,15 và 91,8.
Lời giải:
Đáp án đúng là: A
Phương trình hoá học: 4Al + 3O2 2Al2O3
Theo phương trình hoá học cứ 3 mol O2 phản ứng hết với 4 mol Al.
Vậy 0,6 mol O2 phản ứng hết với 0,8 mol Al.
Giá trị của a = mAl = 0,8.27 = 21,6 gam.
Áp dụng định luật bảo toàn khối lượng có b = 21,6 + 19,2 = 40,8 gam.
C + O2 CO2↑.
Biết khối lượng than đá đem đốt là 30 gam, thể tích khí CO2 đo được (ở đkc) là 49,58 lít. Thành phần phần trăm về khối lượng của carbon trong than đá là
A. 40,00%. B. 66,9%. C. 80,0%. D. 6,7%.
Lời giải:
Đáp án đúng là: C
C + O2CO2
Theo đề bài:
Theo phương trình hóa học:
=> mC = 2 X 12 = 24 (gam).
=> %mC =
CaCO3 CaO + CO2↑
Tính khối lượng CaO thu được khi nung 1 tấn CaCO3 nếu hiệu suất phản ứng là
a) 100%. b) 90%.
Lời giải:
CaCO3 CaO + CO2
a) Theo phương trình hóa học:
nCaO = 10000 mol => mCaO = 10000 ´ 56 = 560 000 (gam).
b) Do hiệu suất phản ứng là 90%:
=> mCaO = 9 000 × 56 = 504 000 gam.
2Al2O3 4Al + 3O2↑.
Một loại quặng boxide có chứa 85% là Al2O3. Hãy tính khối lượng nhôm được tạo thành từ 2 tấn quặng boxide, biết hiệu suất của quá trình sản xuất là 90%.
Lời giải:
Trong 2 tấn quặng có: tấn.
Theo phương trình hóa học:
Do hiệu suất chỉ đạt 90% nên khối lượng nhôm thu được trong thực tế là:
Xem thêm lời giải Sách bài tập Khoa học tự nhiên 8 sách Cánh diều hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 8 Cánh diều (hay nhất)
- Văn mẫu lớp 8 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 8 – Cánh diều
- Bố cục tác phẩm Ngữ văn lớp 8 – Cánh diều
- Tác giả tác phẩm Ngữ văn lớp 8 - Cánh diều
- Giải SBT Ngữ văn 8 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 8 – Cánh diều
- Soạn văn 8 Cánh diều (ngắn nhất)
- Giải sgk Toán 8 – Cánh diều
- Lý thuyết Toán 8 – Cánh diều
- Giải sbt Toán 8 – Cánh diều
- Giải sgk Tiếng Anh 8 – iLearn Smart World
- Giải sbt Tiếng Anh 8 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 8 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 8 ilearn Smart World
- Bài tập Tiếng Anh 8 iLearn Smart World theo Unit có đáp án
- Giải sgk Lịch sử 8 – Cánh diều
- Lý thuyết Lịch sử 8 - Cánh diều
- Giải sbt Lịch sử 8 – Cánh diều
- Giải sgk Địa lí 8 – Cánh diều
- Lý thuyết Địa lí 8 - Cánh diều
- Giải sbt Địa lí 8 – Cánh diều
- Giải sgk Giáo dục công dân 8 – Cánh diều
- Lý thuyết Giáo dục công dân 8 – Cánh diều
- Giải sbt Giáo dục công dân 8 – Cánh diều
- Giải sgk Công nghệ 8 – Cánh diều
- Lý thuyết Công nghệ 8 - Cánh diều
- Giải sbt Công nghệ 8 – Cánh diều
- Giải sgk Tin học 8 – Cánh diều
- Lý thuyết Tin học 8 - Cánh diều
- Giải sbt Tin học 8 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 8 – Cánh diều