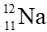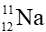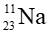Lý thuyết Nguyên tố hóa học – Hóa 10 Chân trời sáng tạo
Tóm tắt lý thuyết Hóa học lớp 10 Bài 3: Nguyên tố hóa học ngắn gọn, chi tiết sách Chân trời sáng tạo với cuộc sống sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Hóa học 10.
Lý thuyết Hóa học 10 Bài 3: Nguyên tố hóa học
Bài giảng Hóa học 10 Bài 3: Nguyên tố hóa học
A. Lý thuyết Nguyên tố hóa học
1. Hạt nhân nguyên tử
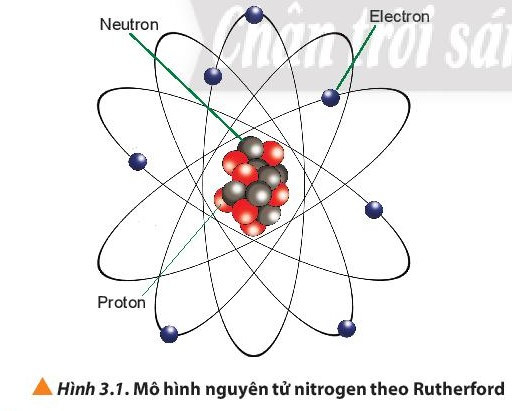
- Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E).
- Điện tích hạt nhân = + Z.
- Số khối (A) = số proton (P) + số neutron (N)
Ví dụ: Nguyên tử aluminium (Al) có 13 proton, 14 neutron. Suy ra:
+ Nguyên tử aluminium có số đơn vị điện tích hạt nhân = số proton = số electron = 13.
+ Điện tích hạt nhân nguyên tử aluminium là +13.
+ Số khối A = số proton (P) + số neutron (N) = 13 + 14 = 27.
II. Nguyên tố hóa học
1. Số hiệu nguyên tử
- Số đơn vị điện tích hạt nhân nguyên tử của một nguyên tố được gọi là số hiệu nguyên tử (Z) của nguyên tố đó.
- Mỗi nguyên tố hóa học có một số hiệu nguyên tử.
- Số hiệu nguyên tử (kí hiệu là Z) cho biết:
+ Số proton trong hạt nhân nguyên tử.
+ Số electron trong nguyên tử.
Ví dụ: Nguyên tố carbon có số hiệu nguyên tử là 6. Suy ra:
+ Số proton trong hạt nhân nguyên tử carbon = 6
+ Số electron trong nguyên tử carbon = 6
2. Nguyên tố hóa học
- Nguyên tố hóa học là tập hợp những nguyên tử có cùng điện tích hạt nhân.
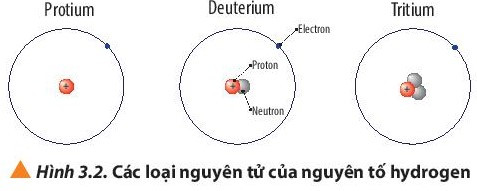
Ví dụ: Protium; deuterium và tritium là các loại nguyên tử của nguyên tố hydrogen.
3. Kí hiệu nguyên tử
- Số đơn vị điện tích hạt nhân nguyên tử (số hiệu nguyên tử) của một nguyên tố hóa học và số khối được xem là những đặc trưng cơ bản của nguyên tử.
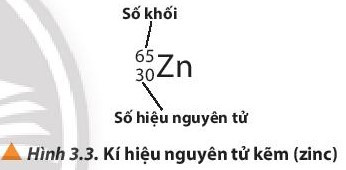
- Để kí hiệu nguyên tử, người ta thường ghi các chỉ số đặc trưng ở bên trái kí hiệu nguyên tố với số khối A ở phía trên, số hiệu nguyên tử Z ở phía dưới.

Ví dụ:
III. Đồng vị
- Các đồng vị của một nguyên tố hóa học là những nguyên tử có cùng số proton (P), cùng số hiệu nguyên tử (Z), nhưng khác nhau về số neutron (N). Do đó, số khối (A) của chúng khác nhau.
- Ví dụ: Potassium (K) có 3 đồng vị là: K3919; K4019; K4119
- Trong tự nhiên, hầu hết các nguyên tố được tìm thấy dưới dạng hỗn hợp của các đồng vị.
- Ngoài các đồng vị bền, các nguyên tố hóa học còn có một số đồng vị không bền, gọi là các đồng vị phóng xạ, được sử dụng nhiều trong đời sống, y học, nghiên cứu khoa học…
IV. Nguyên tử khối và nguyên tử khối trung bình
1. Nguyên tử khối
- Nguyên tử khối là khối lượng tương đối của nguyên tử.
- Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử (1 amu).
- Một cách gần đúng, coi nguyên tử khối có giá trị bằng số khối.
Ví dụ: Nguyên tử của nguyên tố magnesium (Mg) có 12 proton và 12 neutron.
⇒ Nguyên tử khối của Mg = 12 + 12 = 24 amu
2. Nguyên tử khối trung bình
- Mỗi nguyên tố thường có nhiều đồng vị, do đó trong thực tế người ta thường sử dụng giá trị nguyên tử khối trung bình.
- Muốn xác định giá trị nguyên tử khối trung bình của một nguyên tố, ta cần phải biết được phần trăm số nguyên tử các đồng vị của nguyên tố đó trong tự nhiên. Người ta thường dùng phương pháp phổ khối lượng để xác định phần trăm số nguyên tử các đồng vị tự nhiên của các nguyên tố.
- Công thức tính nguyên tử khối trung bình của nguyên tố X: ¯AX=a1×A1+a2×A2+...+ai×Ai100
Trong đó:
¯AX: là nguyên tử khối trung bình của X
Ai: là nguyên tử khối đồng vị thứ i
ai: là tỉ lệ % số nguyên tử đồng vị thứ i
Ví dụ:
Trong tự nhiên, nguyên tố copper có hai đồng vị với phần trăm số nguyên tử tương ứng là Cu6329 (69,15%) và Cu6529 (30,85%). Nguyên tử khối trung bình của nguyên tố copper là:
¯ACu=63.69,15+65.30,85100=63,617
B. Trắc nghiệm Nguyên tố hóa học
Câu 1. Nguyên tử aluminium có 13 electron. Điện tích hạt nhân của nguyên tử này là
A. 13
B. 27
C. + 13
D. + 27
Đáp án đúng là: C
Số đơn vị điện tích hạt nhân (Z) = số electron (E) = 13.
Điện tích hạt nhân = + Z = + 13.
Câu 2. Công thức tính số khối (A) là
A. Số khối (A) = số proton (P) + số electron (E)
B. Số khối (A) = số neutron (N) + số electron (E)
C. Số khối (A) = số proton (P) × 2
D. Số khối (A) = số proton (P) + số neutron (N)
Đáp án đúng là: D
Số khối (A) = số proton (P) + số neutron (N).
Câu 3. Nguyên tử potassium (K) có 19 electron; 19 proton và 20 neutron. Số khối nguyên tử của K là
A. 20
B. 19
C. 39
D. 58
Đáp án đúng là: C
Số khối A = số proton + số neutron = 19 + 20 = 39.
Câu 4. Số hiệu nguyên tử của một nguyên tố là
A. điện tích hạt nhân nguyên tử của nguyên tố đó
B. số đơn vị điện tích hạt nhân nguyên tử của nguyên tố đó
C. tổng số proton và neutron trong nguyên tử của nguyên tố đó
D. tổng số proton và electron trong nguyên tử của nguyên tố đó
Đáp án đúng là: B
Số hiệu nguyên tử của một nguyên tố (Z) là số đơn vị điện tích hạt nhân nguyên tử của nguyên tố đó.
Câu 5. Khẳng định đúng là
A. Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E)
B. Số đơn vị điện tích hạt nhân (+Z) = số proton (P) = số electron (E)
C. Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số neutron (N)
D. Số đơn vị điện tích hạt nhân (Z) = số neutron (N) = số electron (E)
Đáp án đúng là: A
Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E).
Điện tích hạt nhân = + Z.
Câu 6. Nguyên tử nitơ (nitrogen) có 7 proton. Số đơn vị điện tích hạt nhân của nguyên tử này là
A. + 7
B. 7
C. + 14
D. 14
Đáp án đúng là: B
Số đơn vị điện tích hạt nhân (Z) = số proton (P) = 7.
Câu 7. Nguyên tố hóa học là
A. tập hợp các nguyên tử có cùng số hạt neutron;
B. tập hợp các nguyên tử có cùng điện tích hạt nhân;
C. tập hợp các nguyên tử có cùng số hạt neutron và proton;
D. tập hợp các nguyên tử có cùng số số khối A.
Đáp án đúng là: B
Nguyên tố hóa học là tập hợp các nguyên tử có cùng điện tích hạt nhân.
Câu 8. Kí hiệu nguyên tử 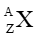
A. kí hiệu hóa học của nguyên tố (X);
B. số hiệu nguyên tử (Z);
C. số khối (A);
D. Cả A, B và C đều đúng.
Đáp án đúng là: D
Kí hiệu nguyên tử 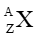
Câu 9. Một nguyên tử sodium (Na) có 11 electron; 11 proton và 12 neutron. Kí hiệu của nguyên tử này là
A.
B.
C.
D.
Đáp án đúng là: C
Một nguyên tử sodium (Na) có:
- Số hiệu nguyên tử Z = số đơn vị điện tích hạt nhân = số p = 11
- Số khối A = P + N = số p + số n = 11 + 12 = 23
Kí hiệu nguyên tử là 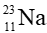
Câu 10. Cho kí hiệu nguyên tử 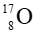
A. Kí hiệu hóa học của nguyên tố là O;
B. Số hiệu nguyên tử là 8;
C. Số proton trong một hạt nhân nguyên tử là 8;
D. Số neutron trong một hạt nhân nguyên tử là 8.
Đáp án đúng là: B
Kí hiệu nguyên tử 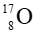
- Kí hiệu hóa học của nguyên tố là O;
- Số hiệu nguyên tử Z = 8 ⇒ số proton (P) là 8.
- Số khối A = 17 mà A = P + N ⇒ N = A – P = 17 – 8 = 9 ⇒ số neutron là 9.
Vậy khẳng định: Số neutron trong một hạt nhân nguyên tử là 8 là khẳng định sai.
Xem thêm tóm tắt lý thuyết Hóa học 10 sách Chân trời sáng tạo hay, chi tiết khác:
Lý thuyết Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Lý thuyết Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Lý thuyết Bài 7: Định luật tuần hoàn – ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Soạn văn lớp 10 (ngắn nhất) – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Giải sbt Ngữ văn lớp 10 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Văn mẫu lớp 10 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 10 – Chân trời sáng tạo
- Giải sgk Toán 10 – Chân trời sáng tạo
- Giải Chuyên đề Toán 10 – Chân trời sáng tạo
- Lý thuyết Toán 10 – Chân trời sáng tạo
- Giải sbt Toán 10 – Chân trời sáng tạo
- Chuyên đề dạy thêm Toán 10 Chân trời sáng tạo (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Giải sbt Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 10 Friends Global đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 Friends Global
- Giải sgk Vật lí 10 – Chân trời sáng tạo
- Giải sbt Vật lí 10 – Chân trời sáng tạo
- Lý thuyết Vật lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Vật lí 10 – Chân trời sáng tạo
- Giải sgk Sinh học 10 – Chân trời sáng tạo
- Giải sbt Sinh học 10 – Chân trời sáng tạo
- Lý thuyết Sinh học 10 – Chân trời sáng tạo
- Giải Chuyên đề Sinh học 10 – Chân trời sáng tạo
- Giải sgk Lịch sử 10 – Chân trời sáng tạo
- Giải sbt Lịch sử 10 – Chân trời sáng tạo
- Giải Chuyên đề Lịch sử 10 – Chân trời sáng tạo
- Lý thuyết Lịch sử 10 – Chân trời sáng tạo
- Giải sgk Địa lí 10 – Chân trời sáng tạo
- Lý thuyết Địa Lí 10 - Chân trời sáng tạo
- Giải sbt Địa lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Địa lí 10 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải Chuyên đề Kinh tế và pháp luật 10 – Chân trời sáng tạo
- Lý thuyết KTPL 10 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 10 – Chân trời sáng tạo