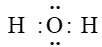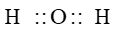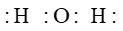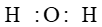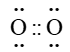Lý thuyết Liên kết cộng hóa trị – Hóa 10 Chân trời sáng tạo
Tóm tắt lý thuyết Hóa học lớp 10 Bài 10: Liên kết cộng hóa trị ngắn gọn, chi tiết sách Chân trời sáng tạo với cuộc sống sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Hóa học 10.
Lý thuyết Hóa học 10 Bài 10: Liên kết cộng hóa trị
Bài giảng Hóa học 10 Bài 10: Liên kết cộng hóa trị
A. Lý thuyết Liên kết cộng hóa trị
I. Sự hình thành liên kết cộng hóa trị
1. Sự hình thành liên kết cộng hóa trị
- Liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
- Liên kết cộng hóa trị được hình thành giữa các nguyên tử của cùng một nguyên tố hoặc giữa các nguyên tử của các nguyên tố không khác nhau nhiều về độ âm điện.
Ví dụ 1: Sự hình thành liên kết cộng hóa trị trong phân tử hydrogen chloride
+ Nguyên tử H có 1 electron ở lớp ngoài cùng, nguyên tử Cl có 7 electron ở lớp ngoài cùng. Để đạt được cấu hình electron của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử H và Cl cùng góp 1 electron để tạo nên 1 cặp electron chung cho cả 2 nguyên tử.
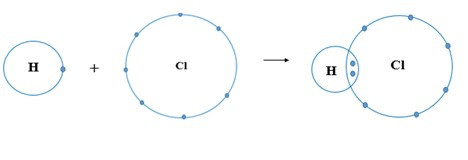
+ Cặp electron chung giữa 2 nguyên tử H và Cl được biểu diễn bằng 1 gạch nối “–”, đó là liên kết đơn. Do đó, liên kết trong phân tử HCl còn được biểu diễn là H – Cl.
Ví dụ 2: Sự hình thành liên kết cộng hóa trị trong phân tử oxygen (O2)
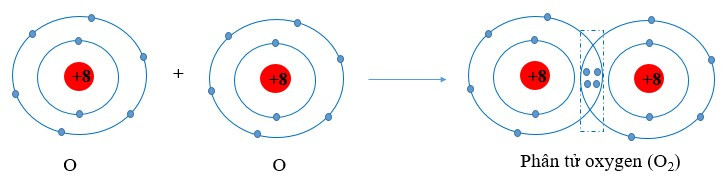
Nguyên tử oxygen (O) có cấu hình electron là 1s22s22p4. Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử O đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử O cùng góp 2 electron để tạo nên 2 cặp electron dùng chung cho cả hai nguyên tử.
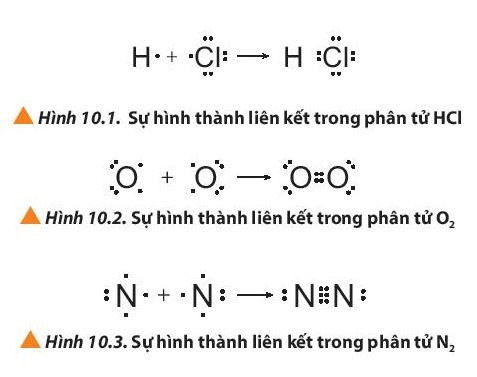
+ Giữa hai nguyên tử oxygen trong phân tử O2 có hai cặp electron chung, được biểu diễn bằng hai gạch nối “=”, đó là liên kết đôi. Do đó liên kết trong phân tử O2 được biểu diễn là O=O.
Ví dụ 3: Sự hình thành liên kết cộng hóa trị trong phân tử nitrogen.
+ Mỗi nguyên tử N có 5 electron ở lớp ngoài cùng. Để đạt được cấu hình electron của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 3 electron. Vì vậy, mỗi nguyên tử N cùng góp 3 electron để tạo nên 3 cặp electron chung cho cả 2 nguyên tử.
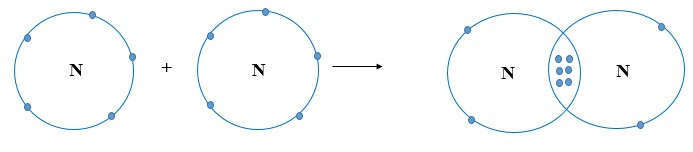

+ Ba cặp electron chung giữa 2 nguyên tử N được biểu diễn bằng ba gạch nối “≡”, đó là liên kết ba. Do đó, liên kết trong phân tử N2 còn được biểu diễn là N ≡ N.
Chú ý:
+ Các công thức H – Cl; O = O; N ≡ N gọi là công thức cấu tạo của HCl; O2; N2.
+ Liên kết đơn là liên kết được tạo bởi 1 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng một gạch nối “–”
+ Liên kết đôi là liên kết được tạo bởi 2 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng hai gạch nối “=”
+ Liên kết ba là liên kết được tạo bởi 3 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng ba gạch nối “≡”
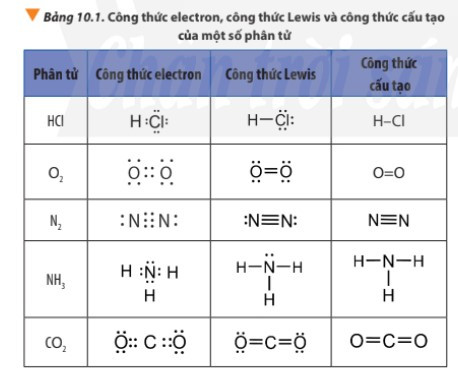
2. Tìm hiểu cách viết công thức Lewis
- Công thức Lewis biểu diễn sự hình thành liên kết hóa học giữa các nguyên tử trong một phân tử.
- Công thức Lewis của một phân tử được xây dựng từ công thức electron của phân tử, trong đó mỗi cặp electron chung giữa hai nguyên tử tham gia liên kết được thay bằng một gạch nối “–”.
II. Liên kết cho - nhận
- Liên kết cho – nhận là một trường hợp đặc biệt của liên kết cộng hóa trị, trong đó cặp electron chung chỉ do một nguyên tử đóng góp.
- Nguyên tử “cho” là nguyên tử đóng góp cặp electron chung, nguyên tử đó phải còn cặp electron chưa liên kết.
- Nguyên tử “nhận” là nguyên tử không đóng góp electron, nguyên tử đó phải còn orbital trống, không chứa electron.
- Để biễu diễn liên kết cho - nhận, một mũi tên được hướng từ nguyên tử cho sang nguyên tử nhận để phân biệt với các liên kết còn lại.
Ví dụ: Sự tạo thành liên kết cho - nhận trong ion NH4+
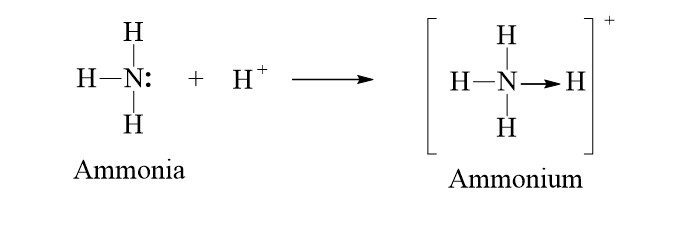
+ Trong phân tử NH3, nguyên tử N còn 1 cặp electron chưa tham gia liên kết, ion H+ có orbital trống, không chứa electron. Khi cho NH3 kết hợp với ion H+, nguyên tử N sử dụng một cặp electron chưa liên kết làm cặp electron chung với ion H+ tạo thành ion NH4+.
+ Nguyên tử N đóng góp cặp electron chung nên là nguyên tử cho.
+ Ion H+ không đóng góp electron, đóng vai trò nhận electron.
III. Phân biệt các loại liên kết dựa theo độ âm điện
1. Phân biệt liên kết cộng hóa trị phân cực và không phân cực
- Liên kết cộng hóa trị không phân cực là liên kết cộng hóa trị trong đó cặp electron chung không lệch về phía nguyên tử nào.
Ví dụ: Liên kết cộng hóa trị trong các phân tử H2, Br2 là liên kết cộng hóa trị không phân cực.
![]()
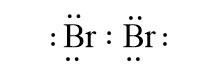
- Liên kết cộng hóa trị phân cực là liên kết cộng hóa trị trong đó cặp electron chung lệch về phía nguyên tử có độ âm điện lớn hơn.
Ví dụ: Liên kết cộng hóa trị trong các phân tử HBr, H2O là liên kết cộng hóa trị phân cực.
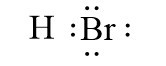
![]()
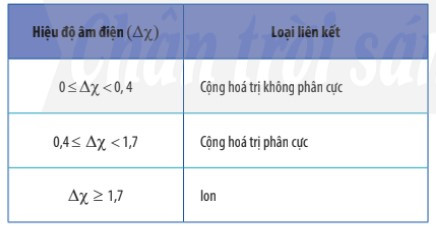
2. Phân biệt loại liên kết trong phân tử dựa trên giá trị hiệu độ âm điện
- Có thể dựa vào hiệu độ âm điện (∆χ) giữa hai nguyên tử tham gia liên kết để dự đoán loại liên kết giữa chúng.
Ví dụ:
+ Trong phân tử MgCl2
![]()
⇒ Liên kết Mg-Cl trong phân tử MgCl2 là liên kết ion.
+ Trong phân tử CO2
![]()
⇒ Liên kết C=O trong phân tử CO2 là liên kết cộng hóa trị phân cực.
+ Trong phân tử C2H4
![]()
⇒ Liên kết C-H trong phân tử C2H4 là liên kết cộng hóa trị không phân cực.
IV. Sự hình thành liên kết ?, ? và năng lượng liên kết
1. Tìm hiểu sự hình thành liên kết ? và liên kết ?
- Liên kết σ là loại liên kết cộng hóa trị được hình thành do sự xen phủ trục của hai orbital. Vùng xen phủ nằm trên đường nối tâm hai nguyên tử.
Ví dụ:
+ Sự xen phủ trục giữa 2 AO 1s của hai nguyên tử hydrogen hình thành liên kết σ trong phân tử H2.
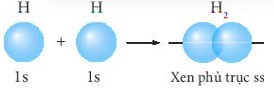
+ Sự xen phủ giữa AO 1s của nguyên tử H và AO 2p của nguyên tử F hình thành liên kết σ trong phân tử HF.
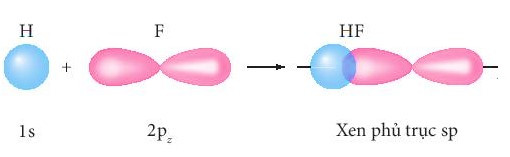
+ Sự xen phủ giữa hai AO 2p của hai nguyên tử fluorine hình thành liên kết σ trong phân tử fluorine.
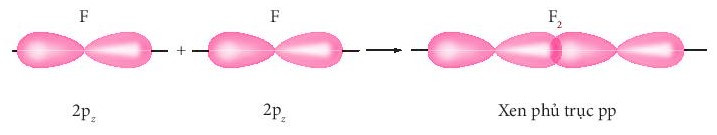
- Liên kết π là loại liên kết cộng hóa trị được hình thành do sự xen phủ bên của hai orbital. Vùng xen phủ nằm hai bên đường nối tâm hai nguyên tử.
Ví dụ:
Sự xen phủ các AO hình thành liên kết σ và liên kết π trong phân tử oxygen.
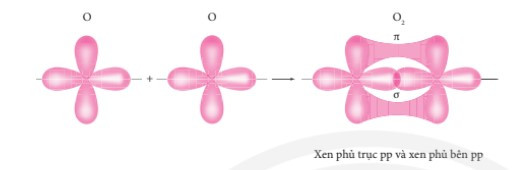
Chú ý:
- Liên kết đơn gồm 1 liên kết σ.
- Liên kết đôi gồm 1 liên kết σ và 1 liên kết π.
- Liên kết ba gồm 1 liên kết σ và hai liên kết π.
- Liên kết σ bền vững hơn liên kết π.
2. Tìm hiểu khái niệm năng lượng liên kết (Eb)
- Năng lượng liên kết của một liên kết hóa học là năng lượng cần thiết để phá vỡ 1 mol liên kết đó ở thể khí, tạo thành các nguyên tử ở thể khí.
- Năng lượng liên kết đặc trưng cho độ bền liên kết. Năng lượng liên kết càng lớn thì liên kết càng bền và ngược lại.
Ví dụ:
N2(g) → 2N(g) Eb = 945 kJ/ mol
Ta nói năng lượng liên kết trong phân ử N2 là 945 kJ/ mol. Điều này có nghĩa cần cung cấp 945 kJ để phá vỡ 1 mol khí N2 thành các nguyên tử ở thể khí.
- Đối với các phân tử nhiều nguyên tử, tổng năng lượng liên kết trong phân tử bằng năng lượng cần cung cấp để phá vỡ hoàn toàn 1 mol phân tử đó ở thể khí thành các nguyên tử ở thể khí.
Ví dụ:
Tổng năng lượng liên kết trong phân tử CH4 là 1660 kJ/ mol.
CH4 (g) → C(g) + 4H(g) Eb = 1660 kJ/ mol
Do đó, năng lượng liên kết trung bình của một liên kết C – H là:
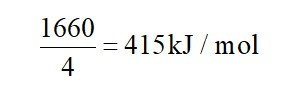
Chú ý: Nhận biết phân tử phân cực và phân tử không phân cực:
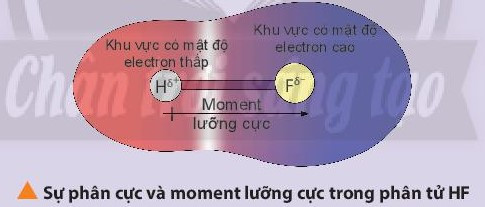
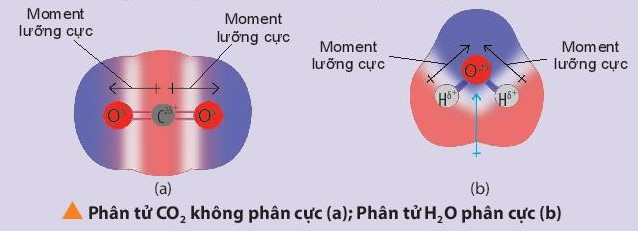
+ Phân tử phân cực là phân tử có tổng tất cả moment lưỡng cực trong phân tử khác không. Các phân tử phân cực thường tan tốt trong nước và các dung môi phân cực khác.
+ Phân tử không phân cực là phân tử có tổng tất cả các moment lưỡng cực trong phân tử bằng không. Phân tử không phân cực thường hòa tan tốt trong các dung môi không phân cực.
B. Trắc nghiệm Liên kết cộng hóa trị
Câu 1. Liên kết giữa hai nguyên tử được hình thành bởi một cặp electron chung được gọi là
A. liên kết bội
B. liên kết đơn
C. liên kết đôi
D. liên kết ba
Đáp án đúng là: B
Liên kết giữa hai nguyên tử được hình thành bởi một cặp electron chung được gọi là liên kết đơn và được biểu diễn bằng một gạch nối “−”.
Câu 2. Dựa vào số cặp electron chung, liên kết cộng hóa trị được chia thành mấy loại?
A. 2 loại: liên kết σ và liên kết π
B. 2 loại: liên kết cộng hóa trị không phân cực và liên kết cộng hóa trị phân cực
C. 3 loại: liên kết đơn, liên kết đôi và liên kết ba
D. 2 loại: liên kết đơn và liên kết đôi
Đáp án đúng là: C
Dựa vào số cặp electron chung, liên kết cộng hóa trị được chia thành 3 loại:
+ Liên kết đơn (1 cặp electron chung)
+ Liên kết đôi (2 cặp electron chung)
+ Liên kết ba (3 cặp electron chung).
Câu 3. Liên kết cộng hóa trị được chia thành liên kết cộng hóa trị không phân cực và phân cực dựa vào
A. số cặp electron chung
B. sự xen phủ các orbital
C. vị trí của các cặp electron chung
D. vị trí của các electron hóa trị riêng
Đáp án đúng là: C
Liên kết cộng hóa trị được chia thành liên kết cộng hóa trị không phân cực và phân cực dựa vào vị trí của các cặp electron chung.
+ Liên kết cộng hóa trị không phân cực: cặp electron chung không lệch về phía nguyên tử nào.
+ Liên kết cộng hóa trị phân cực: cặp electron chung bị lệch về phía nguyên tử có độ âm điện lớn hơn.
Câu 4. Liên kết cộng hóa trị là liên kết hình thành giữa hai nguyên tử bằng
A. lực hút tĩnh điện giữa các ion mang điện tích trái dấu
B. một cặp electron chung
C. một hay nhiều cặp electron chung
D. các electron hóa trị riêng
Đáp án đúng là: C
Liên kết cộng hóa trị là liên kết hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
Câu 5. Trong phân tử N2, mỗi nguyên tử N đã góp 3 electron để tạo cặp electron chung. Nhờ đó mỗi nguyên tử N đã đạt cấu hình electron bền vững của khí hiếm
A. Xe
B. Ne
C. Ar
D. Kr
Đáp án đúng là: B
N (Z = 7): 1s22s22p3 có 5 electron lớp ngoài cùng ⇒ mỗi nguyên tử N góp 3 electron để đạt cấu hình electron lớp ngoài cùng bền vững của khí hiếm gần nhất là Ne.

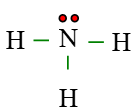
Câu 6. Cho công thức Lewis của phân tử NH3 dưới đây. Số electron dùng chung của N là
A. 2 electron dùng chung
B. 3 electron dùng chung
C. 6 electron dùng chung
D. 5 electron dùng chung
Đáp án đúng là: C
Xung quanh nguyên tử N có tổng cộng 3 nối đơn (−) mà mỗi nối đơn biểu diễn 1 cặp electron dùng chung ⇒ có 6 electron dùng chung.
Câu 7. Công thức biểu diễn cấu tạo nguyên tử qua các liên kết và các electron hóa trị riêng là
A. công thức phân tử
B. công thức electron
C. công thức Lewis
D. công thức đơn giản nhất
Đáp án đúng là: C
Công thức biểu diễn cấu tạo nguyên tử qua các liên kết (cặp electron dùng chung) và các electron hóa trị riêng là công thức Lewis.
Câu 8. Trong một phân tử CO2 có số cặp electron chung là
A. 1
B. 2
C. 3
D. 4
Đáp án đúng là: D
O (Z = 8): [He]2s22p4 ⇒ có 6 electron lớp ngoài cùng ⇒ xu hướng nhận 2 electron để đạt cấu hình electron bền vững ⇒ góp 2 electron.
C (Z = 6): [He]2s22p2 ⇒ có 4 electron lớp ngoài cùng ⇒ xu hướng nhận 4 electron để đạt cấu hình electron bền vững ⇒ góp 4 electron tạo 4 cặp electron dùng chung với O.
Sự hình thành liên kết cộng hóa trị trong phân tử CO2:
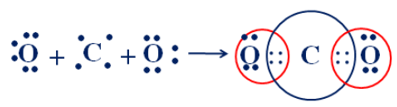
Vậy trong một phân tử CO2 có 4 cặp electron chung.
Câu 9. Công thức electron của phân tử H2O là
A.
B.
C.
D.
Đáp án đúng là: A
H (Z = 1): 1s1 ⇒ có 1 electron lớp ngoài cùng ⇒ xu hướng nhận 1 electron để đạt cấu hình electron bền vững của khí hiếm He ⇒ góp 1 electron.
O (Z = 8): [He]2s22p4 ⇒ có 6 electron lớp ngoài cùng ⇒ xu hướng nhận 2 electron để đạt cấu hình electron bền vững ⇒ góp 2 electron tạo hai cặp electron dùng chung với H.
Công thức electron của phân tử H2O là:
Câu 10. Liên kết trong phân tử nào dưới đây là liên kết đôi?
A. NH3
B. HCl
C. O2
D. N2
Đáp án đúng là: C
O (Z = 8): [He]2s22p4 ⇒ có 6 electron lớp ngoài cùng ⇒ xu hướng nhận 2 electron để đạt cấu hình electron bền vững ⇒ góp 2 electron.
Công thức electron của phân tử O2 là:
Công thức cấu tạo là: O = O
Vậy liên kết trong phân tử O2 là liên kết đôi.
Xem thêm tóm tắt lý thuyết Hóa học 10 sách Chân trời sáng tạo hay, chi tiết khác:
Lý thuyết Bài 11: Liên kết hydrogen và tương tác van der waals
Lý thuyết Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Lý thuyết Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Lý thuyết Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Lý thuyết Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Soạn văn lớp 10 (ngắn nhất) – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Giải sbt Ngữ văn lớp 10 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Văn mẫu lớp 10 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 10 – Chân trời sáng tạo
- Giải sgk Toán 10 – Chân trời sáng tạo
- Giải Chuyên đề Toán 10 – Chân trời sáng tạo
- Lý thuyết Toán 10 – Chân trời sáng tạo
- Giải sbt Toán 10 – Chân trời sáng tạo
- Chuyên đề dạy thêm Toán 10 Chân trời sáng tạo (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Giải sbt Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 10 Friends Global đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 Friends Global
- Giải sgk Vật lí 10 – Chân trời sáng tạo
- Giải sbt Vật lí 10 – Chân trời sáng tạo
- Lý thuyết Vật lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Vật lí 10 – Chân trời sáng tạo
- Giải sgk Sinh học 10 – Chân trời sáng tạo
- Giải sbt Sinh học 10 – Chân trời sáng tạo
- Lý thuyết Sinh học 10 – Chân trời sáng tạo
- Giải Chuyên đề Sinh học 10 – Chân trời sáng tạo
- Giải sgk Lịch sử 10 – Chân trời sáng tạo
- Giải sbt Lịch sử 10 – Chân trời sáng tạo
- Giải Chuyên đề Lịch sử 10 – Chân trời sáng tạo
- Lý thuyết Lịch sử 10 – Chân trời sáng tạo
- Giải sgk Địa lí 10 – Chân trời sáng tạo
- Lý thuyết Địa Lí 10 - Chân trời sáng tạo
- Giải sbt Địa lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Địa lí 10 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải Chuyên đề Kinh tế và pháp luật 10 – Chân trời sáng tạo
- Lý thuyết KTPL 10 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 10 – Chân trời sáng tạo