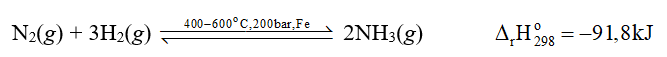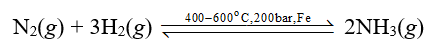Giải Hóa 11 trang 38 Cánh diều
Với giải bài tập Hóa học lớp 11 trang 38 trong Bài 5: Một số hợp chất quan trọng của nitrogen sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 11 trang 38.
Giải Hóa 11 trang 38 Cánh diều
Lời giải:
Gần đây, mỗi năm có khoảng hàng trăm triệu tấn ammonia được sản xuất trên toàn cầu. Trong đó, có khoảng 80% được sử dụng để sản xuất phân đạm ammonium, urea … để cung cấp nguyên tố nitrogen cho đất và cây trồng. Ví dụ phản ứng dưới đây dùng để tổng hợp ra phân bón với thành phần chính là ammonium sulfate:
2NH3(aq) + H2SO4(aq) → (NH4)2SO4(aq)
Vì thế có thể nói ammonia có vai trò rất quan trọng đối với nông nghiệp.
Lời giải:
ΔrHo298=−91,8kJ<0 phản ứng thuận toả nhiệt. Tuy nhiên, khi thực hiện phản ứng ở nhiệt độ quá thấp thì tốc độ của phản ứng nhỏ, phản ứng diễn ra chậm. Thực tế, người ta đã chọn nhiệt độ phù hợp, khoảng 400 oC – 600 oC.
a) Hãy tính nồng độ mol của ammonia có trong buồng phản ứng tại thời điểm cân bằng.
b) Làm thế nào để tách được ammonia ra khỏi hỗn hợp?
Lời giải:
Ban đầu: a b 0 M
Phản ứng: x 3x 2x M
Cân bằng: 0,0201 0,0602 2x M
Áp dụng công thức có:
K=[NH3]2[N2].[H2]3⇔[NH3]=2x=√K.[N2].[H2]3=√0,105.0,0201.0,06023=6,79.10−4M
b) Tại thời điểm cân bằng, nồng độ ammonia, nitrogen và hydrogen trong buồng phản ứng là không đổi. Khi đó hỗn hợp khí này được dẫn qua hệ thống làm lạnh để hoá lỏng ammonia và tách ra khỏi hỗn hợp.
2CO(g) + 2NO(g) → 2CO2(g) +N2(g)
a) Cho biết ý nghĩa của phản ứng trên đối với môi trường.
b) Trong phản ứng trên, chất nào là chất oxi hoá, chất nào là chất khử? Giải thích.
c) Giá trị enthalpy tạo thành chuẩn của CO(g), NO(g), CO2(g) lần lượt là –110,5; 91,3; –393,5 (kJ mol-1). Hãy tính biến thiên enthalpy chuẩn của phản ứng trên. Phản ứng trên có thuận lợi về mặt năng lượng không? Giải thích.
Lời giải:
a) Ý nghĩa của phản ứng: 2CO(g) + 2NO(g) → 2CO2(g) + N2(g) đối với môi trường là giảm khí độc CO, giảm tác nhân gây mưa acid NO phát sinh từ quá trình đốt cháy nhiên liệu.
b) 2+2CO(g) + 2+2NO(g) → 2+4CO2(g) +0N2(g)
Số oxi hoá của carbon tăng từ +2 lên +4 sau phản ứng nên CO đóng vai trò là chất khử.
Số oxi hoá của nitrogen giảm từ +2 xuống 0 sau phản ứng nên NO đóng vai trò là chất oxi hoá.
c)
ΔrHo298=2.ΔfHo298(CO2(g))+ΔfHo298(N2(g))−2.ΔfHo298(CO(g))−2.ΔfHo298(NO(g))
= 2. (-393,5) + 0 – 2.(-110,5) – 2.91,3 = -748,6 (kJ) < 0.
Vậy phản ứng này toả nhiệt, thuận lợi về mặt năng lượng.
Bài tập 5 trang 38 Hoá học 11: Viết sơ đồ phản ứng gây ra mưa chứa nitric acid và sulfuric acid.
Lời giải:
- Sơ đồ phản ứng gây ra mưa chứa nitric acid:
N2+O2→NO +O2→NO2+O2+H2O→HNO3→H++NO−3
Các phương trình hoá học minh hoạ cho sơ đồ:
N2(g) + O2(g) to⇌ 2NO(g)
2NO(g) + O2(g) → 2NO2(g)
4NO2(g) + 2H2O(l) + O2(g) → 4HNO3(aq)
HNO3 → H+ + NO3-
- Sơ đồ phản ứng gây ra mưa chứa sulfuric acid:
H2SO3+H2O← SO2+O2→ SO3+H2O→ H2SO4
Các phương trình hoá học minh hoạ cho sơ đồ:
SO2 + H2O → H2SO3
SO2+12O2NO/NO2→SO3
SO3 + H2O → H2SO4.
Lời giải:
- Một số hoạt động tạo thành các khí gây mưa acid tại địa phương em: khí thải của phương tiện giao thông; khí thải của nhà máy chưa qua xử lí ra môi trường; khí thải do đốt rác, đốt than …
- Một số biện pháp giảm thiểu sự tạo thành các khí này:
+ Tăng cường sử dụng xe đạp, phương tiện công cộng thay cho các phương tiện động cơ cá nhân như ô tô, xe máy …
+ Tăng cường sử dụng các nguồn năng lượng mới, năng lượng sạch, năng lượng tái tạo;
+ Sử dụng tiết kiệm, hiệu quả nguồn tài nguyên thiên nhiên;
+ Cải tiến công nghệ sản xuất, có biện pháp xử lí khí thải và tái chế các sản phẩm phụ có chứa sulfur.
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Mở đầu trang 30 Hoá học 11: Trong các ao tù có thể tích tụ lượng đáng kể ion ammonium.
Luyện tập 1 trang 31 Hoá học 11: Cho thí nghiệm được thiết kế như hình dưới đây:
Câu hỏi 4 trang 35 Hoá học 11: Cho biết số oxi hoá
Câu hỏi 5 trang 36 Hoá học 11: Công thức Lewis của HNO3 như dưới đây có phù hợp không?
Bài tập 5 trang 38 Hoá học 11: Viết sơ đồ phản ứng gây ra mưa chứa nitric acid và sulfuric acid.
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Bài 6: Sulfur và sulfur dioxide
Bài 7: Sulfuric acid và muối sulfate
Bài 8: Hợp chất hữu cơ và hoá học hữu cơ
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Cánh diều (hay nhất)
- Văn mẫu lớp 11 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 11 – Cánh diều
- Tác giả tác phẩm Ngữ văn 11 - Cánh diều
- Giải SBT Ngữ văn 11 – Cánh diều
- Bố cục tác phẩm Ngữ văn 11 – Cánh diều
- Giải Chuyên đề học tập Ngữ văn 11 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Cánh diều
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 – Cánh diều
- Giải Chuyên đề học tập Toán 11 – Cánh diều
- Lý thuyết Toán 11 - Cánh diều
- Giải sbt Toán 11 – Cánh diều
- Giải sgk Tiếng Anh 11 – ilearn Smart World
- Giải sbt Tiếng Anh 11 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 11 ilearn Smart World đầy đủ nhất
- Giải sgk Vật lí 11 – Cánh diều
- Lý thuyết Vật lí 11 – Cánh diều
- Giải sbt Vật lí 11 – Cánh diều
- Giải Chuyên đề học tập Vật lí 11 – Cánh diều
- Giải sgk Sinh học 11 – Cánh diều
- Lý thuyết Sinh học 11 – Cánh diều
- Giải Chuyên đề học tập Sinh học 11 – Cánh diều
- Giải sbt Sinh học 11 – Cánh diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Cánh diều
- Lý thuyết Kinh tế pháp luật 11 – Cánh diều
- Giải sbt Kinh tế pháp luật 11 – Cánh diều
- Giải sgk Lịch sử 11 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 11 – Cánh diều
- Lý thuyết Lịch sử 11 - Cánh diều
- Giải sbt Lịch sử 11 – Cánh diều
- Giải sgk Địa lí 11 – Cánh diều
- Giải Chuyên đề học tập Địa lí 11 – Cánh diều
- Lý thuyết Địa lí 11 - Cánh diều
- Giải sbt Địa lí 11 – Cánh diều
- Giải sgk Công nghệ 11 – Cánh diều
- Lý thuyết Công nghệ 11 - Cánh diều
- Giải sbt Công nghệ 11 – Cánh diều
- Giải sgk Tin học 11 – Cánh diều
- Giải Chuyên đề học tập Tin học 11 – Cánh diều
- Lý thuyết Tin học 11 - Cánh diều
- Giải sbt Tin học 11 – Cánh diều
- Giải sgk Giáo dục quốc phòng an ninh 11 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 11 – Cánh diều
- Giải sbt Giáo dục quốc phòng 11 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 – Cánh diều