Trong phương pháp chuẩn độ acid – base, xung quanh điểm tương đương có một sự thay đổi
Lời giải Bài 2.21 trang 13 SBT Hóa học 11 sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 11.
Giải SBT Hóa học 11 Bài 2: Cân bằng trong dung dịch nước
Bài 2.21 trang 13 SBT Hóa học 11: Trong phương pháp chuẩn độ acid – base, xung quanh điểm tương đương có một sự thay đổi pH đột ngột gọi là bước nhảy chuẩn độ. Đường biểu diễn trên đồ thị chuẩn độ acid – base gọi là đường định phân. Từ các số liệu sau đây, hãy vẽ đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ dung dịch HCl bằng dung dịch chuẩn NaOH 0,100 M. Trục hoành ghi thể tích dung dịch NaOH, trục tung ghi pH của dung dịch. Xác định giá trị điểm tương đương và khoảng bước nhảy chuẩn độ của quá trình này.
|
VNaOH (mL) |
Giá trị pH |
VNaOH (mL) |
Giá trị pH |
|
0,0 |
1,00 |
25,1 |
10,30 |
|
5,0 |
1,18 |
25,5 |
11,00 |
|
10,0 |
1,37 |
26,0 |
11,29 |
|
15,0 |
1,60 |
28,0 |
11,75 |
|
20,0 |
1,95 |
30,0 |
11,96 |
|
22,0 |
2,20 |
35,0 |
12,22 |
|
24,0 |
2,69 |
40,0 |
12,36 |
|
24,5 |
3,00 |
45,0 |
12,46 |
|
24,9 |
3,70 |
50,0 |
12,52 |
|
25,0 |
7,00 |
|
|
Lời giải:
- Đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ dung dịch HCl bằng dung dịch chuẩn NaOH 0,100 M:
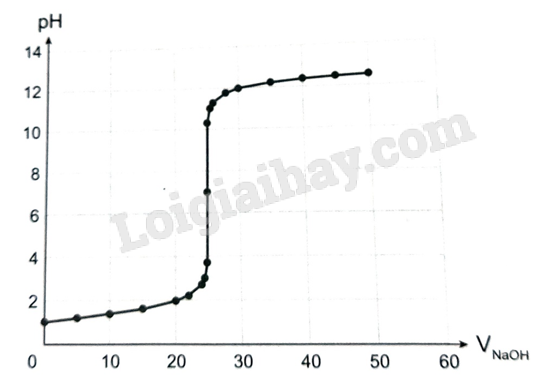
- Chuẩn độ HCl (acid mạnh) bằng NaOH (base mạnh):
+ Tại điểm tương đương, [H+] = [OH-]; pH = 7.
+ Bước nhảy chuẩn độ: ở khoảng pH từ 3,7 đến 10,3.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Bài 2.1 trang 11 SBT Hóa học 11: Vì sao dung dịch của các muối, acid, base dẫn điện?...
Bài 2.2 trang 11 SBT Hóa học 11: Dung dịch sodium chloride (NaCl) dẫn được điện là do...
Bài 2.3 trang 11 SBT Hóa học 11: Saccharose là chất không điện li vì...
Bài 2.4 trang 11 SBT Hóa học 11: Phát biểu nào sau đây đúng khi nói về sự điện li?...
Bài 2.5 trang 11 SBT Hóa học 11: Các chất trong dãy nào sau đây là những chất điện li mạnh?...
Bài 2.6 trang 12 SBT Hóa học 11: Phương trình diện là nào sau đây biểu diễn không đúng?...
Bài 2.7 trang 12 SBT Hóa học 11: Phương trình diện là nào sau đây biểu diễn đúng?...
Bài 2.11 trang 12 SBT Hóa học 11: Tính nồng độ mol của các ion trong các dung dịch sau:..
Bài 2.14 trang 12 SBT Hóa học 11: Cho các phân tử và ion sau:...
Bài 2.15 trang 13 SBT Hóa học 11: a) Tính pH của dung dịch có nồng độ ion H+ là 4,2×10-10 M...
Xem thêm lời giải Sách bài tập Hóa học lớp 11 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Ammonia và một số hợp chất ammonium
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Chân trời sáng tạo (hay nhất)
- Văn mẫu lớp 11 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 11 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 11 - Chân trời sáng tạo
- Giải SBT Ngữ văn 11 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 11 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Chân trời sáng tạo
- Soạn văn 11 Chân trời sáng tạo (ngắn nhất)
- Giải sgk Toán 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Toán 11 – Chân trời sáng tạo
- Lý thuyết Toán 11 - Chân trời sáng tạo
- Giải sbt Toán 11 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 11 – Friends Global
- Giải sbt Tiếng Anh 11 - Friends Global
- Trọn bộ Từ vựng Tiếng Anh 11 Friends Global đầy đủ nhất
- Bài tập Tiếng Anh 11 Friends Global theo Unit có đáp án
- Giải sgk Vật lí 11 – Chân trời sáng tạo
- Lý thuyết Vật lí 11 – Chân trời sáng tạo
- Giải sbt Vật lí 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Vật lí 11 – Chân trời sáng tạo
- Giải sgk Sinh học 11 – Chân trời sáng tạo
- Lý thuyết Sinh học 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Sinh học 11 – Chân trời sáng tạo
- Giải sbt Sinh học 11 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Chân trời sáng tạo
- Lý thuyết Kinh tế pháp luật 11 – Chân trời sáng tạo
- Giải sbt Kinh tế pháp luật 11 – Chân trời sáng tạo
- Giải sgk Lịch sử 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Lịch sử 11 – Chân trời sáng tạo
- Lý thuyết Lịch sử 11 - Chân trời sáng tạo
- Giải sbt Lịch sử 11 – Chân trời sáng tạo
- Giải sgk Địa lí 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Địa lí 11 – Chân trời sáng tạo
- Lý thuyết Địa lí 11 - Chân trời sáng tạo
- Giải sbt Địa lí 11 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 11 – Chân trời sáng tạo
