Sách bài tập Hóa 11 (Chân trời sáng tạo): Ôn tập chương 5
Với giải sách bài tập Hóa 11 Ôn tập chương 5 sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa 11 Ôn tập chương 5.
Giải SBT Hóa 11 Ôn tập chương 5
B. C2H5Cl.
C. C6H5OH.
D. C6H5Cl.
Lời giải:
Đáp án đúng là: A
C2H5OH là chất lỏng, không màu, tan vô hạn trong nước.
B. nước nóng.
C. nước bromine.
D. dung dịch NaOH.
Lời giải:
Đáp án đúng là: C
Phenol làm mất màu dung dịch bromine còn ethanol không phản ứng.
C. C6H5Cl.
D. CH3CH(Br)CH3.
Lời giải:
Đáp án đúng là: C
C6H5Cl + NaOH → C6H5OH + NaCl
Bài OT5.4 trang 87 Sách bài tập Hóa học 11: Phát biểu nào sau đây không đúng?
A. Phenol có nhiệt độ sôi cao hơn và độ tan trong nước kém hơn ethanol.
B. Dẫn xuất halogen của hydrocarbon không tan trong nước lạnh, tan nhiều trong nước ở 66 °C.
C. Theo chiều tăng phân tử khối, nhiệt độ sôi của các dẫn xuất halogen tăng từ F đến I.
D. Độ tan của các alcohol có cùng số nhóm -OH giảm khi mạch carbon tăng.
Lời giải:
Đáp án đúng là: B
Phần lớn dẫn xuất halogen nặng hơn nước và không tan trong nước, tan tốt trong dung môi hữu cơ kém phân cực như hydrocarbon, ether,…
Lời giải:
Đáp án đúng là: D
C2H5Br + NaOH to→ C2H5OH + NaBr
C6H5Cl + NaOH → C6H5OH + NaCl
Bài OT5.6 trang 88 Sách bài tập Hóa học 11: Xác nhận đúng hoặc sai cho các phát biểu trong bảng sau:
|
STT |
Phát biểu |
Đúng/sai |
|
1 |
Các dẫn xuất halogen đều chứa nguyên tử carbon, hydrogen và halogen trong phân tử. |
? |
|
2 |
Alcohol là hợp chất hữu có nhóm -OH liên kết trực tiếp với nguyên tử carbon. |
? |
|
3 |
|
? |
|
4 |
Các dẫn xuất halogen rất ít tan trong nước. |
? |
|
5 |
Các halogenoalkane và alkanol tham gia phản ứng tách để tạo ra alkene. |
? |
|
6 |
Phenol tham gia phản ứng thế (thế halogen, thế nitro, ...) dễ hơn benzene. |
? |
|
7 |
Các alcohol tạo được liên kết hydrogen với các phân tử nước nên nhiệt độ sôi của alcohol tương đối cao. |
? |
Lời giải:
|
STT |
Phát biểu |
Đúng/sai |
|
1 |
Các dẫn xuất halogen đều chứa nguyên tử carbon, hydrogen và halogen trong phân tử. |
Sai |
|
2 |
Alcohol là hợp chất hữu có nhóm -OH liên kết trực tiếp với nguyên tử carbon. |
Sai |
|
3 |
|
Đúng |
|
4 |
Các dẫn xuất halogen rất ít tan trong nước. |
Đúng |
|
5 |
Các halogenoalkane và alkanol tham gia phản ứng tách để tạo ra alkene. |
Sai |
|
6 |
Phenol tham gia phản ứng thế (thế halogen, thế nitro, ...) dễ hơn benzene. |
Đúng |
|
7 |
Các alcohol tạo được liên kết hydrogen với các phân tử nước nên nhiệt độ sôi của alcohol tương đối cao. |
Sai |
Lời giải:
Năng lượng liên kết C-X lớn, độ dài liên kết C-X giảm, độ bền liên kết C-X tăng. Theo chiều từ liên kết C-F đến C-I, năng lượng liên kết giảm dần, độ dài liên kết tăng, đồng thời sự phân cực giảm nên khả năng thế nhóm -OH tăng theo chiều:
C-F < C-Cl < C-Br < C-I.
|
Chất |
Nhiệt độ sôì (°C) |
Độ tan trong nước tại 25 °C |
|
(A) |
72,0 |
- |
|
(B) |
64,7 |
∞ |
|
(C) |
198,0 |
∞ |
|
(D) |
182,0 |
0,895 (mol/L) |
Lập luận để xác định công thức của các chất (A), (B), (C) và (D).
Lời giải:
- Dựa vào độ tan trong nước, nhận thấy được (A), (B), (C) và (D) có nhiệt độ sôi khác nhau không nhiều.
- Dựa vào sự khác nhau nhiều về nhiệt độ sôi, nhận thấy được (B) và (C) tan vô hạn trong nước.
Vậy (A) là C2H5I; (B) là C2H5OH; (C) là C2H4(OH)2; (D) là C6H5OH.
Một loại nước uống có cồn, thể tích bình chứa 330 mL dung dịch và trên nhãn ghi độ cồn là 4,5°.
a) Tính thể tích ethanol có trong 330mL dung dịch của loại nước uống này.
b) Tính khối lượng của ethanol có trong 330 mL dung dịch (khối lượng riêng của ethanol 0,789 g/mL).
c) Một số poster tuyên truyền về LD50 của ethanol bằng cách quy đổi khối lượng ethanol về số lượng cốc rượu, bia hoặc đơn vị lon, chai, ... uống vào cơ thể. LD50 của ethanol đối với người trưởng thành là 5 gam - 8 gam. Khi thiết kế poster, cần vẽ bao nhiêu đơn vị bình chứa để thể hiện giá trị LD50 của ethanol cho một người trưởng thành có cân nặng trung bình 60 kg.
Lời giải:
a) Thể tích ethanol có trong 330 mL dung dịch:
VC2H5OH=330×4,5100=14,85 (mL).
b) Khối lượng của ethanol có trong 330 mL dung dịch:
mC2H5OH=dC2H5OH×VC2H5OH=14,85×0,789=11,72(g).
c) Lượng ethanol trung bình có thể gây tử vong cho 50% đối tượng là người trưởng thành nặng 60 kg khoảng: 5 × 60 = 300 (g).
Mỗi đơn vị bình chứa 11,72 gam ethanol. Với giá trị 300 gam ethanol, cần số đơn vị bình chứa:
30011,72=25,6 (bình chứa)
Vậy khi thiết kế poster cần vẽ 25 đơn vị bình chứa.
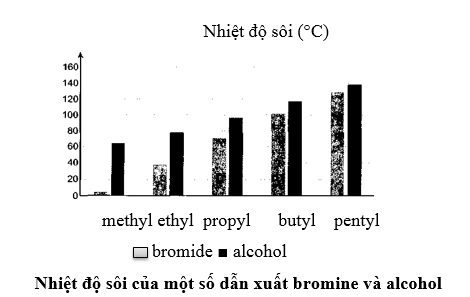
a) Nhận xét sự biến thiên nhiệt độ sôi của các hợp chất trong biểu đồ trên theo chiều tăng gốc alkyl và giải thích.
b) Vì sao nhiệt độ sôi của ethanol cao hơn bromoethane (ethyl bromide)?
Lời giải:
a) Theo chiều tăng gốc alkyl, từ methyl đến pentyl, nhiệt độ sôi của các dẫn xuất bromide và alcohol tăng dần. Nguyên nhân là do sự tăng tương tác van der Waals giữa các phân tử.
b) Nhiệt độ sôi của ethanol cao hơn bromoethane (ethyl bromide) là do giữa các phân tử alcohol hình thành liên kết hydrogen.
Phổ khối lượng của hợp chất (X)
Biện luận để xác định cấu tạo phân tử hợp chất hữu cơ (X).
Lời giải:
Trong phổ IR:
- Hợp chất hữu cơ (X) có vòng benzene, có thể là gốc phenyl (C6H5-) hoặc -C6H4-, ...
- Tín hiệu mạnh ở số sóng 3 329 cm-1, đặc trưng cho nhóm -OH ⇒ phenol hoặc alcohol.
- Tín hiệu ở số sóng 1 023 cm-1, đặc trưng cho C-O ⇒ alcohol (C-O phenol thường nằm trong vùng 1 260 - 1 200 cm_1).
Trong phổ MS:
- Tín hiệu có m/z = 77, C6H5.
- Tín hiệu có m/z = 108 ⇒ công thức phân tử và công thức cấu tạo của (X) lần lượt là C7H8O và C6H5-CH2-OH.
- Các tín hiệu mạnh còn lại có thể là hợp chất trung gian.
Xem thêm giải Sách bài tập Hóa học 11 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Chân trời sáng tạo (hay nhất)
- Văn mẫu lớp 11 - Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn 11 – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 11 - Chân trời sáng tạo
- Giải SBT Ngữ văn 11 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 11 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Chân trời sáng tạo
- Soạn văn 11 Chân trời sáng tạo (ngắn nhất)
- Giải sgk Toán 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Toán 11 – Chân trời sáng tạo
- Lý thuyết Toán 11 - Chân trời sáng tạo
- Giải sbt Toán 11 – Chân trời sáng tạo
- Giải sgk Tiếng Anh 11 – Friends Global
- Giải sbt Tiếng Anh 11 - Friends Global
- Trọn bộ Từ vựng Tiếng Anh 11 Friends Global đầy đủ nhất
- Bài tập Tiếng Anh 11 Friends Global theo Unit có đáp án
- Giải sgk Vật lí 11 – Chân trời sáng tạo
- Lý thuyết Vật lí 11 – Chân trời sáng tạo
- Giải sbt Vật lí 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Vật lí 11 – Chân trời sáng tạo
- Giải sgk Sinh học 11 – Chân trời sáng tạo
- Lý thuyết Sinh học 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Sinh học 11 – Chân trời sáng tạo
- Giải sbt Sinh học 11 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Chân trời sáng tạo
- Lý thuyết Kinh tế pháp luật 11 – Chân trời sáng tạo
- Giải sbt Kinh tế pháp luật 11 – Chân trời sáng tạo
- Giải sgk Lịch sử 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Lịch sử 11 – Chân trời sáng tạo
- Lý thuyết Lịch sử 11 - Chân trời sáng tạo
- Giải sbt Lịch sử 11 – Chân trời sáng tạo
- Giải sgk Địa lí 11 – Chân trời sáng tạo
- Giải Chuyên đề học tập Địa lí 11 – Chân trời sáng tạo
- Lý thuyết Địa lí 11 - Chân trời sáng tạo
- Giải sbt Địa lí 11 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 11 – Chân trời sáng tạo

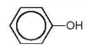 là hợp chất không thuộc loại alcohol.
là hợp chất không thuộc loại alcohol.