Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết
Lời giải bài 14.5 trang 57 SBT Hóa học 10 sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải SBT Hóa học 10 Chân trời sáng tạo Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 14.5 trang 57 SBT Hóa học 10. Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 SGK), của F2, H2, HF, N2, O2, NO. Giải thích sự khác nhau về nhiệt tạo thành của HF và NO.
Lời giải:
Áp dụng công thức:
= 945 kJ/mol,
Eb(O=O) = 498 kJ/mol; Eb(N≡O) = 631 kJ/mol;
Nhiệt tạo thành 1 mol HF:
432 + 159 – 2.565 = -539 kJ < 0
⇒ Phản ứng xảy ra.
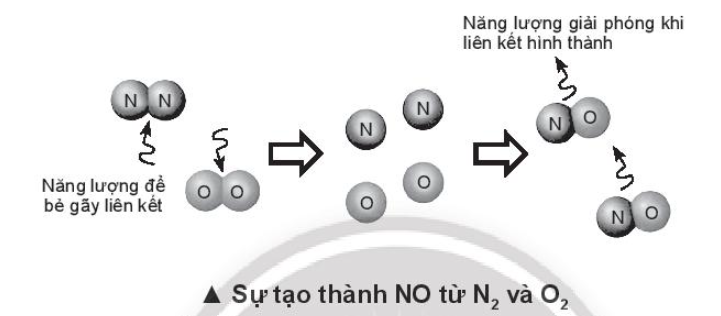
Nhiệt tạo thành 1 mol NO:
(NO) = 945 + 498 – 2.631 = +181 kJ > 0
⇒ Phản ứng không xảy ra
Xem thêm các bài giải sách bài tập Hóa học 10 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Bài 14.4 trang 56 SBT Hóa học 10. Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP)....
Bài 14.7 trang 57 SBT Hóa học 10. Kim loại nhôm có thể khử được oxide của nhiều nguyên tố...
Bài 14.8* trang 58 SBT Hóa học 10. Cho 3 hydrocarbon X, Y, Z đều có 2 nguyên tử C trong phân tử...
Bài 14.9 trang 58 SBT Hóa học 10. a) Phản ứng nào có thể tự xảy ra (sau giai đoạn khơi mào ban đầu)...
Bài 14.13 trang 59 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
Bài 14.14* trang 59 SBT Hóa học 10. Cho phản ứng phân hủy hydrazine. Tính theo năng lượng liên kết của phản ứng trên...
Bài 14.15 trang 59 SBT Hóa học 10. Quá trình hòa tan calcium chloride trong nước...
Xem thêm lời giải sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Soạn văn lớp 10 (ngắn nhất) – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Giải sbt Ngữ văn lớp 10 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Văn mẫu lớp 10 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 10 – Chân trời sáng tạo
- Giải sgk Toán 10 – Chân trời sáng tạo
- Giải Chuyên đề Toán 10 – Chân trời sáng tạo
- Lý thuyết Toán 10 – Chân trời sáng tạo
- Giải sbt Toán 10 – Chân trời sáng tạo
- Chuyên đề dạy thêm Toán 10 Chân trời sáng tạo (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Giải sbt Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 10 Friends Global đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 Friends Global
- Giải sgk Vật lí 10 – Chân trời sáng tạo
- Giải sbt Vật lí 10 – Chân trời sáng tạo
- Lý thuyết Vật lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Vật lí 10 – Chân trời sáng tạo
- Giải sgk Sinh học 10 – Chân trời sáng tạo
- Giải sbt Sinh học 10 – Chân trời sáng tạo
- Lý thuyết Sinh học 10 – Chân trời sáng tạo
- Giải Chuyên đề Sinh học 10 – Chân trời sáng tạo
- Giải sgk Lịch sử 10 – Chân trời sáng tạo
- Giải sbt Lịch sử 10 – Chân trời sáng tạo
- Giải Chuyên đề Lịch sử 10 – Chân trời sáng tạo
- Lý thuyết Lịch sử 10 – Chân trời sáng tạo
- Giải sgk Địa lí 10 – Chân trời sáng tạo
- Lý thuyết Địa Lí 10 - Chân trời sáng tạo
- Giải sbt Địa lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Địa lí 10 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải Chuyên đề Kinh tế và pháp luật 10 – Chân trời sáng tạo
- Lý thuyết KTPL 10 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 10 – Chân trời sáng tạo
