Sách bài tập Hóa học 10 Bài 13 (Chân trời sáng tạo): Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Với giải sách bài tập Hóa học 10 Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa học 10 Bài 13.
Giải sách bài tập Hóa học lớp 10 Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 13.1 trang 52 SBT Hóa học 10. Cho phương trình nhiệt hóa học của phản ứng:
2H2(g)+O2(g)→2H2O(l) ΔrHo298=−571,68kJ
C. không có sự thay đổi năng lượng
D. có sự hấp thụ nhiệt lượng từ môi trường xung quanh.
Lời giải:
Đáp án đúng là: B.
ΔrHo298=−571,68kJ<0
Phản ứng trên là phản ứng tỏa nhiệt.
Bài 13.2 trang 52 SBT Hóa học 10. Cho phương trình nhiệt hóa học của phản ứng
B. không có sự thay đổi năng lượng
D. có sự giải phóng nhiệt lượng ra môi trường
Lời giải:
Đáp án đúng là: A.
Phản ứng trên là phản ứng thu nhiệt.
Bài 13.3 trang 52 SBT Hóa học 10. Dựa vào phương trình nhiệt hóa học của phản ứng sau:
Lời giải:
Đáp án đúng là: C.
Theo phương trình nhiệt học, phản ứng phân hủy 1 mol CO2 thu được 1 mol CO và 0,5 mol O2 cần thu 280kJ nhiệt.
Vậy để phân hủy 2 mol CO2 thu được 2 mol CO và 1 mol O2 cần thu 280.2 = 560 kJ nhiệt.
Giá trị của phản ứng là +560 kJ.
Bài 13.4 trang 52 SBT Hóa học 10. Phương trình nhiệt hóa học:
Lượng nhiệt tỏa ra khi dùng 9 g H2(g) để tạo thành NH3(g) là
Lời giải:
Đáp án đúng là: B.
9 gam H2 tương đương với 4,5 mol.
Theo đề bài, phản ứng của 3 mol H2 thể khí với 1 mol N2 thể khí tạo 2 mol NH3 thể khí giải phóng 91,8 kJ nhiệt.
Vậy phản ứng của 9 gam H2 (tương đương với 4,5 mol) ở thể khí tạo thành NH3 ở thể khí giải phóng: nhiệt.
Bài 13.5 trang 53 SBT Hóa học 10. Điều kiện nào sau đây không phải là điều kiện chuẩn?
A. Áp suất 1 bar và nhiệt độ 25oC hay 298K.
B. Áp suất 1 bar và nhiệt độ 298K
C. Áp suất 1 bar và nhiệt độ 25oC
D. Áp suất 1 bar và nhiệt độ 25K
Lời giải:
Đáp án đúng là: D.
Chú ý: Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar (đối với chất khí), nồng độ 1 mol L-1 (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 298 K (25oC).
Bài 13.6 trang 53 SBT Hóa học 10. Dựa vào phương trình nhiệt hóa học của các phản ứng sau:
Lời giải:
Đáp án đúng là: D.
Phản ứng (2) và (4) có nên là phản ứng thu nhiệt.
Bài 13.7 trang 53 SBT Hóa học 10. Dựa vào phương trình nhiệt hóa học của phản ứng sau:
Lời giải:
Đáp án đúng là: A.
Do
Nên
Bài 13.8 trang 53 SBT Hóa học 10.
a) Enthalpy tạo thành của hợp chất là gì?
b) Biến thiên enthalpy tạo thành trong các phản ứng hóa học là gì?
c) Enthalpy tạo thành khác với enthalpy tạo thành chuẩn ở điểm nào?
d) Tại sao enthalpy tạo thành chuẩn của đơn chất lại bằng không?
Lời giải:
a) Enthalpy tạo thành của một chất là lượng nhiệt kèm theo phản ứng tạo thành 1 mol
chất đó từ các đơn chất bền.
b) Biến thiên enthalpy tạo thành trong các phản ứng hoá học là lượng nhiệt toả ra hay thu vào của một phản ứng hoá học ( được tính theo đơn vị kJ hoặc kcal).
c) Enthalpy tạo thành được đo trong điều kiện chuẩn được gọi là enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) và được kí hiệu là
d) Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành một mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn. Đơn chất bền nên không có sự biến đổi, enthalpy tạo thành bằng 0.
Bài 13.9 trang 53 SBT Hóa học 10. Các quá trình sau đây là tỏa nhiệt hay thu nhiệt?
c) Quá trình chạy của con người
e. Hòa tan KBr vào nước làm cho nước trở nên lạnh
g) Sulfuric acid đặc khi thêm vào nước làm cho nước nóng lên.
Lời giải:
a) Nước hoá rắn là quá trình toả nhiệt.
b) Sự tiêu hoá thức ăn là quá trình thu nhiệt.
c) Quá trình chạy của con người là quá trình toả nhiệt.
d) Khí CH4 đốt ở trong lò là quá trình toả nhiệt.
e) Hoà tan KBr vào nước làm cho nước trở nên lạnh là quá trình thu nhiệt.
g) Thêm sulfuric acid đặc vào nước, nước nóng lên là quá trình toả nhiệt.
Bài 13.10 trang 54 SBT Hóa học 10. Hãy nêu 1 phản ứng tỏa nhiệt và 1 phản ứng thu nhiệt mà em biết.
Lời giải:
- Cho kim loại iron (Fe) tác dụng với giấm (CH3COOH – acetic acid). Phương trình nhiệt hoá học:
⇒ Phản ứng toả nhiệt.
- Cho NaHCO3 tác dụng với acid. Phương trình nhiệt hoá học:
⇒ Phản ứng thu nhiệt.
Hãy dự đoán phản ứng trên là tỏa nhiệt hay thu nhiệt.
Lời giải:
Phản ứng nhiệt phân ammonium nitrate là phản ứng thu nhiệt do phải cung cấp nhiệt năng.
Lời giải:
Phản ứng có thì không tự xảy ra do cần phải được cung cấp nhiệt từ bên ngoài. Do vậy, nếu chỉ có hỗn hợp phản ứng mà không có nguồn nhiệt khác thì phản ứng không tự xảy ra.
Lời giải:
Các đơn chất C (graphite, s), Br2 (l), Na (s), Hg(l), bền có .
Lời giải:
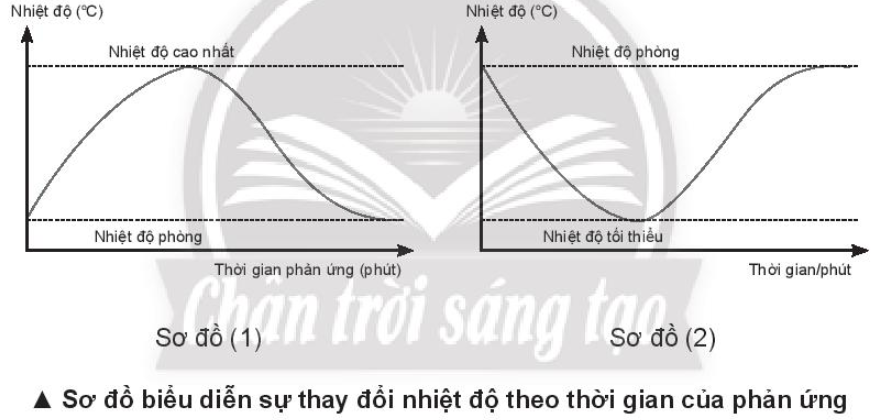
- Sơ đồ (1) chỉ quá trình toả nhiệt, do nhiệt độ phản ứng tăng so với nhiệt độ ban đầu (nhiệt độ phòng).
- Sơ đồ (2) chỉ quá trình thu nhiệt, do nhiệt độ phản ứng giảm so với nhiệt độ ban đầu (nhiệt độ phòng).
Lời giải:
Phương trình nhiệt hoá học của các phản ứng:
a. Phản ứng tạo thành Al2O3
b. Phản ứng tạo thành NO.
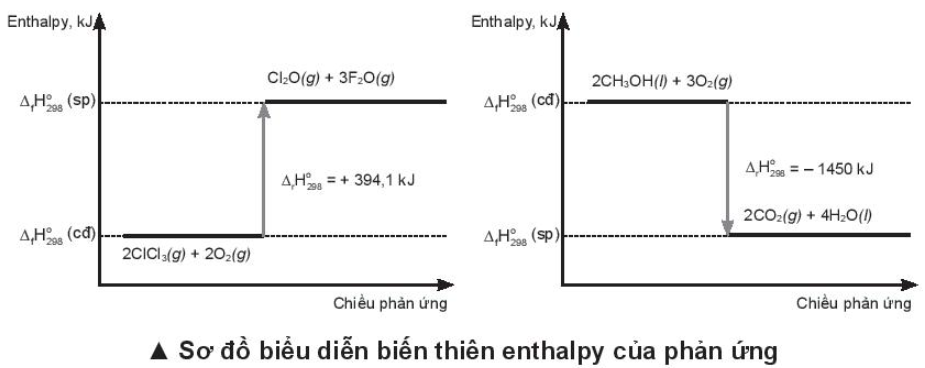
Lời giải:
Phương trình nhiệt hoá học ứng với sơ đồ:
Bài 13.17 trang 55 SBT Hóa học 10. Cho phản ứng:
a. Lấy gấp 3 lần khối lượng của các chất phản ứng.
b. Lấy một nửa khối lượng của các chất phản ứng
Lời giải:
a) Lấy gấp 3 lần khối lượng của các chất phản ứng:
b) Lấy một nửa khối lượng của các chất phản ứng:
c) Đảo chiều của phản ứng:
Lời giải:
Số mol N2: .
Để tạo 1 mol NH3 cần 0,5 mol N2.
Phương trình nhiệt hoá học:
a) Nước ở trạng thái khí, biết rằng khi tạo thành 1 mol hơi nước tỏa ra 214,6 kJ nhiệt.
b) Nước lỏng, biết rằng sự tạo thành 1 mol nước lỏng tỏa ra 285,49 kJ nhiệt.
c) Ammonia (NH3), biết rằng sự tạo thành 2,5 g ammonia tỏa ra 22,99 kJ nhiệt.
Lời giải:
a) Khi tạo thành 1 mol hơi nước tỏa ra 214,6 kJ nhiệt, phương trình nhiệt hóa học của quá trình là:
b) Sự tạo thành 1 mol nước lỏng tỏa ra 285,49 kJ nhiệt, phương trình nhiệt hóa học của quá trình là:
c) Sự tạo thành 2,5 g ammonia tỏa ra 22,99 kJ nhiệt:
Số mol ammonia =
Sự tạo thành 1 mol ammonia toả ra 156,33 kJ nhiệt.
Tạo thành 2 mol ammonia toả ra 156,33.2 = 312,66 kJ nhiệt.
Phương trình nhiệt hóa học của quá trình là:
d) Để thu được 11,2 g vôi (CaO) phải cung cấp 6,94 kcal:
Số mol vôi bằng 0,2 mol, vậy để thu được 1 mol vôi cần cung cấp 6,94.5 = 34,7 kcal.
Phương trình nhiệt hóa học của quá trình là:
Lời giải:
. Thứ tự giảm dần độ bền nhiệt là
Xem thêm lời giải sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Soạn văn lớp 10 (ngắn nhất) – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Giải sbt Ngữ văn lớp 10 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Văn mẫu lớp 10 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 10 – Chân trời sáng tạo
- Giải sgk Toán 10 – Chân trời sáng tạo
- Giải Chuyên đề Toán 10 – Chân trời sáng tạo
- Lý thuyết Toán 10 – Chân trời sáng tạo
- Giải sbt Toán 10 – Chân trời sáng tạo
- Chuyên đề dạy thêm Toán 10 Chân trời sáng tạo (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Giải sbt Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 10 Friends Global đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 Friends Global
- Giải sgk Vật lí 10 – Chân trời sáng tạo
- Giải sbt Vật lí 10 – Chân trời sáng tạo
- Lý thuyết Vật lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Vật lí 10 – Chân trời sáng tạo
- Giải sgk Sinh học 10 – Chân trời sáng tạo
- Giải sbt Sinh học 10 – Chân trời sáng tạo
- Lý thuyết Sinh học 10 – Chân trời sáng tạo
- Giải Chuyên đề Sinh học 10 – Chân trời sáng tạo
- Giải sgk Lịch sử 10 – Chân trời sáng tạo
- Giải sbt Lịch sử 10 – Chân trời sáng tạo
- Giải Chuyên đề Lịch sử 10 – Chân trời sáng tạo
- Lý thuyết Lịch sử 10 – Chân trời sáng tạo
- Giải sgk Địa lí 10 – Chân trời sáng tạo
- Lý thuyết Địa Lí 10 - Chân trời sáng tạo
- Giải sbt Địa lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Địa lí 10 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải Chuyên đề Kinh tế và pháp luật 10 – Chân trời sáng tạo
- Lý thuyết KTPL 10 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 10 – Chân trời sáng tạo
