Giải Hóa 11 Bài 6 (Kết nối tri thức): Một số hợp chất của nitrogen với oxygen
Với giải bài tập Hóa 11 Bài 6: Một số hợp chất của nitrogen với oxygen sách Kết nối tri thức hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa học 11 Bài 6.
Giải Hóa 11 Bài 6: Một số hợp chất của nitrogen với oxygen
Lời giải:
- Nước mưa thông thường có pH khoảng 5,6 chủ yếu do có carbon dioxide hoà tan tạo môi trường acid yếu. Khi nước mưa có pH nhỏ hơn 5,6 thì gọi là hiện tượng mưa acid.
- Hợp chất của nitrogen với oxygen là một trong các nguyên nhân gây nên hiện tượng mưa acid.
I. Các oxide của nitrogen
Lời giải:
- Nguyên nhân phát thải NOx từ hoạt động giao thông vận tải, nhà máy nhiệt điện, luyện kim, đốt nhiên liệu:
+ Nhiệt độ rất cao (trên 3 000 oC) hoặc tia lửa điện làm nitrogen trong không khí bị oxi hoá: N2 + O2 ⇌ 2NO.
+ Nitrogen trong nhiên liệu hoặc sinh khối kết hợp với oxygen trong không khí.
+ Nitrogen trong không khí tác dụng với các gốc tự do (gốc hydrocarbon, gốc hydroxyl, …)
- Một số biện pháp nhằm cắt giảm các nguồn phát thải NOx:
+ Giảm sử dụng phương tiện cá nhân như xe máy, ô tô; tăng cường sử dụng các phương tiện công cộng như xe bus…
+ Tăng cường sử dụng năng lượng tái tạo như thuỷ điện, địa nhiệt, năng lượng mặt trời, năng lượng gió …
+ Xử lí khí thải các nhà máy nhiệt điện, luyện kim, đốt nhiên liệu … trước khi thải ra môi trường.
Lời giải:
Một số hình ảnh về ảnh hưởng của mưa acid tới môi trường:
Một số giải pháp nhằm giảm thiểu nguy cơ gây mưa acid:

- Xử lí khí thải các nhà máy nhiệt điện, luyện kim, đốt nhiên liệu … trước khi thải ra môi trường.
- Tăng cường sử dụng năng lượng tái tạo như thuỷ điện, địa nhiệt, năng lượng mặt trời, năng lượng gió … thay cho năng lượng từ nhiên liệu hoá thạch.
- Kiểm soát chất lượng các phương tiện giao thông có động cơ, cấm sử dụng các phương tiện không đảm bảo chất lượng khí thải động cơ, phương tiện hết niên hạn sử dụng.
II. Nitric acid
Lời giải:
- Liên kết O – H phân cực mạnh về phía nguyên tử oxygen ⇒ nitric acid tan trong nước (là dung môi phân cực).
- Liên kết O – H phân cực mạnh về phía nguyên tử oxygen ⇒ nitric acid có khả năng cho proton, thể hiện tính acid. Ngoài ra, phân tử nitric acid chứa nguyên tử nitrogen có số oxi hoá cao nhất (+5) nên nitric acid có khả năng nhận electron, thể hiện tính oxi hoá mạnh.
Lời giải:
Phương trình phân li: HNO3 → H+ + NO3−.
Phương trình hoá học minh hoạ tính acid mạnh của HNO3:
CuO + 2HNO3 → Cu(NO3)2 + H2O
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O.
III. Hiện tượng phú dưỡng
Lời giải:
Một số biện pháp nhằm hạn chế hiện tượng phú dưỡng xảy ra ở các ao, hồ:
- Tạo điều kiện để nước trong ao, hồ được lưu thông.
- Xử lí nước thải trước khi cho chảy vào ao, hồ.
- Sử dụng phân bón đúng liều lượng, đúng cách, đúng thời điểm trong năm để hạn chế sự rửa trôi ion NO3−, PO43− từ nguồn phân bón dư thừa vào ao, hồ.
Lời giải:
Đặc điểm của ao, hồ có hiện tượng phú dưỡng: xuất hiện dày đặc tảo xanh trong nước; nguồn thuỷ sản trong ao hồ bị suy kiệt; xuất hiện mùi hôi thối khó chịu.
Một số biện pháp đề xuất để cải tạo ao, hồ có hiện tượng phú dưỡng:
- Sử dụng chế phẩm vi sinh để tăng vi sinh có lợi.
- Xử lí nước thải trước khi đổ vào ao hồ.
- Trồng một số thực vật thuỷ sinh phù hợp với môi trường phú dưỡng: bèo tây, ngổ trâu, cải xoong … Trồng thực vật thủy sinh cũng sẽ làm giảm mức độ dinh dưỡng trong nước ao, hồ và do đó không khuyến khích sự nhân lên của thực vật phù du.
- Nước ao, hồ nên được thay, càng nhiều càng tốt (nên dùng nước đã được xử lý trước khi cấp vào ao).
- Tảo phát triển mạnh trong nước thiếu oxygen. Do đó tăng cường oxygen ngay lập tức bằng việc lắp đặt thiết bị sục khí để khuấy trộn bề mặt ao và giúp giải phóng các loại khí như CO2. Điều này cũng cho phép nước hấp thụ nhiều oxygen hơn, trong thời gian ngắn sẽ giúp giảm sự hiện diện của tảo.
Lý thuyết Một số hợp chất của nitrogen với oxygen
I. Các oxide của nitrogen
1. Công thức, tên gọi
- Công thức chung: NOx.
|
Oxide |
N2O |
NO |
NO2 |
N2O4 |
|
Tên gọi |
Dinitrogen oxide |
Nitrogen monoxide |
Nitrogen dioxide |
Dinitrogen tetroxide |
2. Nguồn gốc phát sinh NOx trong không khí.
- Tự nhiên: Núi lửa phun trào, cháy rừng, mưa dông kèm sấm sét.
- Con người: do hoạt động của con người: giao thông vân tải, sản xuất công nghiệp, nông nghiệp…
Tác hại: Là nguyên nhân gây mưa acid, sương mù quang hóa, hiệu ứng nhà kính, thủng tầng ozon…
3. Mưa acid
- Mưa acid là hiện tượng nước mưa có pH nhỏ hơn 5,6.
- Tác nhân: SO2 và NOx.
- VD:
2SO2 + O2 + 2H2O → 2H2SO4
4NO2 + O2 + 2H2O → 4HNO3
- Tác hại: Gây ảnh hướng xấu đến môi trường, con người và sinh vật như: ăn mòn các công trình kiến trúc, xây dựng …
II. Nitric acid
1. Cấu tạo
- Nguyên tử N có số oxi hóa +5, số oxi hóa cao nhất của nitrogen.
- Liên kết O-H phân cực mạnh về phía nguyên tử oxygen.
- Liên kết N → O là liên kết cho nhận
2. Tính chất vật lí
- Nitric acid tinh khiết là chất lỏng, không màu, có khối lượng riêng D = 1,53 g/ml. Nitric acid bốc khói mạnh trong không khí ẩm và tan vô hạn trong nước.
3. Tính chất hóa học
a, Tính acid
- Thể hiện tính chất hóa học của một acid.
- Trong công nghiệp, sản xuất phân bón giàu dinh dưỡng như ammonium nitrat, calcium nitrate.
NH3 + HNO3 → NH4NO3
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
b, Tính oxi hóa
- Acid nitric có tính oxi hóa mạnh.
III. Hiện tượng phú dưỡng
- Nguyên nhân: Do sự dư thừa dinh dưỡng đã cung cấp nguồn thức ăn dồi dào cho sinh vật phù du phát triển rất mạnh.
- Tác hại: Gây cản trở sự hấp thụ ánh sáng mặt trời vào nước, làm giảm sự quang hợp của thực vật thủy sinh; tạo ra sự dư thừa dinh dưỡng.
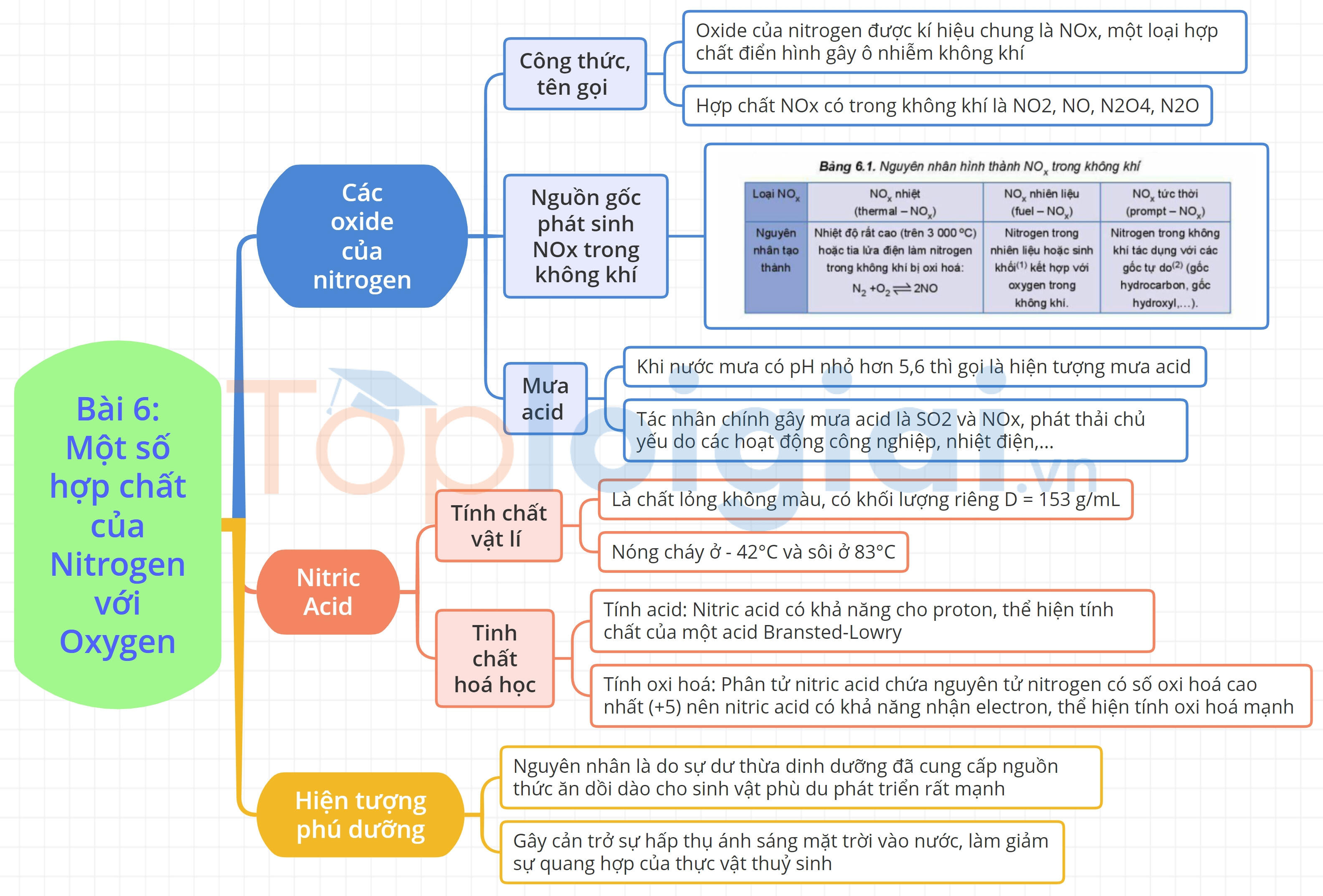
Sơ đồ tư duy Một số hợp chất của nitrogen với oxygen
Xem thêm lời giải bài tập Hóa học lớp 11 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Bài 7: Sulfur và sulfur dioxide
Bài 8: Sulfuric acid và muối sulfate
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Kết nối tri thức - hay nhất
- Văn mẫu lớp 11 - Kết nối tri thức
- Tóm tắt tác phẩm Ngữ văn 11 – Kết nối tri thức
- Tác giả tác phẩm Ngữ văn 11 - Kết nối tri thức
- Giải SBT Ngữ văn 11 – Kết nối tri thức
- Bố cục tác phẩm Ngữ văn 11 – Kết nối tri thức
- Giải Chuyên đề học tập Ngữ văn 11 – Kết nối tri thức
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Kết nối tri thức
- Soạn văn 11 Kết nối tri thức (ngắn nhất)
- Giải sgk Toán 11 – Kết nối tri thức
- Giải Chuyên đề học tập Toán 11 – Kết nối tri thức
- Lý thuyết Toán 11 - Kết nối tri thức
- Giải sbt Toán 11 – Kết nối tri thức
- Bài tập Tiếng Anh 11 Global success theo Unit có đáp án
- Giải sgk Tiếng Anh 11 – Global success
- Giải sbt Tiếng Anh 11 - Global Success
- Trọn bộ Từ vựng Tiếng Anh 11 Global success đầy đủ nhất
- Ngữ pháp Tiếng Anh 11 Global success
- Giải sgk Vật lí 11 – Kết nối tri thức
- Lý thuyết Vật lí 11 – Kết nối tri thức
- Giải sbt Vật lí 11 – Kết nối tri thức
- Giải Chuyên đề học tập Vật lí 11 – Kết nối tri thức
- Chuyên đề dạy thêm Vật lí 11 cả 3 sách (2024 có đáp án)
- Giải sgk Sinh học 11 – Kết nối tri thức
- Lý thuyết Sinh học 11 – Kết nối tri thức
- Giải Chuyên đề học tập Sinh học 11 – Kết nối tri thức
- Giải sbt Sinh học 11 – Kết nối tri thức
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Kết nối tri thức
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Kết nối tri thức
- Lý thuyết Kinh tế pháp luật 11 – Kết nối tri thức
- Giải sbt Kinh tế pháp luật 11 – Kết nối tri thức
- Giải sgk Lịch sử 11 – Kết nối tri thức
- Giải Chuyên đề học tập Lịch sử 11 – Kết nối tri thức
- Lý thuyết Lịch sử 11 - Kết nối tri thức
- Giải sbt Lịch sử 11 – Kết nối tri thức
- Giải sgk Địa lí 11 – Kết nối tri thức
- Giải Chuyên đề học tập Địa lí 11 – Kết nối tri thức
- Lý thuyết Địa lí 11 - Kết nối tri thức
- Giải sbt Địa lí 11 – Kết nối tri thức
- Giải sgk Công nghệ 11 – Kết nối tri thức
- Lý thuyết Công nghệ 11 - Kết nối tri thức
- Giải sbt Công nghệ 11 – Kết nối tri thức
- Giải sgk Tin học 11 – Kết nối tri thức
- Giải Chuyên đề học tập Tin học 11 – Kết nối tri thức
- Lý thuyết Tin học 11 - Kết nối tri thức
- Giải sbt Tin học 11 – Kết nối tri thức
- Giải sgk Giáo dục quốc phòng an ninh 11 – Kết nối tri thức
- Lý thuyết Giáo dục quốc phòng 11 – Kết nối tri thức
- Giải sbt Giáo dục quốc phòng 11 – Kết nối tri thức
- Giải sgk Hoạt động trải nghiệm 11 – Kết nối tri thức


