Tính denta r G 0 298 của các phản ứng sau và cho biết ở điều kiện chuẩn các phản ứng
Lời giải Luyện tập 3 trang 30 Chuyên đề Hóa 10 sách Chuyên đề Hóa học lớp 10 Cánh diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập.
Giải Chuyên đề Hóa 10 Cánh diều Bài 4: Entropy và biến thiên năng lượng tự do Gibbs
Luyện tập 3 trang 30 Chuyên đề Hóa 10: Tính ΔrG0298 của các phản ứng sau và cho biết ở điều kiện chuẩn các phản ứng có tự xảy ra hay không.
a) H2(g) + Cl2(g) → 2HCl(g)
ΔrH0298 = -184,6 kJ
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
ΔrH0298 = -890,3 kJ
c) 2Na(s) + O2(g) → Na2O2(s)
ΔrH0298 = -510,9 kJ
Trả lời:
a) H2(g) + Cl2(g) → 2HCl(g)
Ta có:
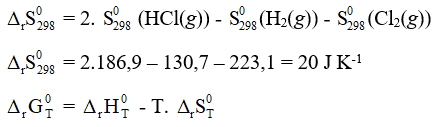
Ở điều kiện chuẩn T = 298 K
Ta có: ΔrG0298 = ΔrH0298 - 298. ΔrS0298 = -184,6.103 – 298.20 = -190560 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Ta có:
ΔrS0298 = S0298 (CO2(g)) + 2. S0298 (H2O(g)) - S0298 (CH4(g)) - 2. S0298 (O2(g))
ΔrS0298 = 213,8 + 2.188,7 – 186,3 – 2. 205,2 = -5,5 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: ΔrG0298 = ΔrH0298 - 298. ΔrS0298 = -890,3.103 – 298.(-5,5) = -888661 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
c) 2Na(s) + O2(g) → Na2O2(s)
Ta có:
ΔrS0298 = S0298(Na2O2(s)) - 2. S0298 (Na(s)) - S0298(O2(g))
ΔrS0298 = 95,0 – 2.51,3 – 205,2 = -212,8 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: ΔrG0298 = ΔrH0298 - 298. ΔrS0298 = -510,9.103 – 298.(-212,8) = -447485,6 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
Xem thêm lời giải bài tập Chuyên đề Hóa lớp 10 Cánh diều hay, chi tiết khác:
Mở đầu trang 28 Chuyên đề Hóa 10: Hình 4.1 mô tả trật tự sắp xếp của các phân tử nước ở ba thể: rắn, lỏng và khí...
Câu hỏi 1 trang 29 Chuyên đề Hóa 10: Khi đun nóng chảy tinh thể NaCl, độ mất trật tự của các ion tăng hay giảm...
Câu hỏi 2 trang 29 Chuyên đề Hóa 10: Tính biến thiên entropy chuẩn cho phản ứng đốt cháy 1 mol CH3OH(l) bằng O2(g)...
Luyện tập 1 trang 29 Chuyên đề Hóa 10: Tính ∆ của các phản ứng sau: a) 2Ca(s) + O2(g) → 2CaO(s)...
Luyện tập 2 trang 29 Chuyên đề Hóa 10: Tại sao của quá trình (1) lại dương...
Vận dụng 2 trang 31 Chuyên đề Hóa 10: Phản ứng (3) trong thực tế còn gọi là phản ứng gì...
Bài tập 2 trang 32 Chuyên đề Hóa 10: Hãy đánh giá khả năng tự xảy ra của phản ứng sau ở nhiệt độ chuẩn: 2Al(s) + 3H2O(l) → Al2O3(s) + 3H2(g)...
Bài tập 4 trang 33 Chuyên đề Hóa 10: Cho phản ứng: ZnCO3(s) → ZnO(s) + CO2(g)...
Bài tập 5 trang 33 Chuyên đề Hóa 10: Hãy xác định nhiệt độ thấp nhất để phản ứng nhiệt phân NaHCO3...
Xem thêm lời giải bài tập Chuyên đề Hóa lớp 10 Cánh diều hay, chi tiết khác:
Bài 1: Liên kết hóa học và hình học phân tử
Bài 3: Năng lượng hoạt hóa của phản ứng hóa học
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Cánh Diều
- Tác giả tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Bố cục tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Soạn văn lớp 10 (ngắn nhất) – Cánh Diều
- Giải sbt Ngữ văn lớp 10 – Cánh Diều
- Văn mẫu lớp 10 – Cánh Diều
- Giải Chuyên đề học tập Ngữ văn 10 – Cánh diều
- Giải sgk Toán 10 – Cánh Diều
- Giải Chuyên đề Toán 10 – Cánh Diều
- Lý thuyết Toán 10 – Cánh Diều
- Giải sbt Toán 10 – Cánh Diều
- Chuyên đề dạy thêm Toán 10 Cánh diều (2024 có đáp án)
- Giải sgk Tiếng Anh 10 – Explore new worlds
- Giải sgk Tiếng Anh 10 – ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 10 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 i-learn Smart World
- Giải sbt Tiếng Anh 10 - iLearn Smart World
- Giải sgk Vật lí 10 – Cánh Diều
- Giải sbt Vật lí 10 – Cánh Diều
- Lý thuyết Vật lí 10 – Cánh Diều
- Giải Chuyên đề Vật lí 10 – Cánh Diều
- Giải sgk Sinh học 10 – Cánh Diều
- Giải sbt Sinh học 10 – Cánh Diều
- Lý thuyết Sinh học 10 – Cánh Diều
- Giải Chuyên đề Sinh học 10 – Cánh diều
- Giải sgk Lịch sử 10 – Cánh Diều
- Giải sbt Lịch sử 10 – Cánh Diều
- Giải Chuyên đề Lịch sử 10 – Cánh Diều
- Lý thuyết Lịch sử 10 – Cánh diều
- Giải sgk Địa lí 10 – Cánh Diều
- Lý thuyết Địa Lí 10 – Cánh Diều
- Giải sbt Địa lí 10 – Cánh Diều
- Giải Chuyên đề Địa lí 10 – Cánh Diều
- Lý thuyết Công nghệ 10 – Cánh Diều
- Giải sgk Công nghệ 10 – Cánh Diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải Chuyên đề Kinh tế pháp luật 10 – Cánh diều
- Lý thuyết KTPL 10 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 10 – Cánh Diều
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Cánh diều
- Giải sbt Giáo dục quốc phòng - an ninh 10 – Cánh Diều
- Giải sgk Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sbt Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sgk Tin học 10 – Cánh Diều
- Giải sbt Tin học 10 – Cánh Diều
- Giải Chuyên đề Tin học 10 – Cánh diều
- Lý thuyết Tin học 10 - Cánh diều
- Giải sgk Giáo dục thể chất 10 – Cánh Diều
