Chuyên đề Hóa 10 Bài 4 (Cánh diều): Entropy và biến thiên năng lượng tự do Gibbs
Với giải bài tập Chuyên đề Hóa 10 Bài 4: Entropy và biến thiên năng lượng tự do Gibbs sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Chuyên đề học tập Hóa 10 CD Bài 4.
Giải bài tập Chuyên đề Hóa 10 Bài 4: Entropy và biến thiên năng lượng tự do Gibbs
Giải bài tập trang 28 Chuyên đề Hóa 10 Bài 4
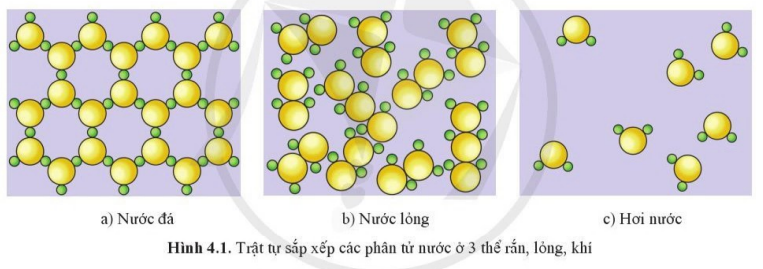
Trả lời:
Quan sát hình 4.1 xác định được: Mức độ “mất trật tự” của hệ tăng theo chiều từ nước đá tới hơi nước.
I. Entropy
Giải bài tập trang 29 Chuyên đề Hóa 10 Bài 4
Trả lời:
Khi đun nóng chảy tinh thể NaCl, độ mất trật tự của các ion tăng vì muối ăn đã chuyển từ trạng thái tinh thể sang trạng thái lỏng.
1. Ý nghĩa của entropy
2. Tính biến thiên entropy của một phản ứng hoặc một quá trình
Trả lời:
CH3OH(l) + O2(g) → CO2(g) + 2H2O(g)
∆r = (CO2(g)) + 2. (H2O(g)) - (CH3OH(l)) - .(O2(g))
∆r = 213,8 + 2.188,7 – 126,8 - .205,2 = 156,6 J K-1
Luyện tập 1 trang 29 Chuyên đề Hóa 10: Tính của các phản ứng sau:
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
Trả lời:
a) = 2. ( CaO(s)) - 2. (Ca(s)) - (O2(g))
= 2.38,1 – 2.41,6 – 205,2 = -212,2 J K-1
b) = (CO2(g)) + 2. (H2O(g)) - (CH4(g)) - 2. (O2(g))
= 213,8 + 2.188,7 – 186,3 – 2. 205,2 = -5,5 J K-1
c) = ( NH4Cl(s)) - (NH3(g)) - (HCl(g))
= 94,6 – 192,8 – 186,9 = -285,1 J K-1
Luyện tập 2 trang 29 Chuyên đề Hóa 10: Tại sao của quá trình (1) lại dương?
Trả lời:
Quá trình (1): H2O (l) → H2O (g)
Độ “mất trật tự” của phân tử hơi nước là lớn hơn các phân tử nước lỏng
⇒ Entropy của hơn nước (H2O(g)) lớn hơn entropy của nước lỏng (H2O(l))
⇒ của quá trình (1) dương.
II. Biến thiên năng lượng tự do Gibbs và khả năng xảy ra của phản ứng hóa học
Giải bài tập trang 30 Chuyên đề Hóa 10 Bài 4
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Trả lời:
a) H2(g) + Cl2(g) → 2HCl(g)
Ta có:
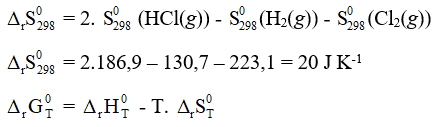
Ở điều kiện chuẩn T = 298 K
Ta có: = - 298. = -184,6.103 – 298.20 = -190560 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
b) CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Ta có:
= (CO2(g)) + 2. (H2O(g)) - (CH4(g)) - 2. (O2(g))
= 213,8 + 2.188,7 – 186,3 – 2. 205,2 = -5,5 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: = - 298. = -890,3.103 – 298.(-5,5) = -888661 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
c) 2Na(s) + O2(g) → Na2O2(s)
Ta có:
= (Na2O2(s)) - 2. (Na(s)) - (O2(g))
= 95,0 – 2.51,3 – 205,2 = -212,8 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: = - 298. = -510,9.103 – 298.(-212,8) = -447485,6 J < 0
Vậy ở điều kiện chuẩn phản ứng này tự xảy ra
Giải bài tập trang 31 Chuyên đề Hóa 10 Bài 4
Trả lời:
Phản ứng (2): 2NO (g) + O2 (g) → 2NO (g)
Trong phản ứng (2), = - 79 050 J có giá trị âm hơn = -75 300 J vì thế ở nhiệt độ thấp hơn thì phản ứng diễn ra thuận lợi hơn
Vận dụng 2 trang 31 Chuyên đề Hóa 10: Phản ứng (3) trong thực tế còn gọi là phản ứng gì?
Trả lời:
Phản ứng (3) trong thực tế còn gọi là phản ứng nung vôi.
Trả lời:
Mặc dù phản ứng (3) có thể xảy ra ở nhiệt độ 848oC, nhưng trong thực tế người ta thường nung nóng CaCO3 tới nhiệt độ 1 000oC vì ở nhiệt độ khoảng 1 000oC thì phản ứng xảy ra mãnh liệt làm tăng năng suất sản xuất vôi sống từ đá vôi.
Bài tập
Giải bài tập trang 32 Chuyên đề Hóa 10 Bài 4
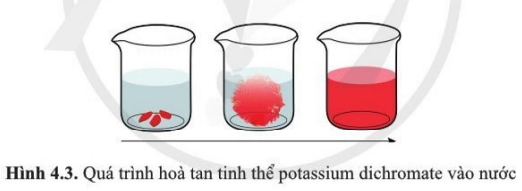
Trả lời:
Thả một vài tinh thể patassium dichromate K2Cr2O7 màu cam đỏ vào nước, tinh thể patassium dichromate (K2Cr2O7) tan trong nước ⇒ Độ mất trật tự của các ion trong tinh thể tăng ⇒ Entropy của quá trình hòa tan này tăng.
2Al(s) + 3H2O(l) → Al2O3(s) + 3H2(g)
Trả lời:
= (Al2O3(s)) + 3. (H2(g)) - 2. (Al(s)) - 3. (H2O(l))
= 50,9 + 3.130,7 – 2.28,3 – 3.70,0 = 176,4 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: = - 298. = -818,3.103 – 298.176,4 = -870867,2 J < 0
rất âm ở điều kiện chuẩn vì thế phản ứng này tự xảy ra.
Các đồ vật bằng nhôm được sử dụng rất phổ biến vì Al phản ứng dễ dàng với H2O ở điều kiện chuẩn để tạo thành lớp màng oxide Al2O3 bền vững. Lớp màng này bảo vệ cho nhôm kim loại chống lại các tác động ăn mòn của môi trường.
Trả lời:
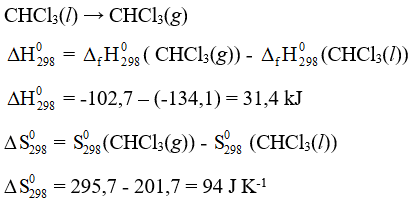
Ở điều kiện chuẩn T = 298 K, 1 bar
Ta có: = - 298. = 31,4.103 – 298.94 = 3388 J
Thực nghiệm T = 61,2 + 273 = 334,2 K
= - 334,2. = 31,4.103 – 334,2.94 = -14,8 J
Thực nghiệm đo được giá trị âm hơn giá trị .
Giải bài tập trang 33 Chuyên đề Hóa 10 Bài 4
Bài tập 4 trang 33 Chuyên đề Hóa 10: Cho phản ứng:
Ở điều kiện chuẩn, phản ứng có tự xảy ra tại các nhiệt độ sau hay không?
Trả lời:
a) Ở 25oC tức 298 K
= - 298. = 710.103 – 298.174,8 = 657909,6 J > 0
⇒ Phản ứng không tự xảy ra ở 25oC.
b) Ở 500oC tức (500 + 273) K = 773 K
= - 773. = 710.103 – 773.174,8 = 574879,6 > 0
⇒ Phản ứng không tự xảy ra ở 500oC
2NaHCO3(s) → Na2CO3(s) + H2O(l) + CO2(g)
Trả lời:
= (Na2CO3(s)) + (H2O(l)) + (CO2(g)) - 2.(NaHCO3(s))
= 135,0 + 70,0 + 213,8 – 2.101,7 = 215,4 J K-1
Để phản ứng diễn ra cần có
= - T. < 0
⇔ 9,16.103 – T.215,4 < 0
⇔ T > 42,53 K hay T > -230,47oC
Trả lời:
4Fe(s) + 3O2(g) → 2Fe2O3(s)
= 2.(Fe2O3(s)) - 3. (O2(g)) – 4. (Fe(s))
= 2.(-824,2) – 3.0 – 4.0 = -1648,4 kJ
= 2. (Fe2O3(s)) - 3.(O2(g)) – 4. (Fe(s))
= 2.87,4 – 3.205,2 – 4.27,3 = -550 J K-1
= - T. = -1648,4.103 – 298.(-550) = -1484500 J < 0
⇒ Ở điều kiện thường có thể tự xảy ra quá trình sắt bị biến đổi thành Fe2O3(s)
Trả lời:
Tại một nhiệt độ T:
Biến thiên năng lượng tự do Gibbs, ∆rG0 là tiêu chuẩn để đánh giá khả năng tự diễn biến của quá trình hoặc phản ứng hóa học ở nhiệt độ T và các yếu tố khác ở điều kiện chuẩn.
Vậy để dự đoán khả năng tự xảy ra phản ứng cần sử dụng và .
Xem thêm lời giải bài tập Chuyên đề Hóa lớp 10 Cánh diều hay, chi tiết khác:
Bài 1: Liên kết hóa học và hình học phân tử
Bài 3: Năng lượng hoạt hóa của phản ứng hóa học
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Cánh Diều
- Tác giả tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Bố cục tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Soạn văn lớp 10 (ngắn nhất) – Cánh Diều
- Giải sbt Ngữ văn lớp 10 – Cánh Diều
- Văn mẫu lớp 10 – Cánh Diều
- Giải Chuyên đề học tập Ngữ văn 10 – Cánh diều
- Giải sgk Toán 10 – Cánh Diều
- Giải Chuyên đề Toán 10 – Cánh Diều
- Lý thuyết Toán 10 – Cánh Diều
- Giải sbt Toán 10 – Cánh Diều
- Chuyên đề dạy thêm Toán 10 Cánh diều (2024 có đáp án)
- Giải sgk Tiếng Anh 10 – Explore new worlds
- Giải sgk Tiếng Anh 10 – ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 10 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 i-learn Smart World
- Giải sbt Tiếng Anh 10 - iLearn Smart World
- Giải sgk Vật lí 10 – Cánh Diều
- Giải sbt Vật lí 10 – Cánh Diều
- Lý thuyết Vật lí 10 – Cánh Diều
- Giải Chuyên đề Vật lí 10 – Cánh Diều
- Giải sgk Sinh học 10 – Cánh Diều
- Giải sbt Sinh học 10 – Cánh Diều
- Lý thuyết Sinh học 10 – Cánh Diều
- Giải Chuyên đề Sinh học 10 – Cánh diều
- Giải sgk Lịch sử 10 – Cánh Diều
- Giải sbt Lịch sử 10 – Cánh Diều
- Giải Chuyên đề Lịch sử 10 – Cánh Diều
- Lý thuyết Lịch sử 10 – Cánh diều
- Giải sgk Địa lí 10 – Cánh Diều
- Lý thuyết Địa Lí 10 – Cánh Diều
- Giải sbt Địa lí 10 – Cánh Diều
- Giải Chuyên đề Địa lí 10 – Cánh Diều
- Lý thuyết Công nghệ 10 – Cánh Diều
- Giải sgk Công nghệ 10 – Cánh Diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải Chuyên đề Kinh tế pháp luật 10 – Cánh diều
- Lý thuyết KTPL 10 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 10 – Cánh Diều
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Cánh diều
- Giải sbt Giáo dục quốc phòng - an ninh 10 – Cánh Diều
- Giải sgk Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sbt Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sgk Tin học 10 – Cánh Diều
- Giải sbt Tin học 10 – Cánh Diều
- Giải Chuyên đề Tin học 10 – Cánh diều
- Lý thuyết Tin học 10 - Cánh diều
- Giải sgk Giáo dục thể chất 10 – Cánh Diều
