Trắc nghiệm Luyện tập điều chế kim loại và sự ăn mòn kim loại (có đáp án)
Trắc nghiệm Hóa học 12 Bài 23: Luyện tập điều chế kim loại và sự ăn mòn kim loại
-
290 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Ở cực âm (catot):
2H2O + 2e 2OH- + H2
Ở cực dương (anot):
2Br- Br2 + 2e
Câu 2:
19/07/2024Một học sinh đã đưa ra các phương án điều chế kim loại Mg như sau:
(1) Kết tủa Mg(OH)2 từ dung dịch MgCl2, nhiệt phân lấy MgO rồi khử bằng H2 ở nhiệt độ cao để điều chế Mg.
(2) Dùng kim loại mạnh đẩy Mg ra khỏi dung dịch MgCl2.
(3) Điện phân dung dịch MgCl2 để thu được Mg.
(4) Cô cạn dung dịch MgCl2, điện phân nóng chảy để thu được Mg.
Trong các phương án trên có bao nhiêu phương án có thể áp dụng để điều chế Mg?
 Xem đáp án
Xem đáp án
Đáp án A
Mg là kim loại hoạt động mạnh nên được điều chế bằng cách điện phân các hợp chất nóng chảy của kim loại.
→ Phương án (4) thỏa mãn.
Câu 3:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Zn bị ăn mòn điện hóa
→ Zn có tính khử mạnh hơn
→ 2 hợp kim Fe–Zn (2); Zn–Cu (3) thỏa mãn
Câu 4:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Cho hỗn hợp kim loại phản ứng vơi Fe(NO3)3:
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
Cu + 2Fe(NO3)3 → 2Fe(NO3)2 + Cu(NO3)2
→ Loại bỏ được tạp chất mà không làm ảnh hưởng đến khối lượng Ag.
Câu 5:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Dùng kim loại có tính khử mạnh hơn Fe để tạo thành một pin điện hóa. Khi đó kim loại này bị ăn mòn điện hóa, Fe được bảo vệ.
Dùng Zn làm điện cực bảo vệ. Na có tính khử quá mạnh nên không thể dùng làm điện cực bảo vệ.
Câu 6:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Cho CO dư qua hỗn hợp X thu được chất rắn Y gồm: Al2O3; MgO; Fe; Cu (vì CO chỉ khử được những oxit của kim loại đứng sau Al trong dãy hoạt động hóa học).
Cho Y vào NaOH dư, Al2O3 tan hết, phần không tan Z gồm: MgO; Fe; Cu.
Câu 7:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Sợi dây kẽm tiếp xúc với thanh thép để ngoài không khí xảy ra hiện tượng ăn mòn điện hóa. Trong đó kim loại kẽm có tính khử mạnh hơn bị ăn mòn.
Câu 8:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp điện hóa: dùng kim loại mạnh hơn để bảo vệ kim loại yếu hơn.
Gắn các lá thép lên vỏ tàu vì Zn có tính khử mạnh hơn Fe (vỏ tàu) đóng vai trò là cực âm (kim loại bị ăn mòn thay sắt), nhưng tốc độ ăn mòn của kẽm tương đối nhỏ và giá thành không quá cao → vỏ tàu được bảo vệ trong thời gian dài.
Câu 9:
21/07/2024Sơ đồ sau đây mô tả cách điều chế kim loại M :
![]()
Trong số các kim loại Mg, Al, Fe, Ni, Cu, Ag, có bao nhiêu kim loại có thể áp dụng sơ đồ điều chế trên ?
 Xem đáp án
Xem đáp án
Đáp án C
Kim loại có tính khử trung bình, yếu (đứng sau Al trong dãy hoạt động hóa học) có thể điều chế bằng phương pháp điện phân dung dịch.
Các kim loại thỏa mãn gồm: Fe, Ni, Cu, Ag
Câu 10:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Na+ và Al3+ không bị khử, H+ bị khử
Quá trình đầu tiên xảy ra ở catot là khử H+
Câu 11:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Kim loại kiềm được điều chế bằng cách điện phân nóng chảy muối halogen hoặc hiđroxit của chúng.
Câu 12:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Giá trị pH tăng → sinh ra OH- → nước điện phân ở catot (-)
→ ion kim loại không bị khử
→ KCl thỏa mãn
Catot (-): 2H2O + 2e → H2 + 2OH-
Anot (+): 2Cl- → Cl2 + 2e
K2SO4 chỉ điện phân nước, giá trị pH không đổi.
Câu 13:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Fe + CuSO4 → FeSO4 + Cu
Thanh sắt có màu đỏ do kim loại Cu thoát ra bám vào. Dung dịch màu xanh lam của CuSO4 nhạt dần
Câu 14:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án A
mCu lý thuyết = 1,92 : 0,8 = 2,4 gam
Catot (-): Cu2+ → Cu + 2e
Theo định luật Faraday:
m =
→ 2,4 =
→ I = 3,75A
Câu 15:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Ta có = 4,48 : 22,4 = 0,2 mol
2RCl 2R + Cl2
= 0,4 mol
→ MRCl = 23,4 : 0,4 = 58,5 (g/mol)
→ MR = 58,5 – 35,5 = 23 (g/mol) (Na)
Câu 16:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Sắt tráng thiếc; sắt tráng niken; sắt tráng đồng thì sắt bị ăn mòn trước còn sắt tráng kẽm thì kẽm bị ăn mòn trước
Câu 17:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án C
= 0,004 <
mol
→ Ag+ điện phân hết, có cả nước bị điện phân.
→ mAg = 0,004.108 = 0,432g
Câu 18:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án B
nFe = 0,04 mol; = 0,01mol
Fe + Cu2+ Fe2+ + Cu
→ Fe dư. Cu2+ phản ứng hết
→ m = mCu + mFe dư
= 0,01.64 + (0,04 – 0,01).56 = 2,32 gam
Câu 19:
22/07/2024Cho các phát biểu sau:
(1) Các oxit của kim loại kiềm phản ứng với CO tạo thành kim loại.
(2) Các kim loại Ag, Fe, Cu và Mg đều được điều chế được bằng phương pháp điện phân dung dịch.
(3) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(4) Cho Cu vào dung dịch FeCl3 dư, thu được dung dịch chứa 3 muối.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
(1) Sai. Oxit của kim loại kiềm không bị khử bởi CO.
(1) Sai. Mg không điều chế được bằng phương pháp điện phân dung dịch.
(3) Sai. K không khử được ion Ag+ trong dung dịch thành Ag.
(4) Đúng. Cu + 2FeCl3 → CuCl2 + 2FeCl2
3 muối thu được là CuCl2, FeCl2 và FeCl3 dư.
Câu 20:
21/07/2024Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3.
(b) Nung FeS2 trong không khí
(c) Cho Mg (dư) vào dung dịch Fe2(SO4)3.
(d) Nhiệt phân Mg(NO3)2.
(e) Cho Fe vào dung dịch CuSO4 (dư)
(g) Cho Zn vào dung dịch FeCl3 (dư)
(h) Nung Ag2S trong không khí.
(i) Cho Ba vào dung dịch CuCl2 (dư)
Số thí nghiệm thu được kim loại sau khi các phản ứng kết thúc là:
 Xem đáp án
Xem đáp án
Đáp án A
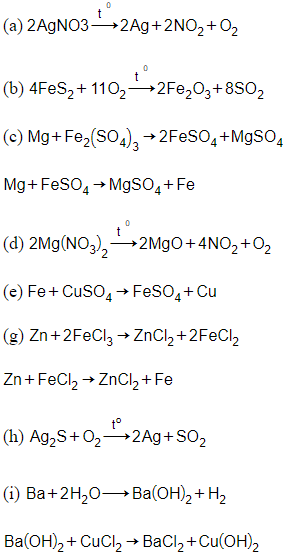
Câu 21:
23/07/2024 Xem đáp án
Xem đáp án
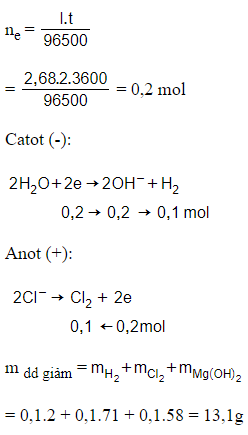
Đáp án D
Câu 22:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Anot (+):
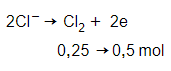
n e nhường = n e nhận = 0,5 mol
Catot (-):
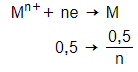
→ 16 = MM.
→ Chỉ có n = 2 và M = 64 phù hợp.
Vậy kim loại M là Cu
Câu 23:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án A
= 0,2.0,5 = 0,1 mol
= 0,2.0,3 = 0,06 mol
ne =
= < 2.
Cu2+ chưa bị điện phân hết.
Phản ứng điện phân:
Cu2+ + 2e Cu
Lượng kim loại thoát ra ở catot là:
mCu =
= . = 5,97 gam
Câu 24:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án D
X A1: BaO; Fe2O3; Al2O3; CuO; MgO
A1 dd B: Ba(OH)2, Ba(AlO2)2; C1: Fe2O3; CuO; MgO
C1 E: Fe, Cu, MgO
Câu 25:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
D. Sai vì trong sắt tây, Fe đóng vai trò là cực âm và bị ăn mòn trước.
Câu 26:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
CO có thể khử được các kim loại hoạt động trung bình, yếu (kim loại đứng sau Al trong dãy hoạt động hóa học
→ Kim loại Fe có thể được điều chế bằng cách dùng CO khử oxit kim loại tương ứng.
Câu 27:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
no trong FeO = nFeO
= = 0,1 mol
Sục hỗn hợp khí X gồm CO2 và CO dư và nước vôi trong dư
→ = 0,1 mol
→
Câu 28:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Nguyên tắc của phương pháp thủy luyện là dùng kim loại có tính khử mạnh hơn (không phản ứng với H2O) để khử ion kim loại trong dung dịch muối.
Phạm vi áp dụng: Điều chế kim loại có tính khử trung bình, yếu (kim loại đứng sau Al trong dãy hoạt động hóa học)
→ Nhóm các kim loại đều có thể điều chế bằng phương pháp thủy luyện là: Cu, Ag.
Câu 29:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Fe3O4 + 4H2 3Fe + 4H2O
Bảo toàn electron cho phản ứng hòa tan Fe vào HCl
2.nFe = 2.
→ nFe = 0,045 mol
Fe3O4 + 4H2 3Fe + 4H2O
= .nFe
= .0,045 = 0,06 mol
→ = 0,06.18 = 1,08 gam
Câu 30:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Ở anot xảy ra sự oxi hóa nước:
2H2O 4H+ + O2 + 4e
= 0,01 mol
→ ne = 0,04 mol
Mà ne =
→ 0,04 =
→ t = 386 giây = 6 phút 26 giây
Có thể bạn quan tâm
- Trắc nghiệm Luyện tập điều chế kim loại và sự ăn mòn kim loại (có đáp án) (289 lượt thi)
- 15 Câu trắc nghiệm luyện tập điều chế kim loại và sự ăn mòn kim loại có đáp án (190 lượt thi)
- Trắc nghiệm Luyện tập: Điều chế kim loại và sự ăn mòn kim loại có đáp án (Nhận biết) (198 lượt thi)
- Trắc nghiệm Luyện tập: Điều chế kim loại và sự ăn mòn kim loại có đáp án (Thông hiểu) (176 lượt thi)
- Trắc nghiệm Luyện tập: Điều chế kim loại và sự ăn mòn kim loại có đáp án (Vận dụng) (204 lượt thi)
Các bài thi hot trong chương
- 80 câu trắc nghiệm Đại cương về kim loại cơ bản (1168 lượt thi)
- 100 câu trắc nghiệm Đại cương về kim loại nâng cao (885 lượt thi)
- Trắc nghiệm Điều chế kim loại (có đáp án) (766 lượt thi)
- Trắc nghiệm Ăn mòn kim loại (có đáp án) (561 lượt thi)
- Trắc nghiệm Luyện tập tính chất của kim loại (có đáp án) (409 lượt thi)
- Trắc nghiệm Tính chất của kim loại, dãy điện hóa kim loại (có đáp án) (379 lượt thi)
- Trắc nghiệm Hợp kim (có đáp án) (375 lượt thi)
- Trắc nghiệm Tính chất của kim loại. Dãy điện hóa của kim loại có đáp án (Thông hiểu) (368 lượt thi)
- Trắc nghiệm Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại (có đáp án) (362 lượt thi)
- Trắc nghiệm Luyện tập: Tính chất của kim loại có đáp án (Thông hiểu) (312 lượt thi)
