Nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố nhóm VA, VIA và VIIA
Lời giải Bài 11.14* trang 41 SBT Hóa học 10 sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập Hóa học 10.
Giải SBT Hóa học 10 Chân trời sáng tạo Bài 11: Liên kết hydrogen và tương tác van der Waals
Bài 11.14* trang 41 SBT Hóa học 10: Nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố nhóm VA, VIA và VIIA được biểu diễn qua đồ thị sau:
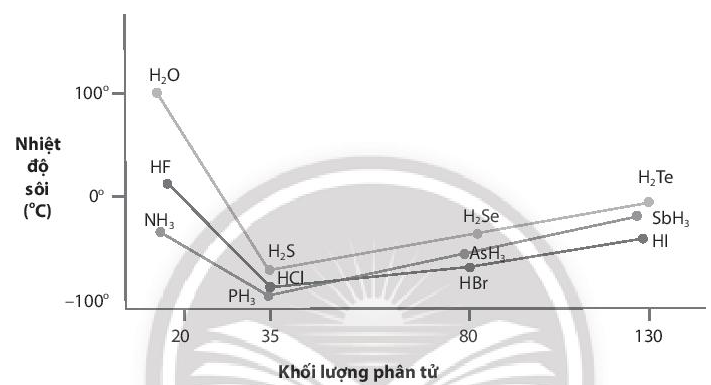
a. Giải thích nhiệt độ sôi cao bất thường của các hợp chất với hydrogen của các nguyên tố đầu tiên trong mỗi nhóm.
b. Nhận xét nhiệt độ sôi của các hợp chất với hydrogen của các nguyên tố còn lại ở mỗi nhóm và giải thích nguyên nhân sự biến đổi nhiệt độ sôi của chúng.
Lời giải:
a) Các nguyên tố đầu tiên trong mỗi nhóm VA, VIA, VIIA (N, O, F) có kích thước nhỏ và độ âm điện lớn, kết quả trong các hợp chất NH3; H2O; HF xuất hiện liên kết hydrogen liên phân tử làm cho các hợp chất này có nhiệt độ sôi cao bất thường so với các hợp chất còn lại trong mỗi nhóm.
b) Hợp chất với hydrogen của các nguyên tố còn lại trong mỗi nhóm có nhiệt độ sôi tăng dần khi khối lượng phân tử của chúng tăng. Vì khi khối lượng phân tử tăng, tương tác van der Waals giữa các phân tử trong hợp chất cũng tăng dẫn đến nhiệt độ sôi của chúng dần cao hơn.
Xem thêm các bài giải sách bài tập Hóa học 10 bộ sách Chân trời sáng tạo hay, chi tiết khác:
Bài 11.1 trang 39 SBT Hóa học 10: Hợp chất nào sau đây tạo được liên kết hydrogen liên phân tử...
Bài 11.4 trang 39 SBT Hóa học 10: Điều nào sau đây đúng khi nói về liên kết hydrogen liên phân tử...
Bài 11.5 trang 40 SBT Hóa học 10: Điều nào sau đây đúng khi nói về liên kết hydrogen nội phân tử...
Bài 11.7 trang 40 SBT Hóa học 10: Trong các khí hiếm sau, khí hiếm có nhiệt độ sôi cao nhất là...
Bài 11.8 trang 40 SBT Hóa học 10: Biểu diễn liên kết hydrogen giữa các phân tử sau...
Bài 11.10 trang 40 SBT Hóa học 10: Hãy so sánh tương tác van der Waals với liên kết ion...
Xem thêm lời giải sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Chân trời sáng tạo
- Tác giả tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Soạn văn lớp 10 (ngắn nhất) – Chân trời sáng tạo
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Giải sbt Ngữ văn lớp 10 – Chân trời sáng tạo
- Bố cục tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Chân trời sáng tạo
- Văn mẫu lớp 10 – Chân trời sáng tạo
- Giải Chuyên đề học tập Ngữ văn 10 – Chân trời sáng tạo
- Giải sgk Toán 10 – Chân trời sáng tạo
- Giải Chuyên đề Toán 10 – Chân trời sáng tạo
- Lý thuyết Toán 10 – Chân trời sáng tạo
- Giải sbt Toán 10 – Chân trời sáng tạo
- Chuyên đề dạy thêm Toán 10 Chân trời sáng tạo (2024 có đáp án)
- Giải sgk Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Giải sbt Tiếng Anh 10 Friends Global – Chân trời sáng tạo
- Trọn bộ Từ vựng Tiếng Anh 10 Friends Global đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 Friends Global
- Giải sgk Vật lí 10 – Chân trời sáng tạo
- Giải sbt Vật lí 10 – Chân trời sáng tạo
- Lý thuyết Vật lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Vật lí 10 – Chân trời sáng tạo
- Giải sgk Sinh học 10 – Chân trời sáng tạo
- Giải sbt Sinh học 10 – Chân trời sáng tạo
- Lý thuyết Sinh học 10 – Chân trời sáng tạo
- Giải Chuyên đề Sinh học 10 – Chân trời sáng tạo
- Giải sgk Lịch sử 10 – Chân trời sáng tạo
- Giải sbt Lịch sử 10 – Chân trời sáng tạo
- Giải Chuyên đề Lịch sử 10 – Chân trời sáng tạo
- Lý thuyết Lịch sử 10 – Chân trời sáng tạo
- Giải sgk Địa lí 10 – Chân trời sáng tạo
- Lý thuyết Địa Lí 10 - Chân trời sáng tạo
- Giải sbt Địa lí 10 – Chân trời sáng tạo
- Giải Chuyên đề Địa lí 10 – Chân trời sáng tạo
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Chân trời sáng tạo
- Giải Chuyên đề Kinh tế và pháp luật 10 – Chân trời sáng tạo
- Lý thuyết KTPL 10 – Chân trời sáng tạo
- Giải sgk Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sbt Hoạt động trải nghiệm 10 – Chân trời sáng tạo
- Giải sgk Giáo dục thể chất 10 – Chân trời sáng tạo
