100 câu trắc nghiệm Nito - Photpho nâng cao
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 1)
-
2014 lượt thi
-
20 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
23/07/2024Cho 8,96 lít khí NH3 (ở đktc) đi qua bình đựng 40 gam CuO nung nóng thu được chất rắn X. Cho toàn bộ chất rắn X vào 800ml dung dịch HCl 1M, sau phản ứng hoàn toàn thì thấy số mol HCl giảm đi một nửa. Hiệu suất của phản ứng khử CuO bởi NH3 là:
 Xem đáp án
Xem đáp án
Đáp án A
2NH3+ 3CuO → N2+ 3Cu + 3H2O
nNH3= 0,4 mol, nCuO =0,5 mol
Do nên hiệu suất tính theo NH3
Đặt số mol NH3 phản ứng là x mol
2NH3+ 3CuO→ N2+ 3Cu + 3H2O
x 1,5x 1,5x mol
Chất rắn X có chứa 0,5-1,5x mol CuO dư và 1,5x mol Cu
nHCl ban đầu= 0,8mol
CuO + 2HCl→ CuCl2+ H2O
Số mol HCl giảm đi một nửa → nHCl pứ= 0,8/2=0,4 mol
Theo PT: nHCl pứ= 2.nCuO= 2.(0,5-1,5x)=0,4
→ x= 0,2 mol
H=nNH3punNH3bd.100%=0,20,4.100%=50%
Câu 2:
22/07/2024Cho 4 lít N2 và 12 lít H2 vào bình kín để thực hiện phản ứng tổng hợp NH3. Biết hiệu suất phản ứng là 25%, hỗn hợp thu được sau phản ứng có thể tích là bao nhiêu (các thể tích khí đo trong cùng điều kiện)?
 Xem đáp án
Xem đáp án
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do hiệu suất phản ứng là 25% nên
VN2 pứ= 4.25%= 1 lít; VH2 pứ= 12.25%= 3 lít;
VNH3 sinh ra= 2VN2 pứ= 2 lít
VN2 dư= 4-1=3 lít, VH2 dư= 12-3=9 lít
Hỗn hợp thu được sau phản ứng có thể tích là
V= VN2 dư+ VH2 dư+ VNH3 sinh ra= 3 +9+2=14 lít
Đáp án B
Câu 3:
18/07/2024Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25%?
 Xem đáp án
Xem đáp án
Chọn đáp án D
N2+ 3H2
Theo phương trình:
H% = 25% → Thể thích N2 và H2 thực tế cần dùng là:
Câu 4:
21/07/2024Cho 25 lít N2 và 60 lít H2 vào bình phản ứng, hỗn hợp thu được sau phản ứng có thể tích bằng 75 lít (thể tích các khí đo ở cùng điều kiện). Hiệu suất phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án B.
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do →Hiệu suất tính theo H2
Đặt thể tích H2 phản ứng là x lít
→VN2 pứ= x/3 lít, VNH3 sinh ra=2x/3 lít
VN2 dư= 25-x/3 (lít), VH2 dư= 60- x(lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 60-x+ 25-x/3+ 2x/3= 75
→ x=15 lít
Câu 5:
21/07/2024Một hỗn hợp gồm 8 mol N2 và 16 mol H2 được nạp vào một bình kín có dung tích 4 lít và giữ ở nhiệt độ không đổi. Khi phản ứng đạt trạng thái cân bằng thì áp suất bằng 9/10 áp suất ban đầu. Hiệu suất phản ứng là?
 Xem đáp án
Xem đáp án
Đáp án D.
N2+ 3H2 ⇌ 2NH3
Dựa vào công thức: PV=nRT
Ở nhiệt độ và thể tích không đổi (thể tích bình chứa luôn là 4 lít) và R là hằng số thì áp suất (P) tỉ lệ với số mol (n)
Theo đề áp suất sau bằng 9/10 áp suất ban đầu
→nkhí sau pứ= 9/10.nkhí ban đầu= 9/10. (8+16)= 21,6 mol
nNH3= nkhí trước pứ- nkhí sau pứ= (8+16)- 21,6= 2,4 mol
Câu 6:
23/07/2024Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác) thu được hỗn hợp khí Y có tỉ khối so với He bằng 2. Hiệu suất của phản ứng tổng hợp NH3 là?
 Xem đáp án
Xem đáp án
Giả sử ban đầu hỗn hợp có 1 mol trong đó có x mol N2 và y mol H2
Ta có x + y =1 mol (1)
Vậy x= 0,2, y=0,8 mol
Đặt số mol N2 phản ứng là a mol
N2+ 3H2 → 2NH3
Ban đầu 0,2 0,8 mol
Phản ứng a 3a 2a mol
Sau pứ (0,2-a) (0,8-3a) 2a mol
Số mol hỗn hợp sau: 1-2a
m hỗn hợp sau là 7,2 gam
Hiệu suất phản ứng tính theo chất hết là
Câu 7:
23/07/2024Cho hỗn hợp gồm N2, H2, NH3 đi qua dung dịch H2SO4 đặc, dư thì thấy thể tích khí còn lại một nửa. Thành phần % theo thể tích của NH3 trong hỗn hợp đầu là bao nhiêu?
 Xem đáp án
Xem đáp án
Cho hỗn hợp gồm N2, H2, NH3 đi qua dung dịch H2SO4 đặc, dư thì chỉ có NH3 phản ứng
2NH3+ H2SO4→ (NH4)2SO4
Sau phản ứng thể tích khí còn một nửa
→ %VNH3= 50%
Câu 8:
22/07/2024Cho 4 lít N2 và 14 lít H2 vào bình phản ứng, hỗn hợp thu được sau phản ứng có thể tích bằng 16,4 lít (các thể tích khí được đo trong cùng điều kiện). Hiệu suất phản ứng là bao nhiêu?
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Ở cùng điều kiện thì tỉ lệ về thể tích bằng tỉ lệ về số mol
Xét tỉ lệ:
→ Hiệu suất tính theo N2
Đặt thể tích N2 phản ứng là x lít
→ phản ứng = 3x lít,
sinh ra = 2x lít
dư = 4 - x lít,
dư = 14 - 3x lít
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
Vkhí = dư + dư + sinh ra
= 14 - 3x + 4 – x + 2x = 16,4 lít
→ x = 0,8 lít
→H% = .100%
= = 20%
Câu 9:
18/07/2024Điều chế NH3 từ hỗn hợp gồm N2 và H2 (tỉ lệ mol 1:3). Tỉ khối hỗn hợp trước so với hỗn hợp sau phản ứng là 0,6. Hiệu suất phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án A

Câu 10:
21/07/2024Trong một bình kín dung tích 56 lít chứa đầy N2 và H2 theo tỉ lệ thể tích 1:4 ở 00C và 200atm, có một ít bột xúc tác Ni. Nung nóng bình một thời gian, sau đó đưa về 00C thì áp suất trong bình giảm 10% so với áp suất ban đầu. Hiệu suất của phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án D.
Ban đầu: nhỗn hợp= PV/RT= 56.200/0,082.273= 500 mol
→nN2=100 mol, nH2= 400 mol
Sau khi phản ứng xảy ra đưa về 00C thì áp suất trong bình giảm 10% so với áp suất ban đầu
→Số mol khí cũng giảm 10%
→nkhí sau pứ= 500- 10%.500= 450 mol
Mà nkhí sau pứ= (100-x)+ (400-3x)+2x= 450
→x=25 mol
→H= (x/100).100%=25%
Câu 11:
17/07/2024Cho 5 lít N2 và 15 lít H2 vào một bình kín dung tích không đổi . Ở 00C, áp suất trong bình là P1 atm. Đun nóng bình một thời gian thấy có 20% N2 tham gia phản ứng, đưa bình về nhiệt độ ban đầu thấy áp suất trong bình lúc này là P2 atm. Tỉ lệ P1 và P2 là:
 Xem đáp án
Xem đáp án
Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì phản ứng vừa đủ nên hiệu suất phản ứng tính theo N2 hoặc H2
Giả sử ban đầu có 1 mol N2 và 3 mol H2, nkhí ban đầu= 4 mol
→nN2 pứ= 1.20%= 0,2 mol
N2+ 3H2 ⇌ 2NH3
Ban đầu 1 3 mol
Phản ứng 0,2 0,6 0,4 mol
Sau pứ 0,8 2,4 0,4 mol
nkhí sau pứ= 0,8 + 2,4 + 0,4= 3,6 mol
Trong cùng điều kiện nhiệt độ và thể tích thì tỉ lệ về số mol chính là tỉ lệ về áp suất
Câu 12:
22/07/2024Một bình kín có thể tích 0,5 lít chứa 0,5 mol H2 và 0,5 mol N2 ở nhiệt độ thích hợp, khi đạt tới trạng thái cân bằng có 0,2 mol NH3 được tạo thành. Hiệu suất của phản ứng là bao nhiêu?
 Xem đáp án
Xem đáp án
Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì nên hiệu suất tính theo H2
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3
Câu 13:
18/07/2024Một hỗn hợp khí X gồm N2 và H2 có tỉ khối so với hiđro là 4,9. Cho hỗn hợp đi qua xúc tác thích hợp, nung nóng được hỗn hợp mới Y có tỉ khối so với hiđro là 6,125. Hiệu suất tổng hợp NH3 là:
 Xem đáp án
Xem đáp án
Đáp án A.

Câu 14:
22/07/2024Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
 Xem đáp án
Xem đáp án
Đáp án C
Giả sử có 1 mol hỗn hợp đầu. Gọi x và y (mol) lần lượt là số mol của N₂ và H₂ trong 1 mol hỗn hợp đầu
Gọi n₁, P₁ và n₂, P₂ lần lượt là số mol hỗn hợp khí + áp suất trong bình ban đầu và lúc sau
⇒ n₁ = x + y = 1 (1)
Khi nhiệt độ không đổi
⇒ n₁ / n₂ = P₁ / P₂
Áp suất khí trong bình giảm 5% so với áp suất ban đầu ⇒ P₁ / P₂ = 20 / 19
⇒ n₁ / n₂ = 20 / 19 (2)
Số mol của nito đã phản ứng là 10% ⇒ N₂ pứ 0,1x mol
N₂ + 3H₂ → 2NH₃
Trước: x y 0
Pứ 0,1x 0,3x 0,2x
Sau: n N₂ = 0,9x ; n H₂ = y - 0,3x ; n NH₃ = 0,2x
⇒ n₂ = 0,9x + y - 0,3x + 0,2x
⇒ n₂ = 0,8x + y (3)
Từ (1) (2) & (3) ta có:
(x + y) / (0,8x + y) = 20 / 19
⇒ 3x - y = 0 (4)
Giải hệ (1) & (4) cho ta: x = 0,25 mol và y = 0,75 mol
Thành phần phần trăm về số mol của N₂ và H₂ trong hỗn hợp đầu là:
%N₂ = 25% và %H₂ = 75%
Câu 15:
17/07/2024Một bình kín dung tích không đổi chứa hỗn hợp cùng thể tích khí N2 và H2 ở 0oC, 100atm. Sau khi tiến hành tổng hợp NH3, đưa nhiệt độ bình về 0oC, áp suất mới của bình là 90atm. Hiệu suất phản ứng tổng hợp NH3 là:
 Xem đáp án
Xem đáp án
Đáp án D
Đặt nH2= nN2= a mol (ban đầu)
→ Tổng số mol khí ban đầu n1= a+a=2a (mol)
Do dư nên hiệu suất tính theo H2
Đặt nH2 pứ= x mol
N2 + 3H2 ⇌ 2NH3
Ban đầu a a mol
Phản ứng x/3 x 2x/3 mol
Sau pứ (a-x/3) (a-x) 2x/3 mol
Tổng số mol khí sau phản ứng n2= (a-x/3) + (a-x) + 2x/3= 2a- 2x/3 (mol)
Trong cùng điều kiện về nhiệt độ, tỉ lệ số mol bằng tỉ lệ áp suất
Câu 16:
22/07/2024Nung nóng 0,5 mol hỗn hợp X gồm H2, N2 trong bình kín có xúc tác thích hợp, sau một thời gian thu được hỗn hợp Y. Cho 1/2 hỗn hợp Y đi qua ống sứ đựng CuO dư, nung nóng thấy khối lượng chất rắn trong ống giảm nhiều nhất là 3,2 gam. Tỉ khối hơi của X so với H2 là:
 Xem đáp án
Xem đáp án
Đáp án C
Đặt số mol N2 , H2 ban đầu lần lượt là a, b mol. Ta có a+b= 0,5 (*1)
N2+ 3H2 ⇌ 2NH3 (1)
Ban đầu: a b mol
Phản ứng: x 3x 2x mol
Sau pứ: (a-x) (b-3x) 2x mol
1/2 hỗn hợp Y chứa (a-x)/2 mol N2, (b-3x)/2 mol H2, x mol NH3
Cho 1/2 hỗn hợp Y đi qua ống sứ đựng CuO dư, nung nóng
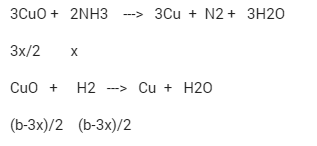
Khối lượng chất rắn trong ống giảm chính là khối lượng oxi trong oxit bị tách ra → mO tách= 3,2 gam
nO(tách)= nH2O= 3x/2+ (b-3x)/2= b/2 mol = 3,2/16
→ b=0,4 mol. Từ (*1) ta có a= 0,1 mol
Tỉ khối hơi của X so với H2 là: 7,2/2= 3,6
Câu 17:
17/07/2024Nung nóng hỗn hợp gồm 0,5 mol N2 và 1,5 mol H2 trong bình kín (có xúc tác) rồi đưa về nhiệt độ toC thấy áp suất trong bình lúc này là P1. Sau đó cho một lượng dư H2SO4 đặc vào bình (nhiệt độ lúc này trong bình là t0C) đến khi áp suất ổn định thì thấy áp suất trong bình lúc này là P2 (P1= 1,75P2). Hiệu suất tổng hợp NH3 là:
 Xem đáp án
Xem đáp án
Đáp án D
Ta có số mol khí ban đầu là
n = 0,5 + 1,5 = 2 (mol)
Vì có nên hiệu suất phản ứng tính theo N2 hoặc H2
Gọi x là số mol N2 phản ứng. Ta có:
N2 + 3H2 ⇌ 2NH3
x 3x 2x (mol)
Số mol N2 còn lại là: (0,5 - x) (mol)
Số mol H2 còn lại là: (1,5 - 3x) (mol)
Số mol NH3 sinh ra là: 2x (mol)
=> Số mol ở áp suất P1 là
n1 = (0,5 - x) + (1,5 - 3x) + 2x = (2 - 2x) (mol)
Áp dụng công thức n = PV/RT
Do phản ứng trong bình có thể tích V không đổi , sau phản ứng đưa về nhiệt độ t°C ban đầu nên:
P2/P1 = n2/n1 = số mol sau phản ứng / số mol trước phản ứng (*)
H2SO4 hấp thụ hoàn toàn NH3 theo PT:
2NH3+ H2SO4→ (NH4)2SO4
nên khí sau phản ứng chỉ có N2 và H2 với tổng số mol là:
n2 = (0,5 - x) + (1,5 - 3x) = 2 - 4x
Thay vào (*)
P2/P1 = (2 - 2x) / (0,2 - 4x)
=> P2 .(2 - 4x) = (2 - 2x)P1
Do P1=1,75P2
=> P2.(2 - 4x) = (2 - 2x).1,75P2
=> x = 0,3 (mol)
Hiệu suất phản ứng là:
H% = (0,3/0,5).100% = 60 %
Câu 18:
20/07/2024Muối amoni đicromat bị nhiệt phân theo phương trình:
(NH4)2Cr2O7 →Cr2O3+ N2+ 4H2O
Khi nhiệt phân 48 gam muối này thấy còn 30 gam hỗn hợp chất rắn và tạp chất không bị biến đổi. Phần trăm tạp chất trong muối là:
 Xem đáp án
Xem đáp án
Đáp án D
Đặt n(NH4)2Cr2O7= x mol
(NH4)2Cr2O7 →Cr2O3+ N2+ 4H2O
x x x 4x mol
Khối lượng chất rắn giảm chính là khối lượng N2 và H2O bay hơi
mchất rắn giảm= 28x+ 18.4x= 48-30 (gam)→ x=0,18 mol
→ m(NH4)2Cr2O7=252x=45,36 gam
Phần trăm tạp chất trong muối là:
Câu 19:
22/07/2024Có 2 dung dịch A, B . Mỗi dung dịch chỉ chứa 2 cation và 2 anion (không trùng lặp giữa các loại ion) trong số các ion sau: K+ (0,15 mol), H+ (0,2 mol), Mg2+ (0,1 mol), NH4+ (0,25 mol), Cl- (0,1 mol), SO42- (0,075 mol), NO3- (0,25 mol), CO32- (0,15 mol). Làm bay hơi (không xảy ra phản ứng hóa học) của 2 dung dịch A, B thì thu được chất rắn khan lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án C
Nhận thấy Mg2+ và H+ không thể tồn tại cùng với CO32-
→Dung dịch A chứa K+, NH4+, CO32- và ion âm An-
Theo định luật bảo toàn điện tích: 0,15+ 0,25=0,15.2+ n.nAn-
→ n.nAn-= 0,1 mol → Anion còn lại trong dung dịch A là Cl-
→Dung dịch A chứa K+, NH4+, CO32- và Cl-
→mchất rắn khan= 0,15.39 + 0,25.18+ 0,15.60 + 0,1.35,5= 22,9 gam
Dung dịch B chứa H+, Mg2+, SO42- và NO3-
Chú ý khi cô cạn thì axit HNO3 (0,2 mol) sẽ bay hơi cùng nước
→mchất rắn khan= mMg2++ mSO4(2-)+ mNO3- dư
= 0,1.24+ 96.0,075+ 0,05.62=12,7 gam
Câu 20:
17/07/2024Hòa tan 1,37 gam Ba vào 30 gam dung dịch (NH4)2SO4 5,38%. Sau khi phản ứng xảy ra hoàn toàn thấy khối lượng dung dịch sau phản ứng giảm m gam. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án B
nBa=0,01 mol, n(NH4)2SO4= 0,0122 mol
Ba+ H2O → Ba(OH)2+ H2↑ (1)
0,01 0,01 0,01 mol
Ba(OH)2+(NH4)2SO4 → BaS04↓ + 2NH3↑+ 2H2O(2)
0,01 0,0122 0,01 0,02
Ta có nBa(OH)2 < n(NH4)2SO4→ Ba(OH)2 hết
→ Tính theo Ba(OH)2
khối lượng dung dịch sau phản ứng giảm
mdd giảm= = mBaSO4+ mNH3+ mH2 - mBa
= (233. 0,01+ 0,02.17+0,01.2)- 1,37=1,32 gam
Bài thi liên quan
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 2)
-
20 câu hỏi
-
40 phút
-
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 3)
-
20 câu hỏi
-
40 phút
-
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 4)
-
20 câu hỏi
-
40 phút
-
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 5)
-
20 câu hỏi
-
40 phút
-
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 6)
-
25 câu hỏi
-
50 phút
-
-
100 câu trắc nghiệm Nito - Photpho nâng cao (Đề 7)
-
22 câu hỏi
-
50 phút
-
Có thể bạn quan tâm
- 100 câu trắc nghiệm Nito - Photpho cơ bản (1215 lượt thi)
- 100 câu trắc nghiệm Nito - Photpho nâng cao (2013 lượt thi)
Các bài thi hot trong chương
- Trắc nghiệm Amoniac và muối amoni có đáp án (Thông hiểu) (1311 lượt thi)
- Trắc nghiệm Nitơ (có đáp án) (647 lượt thi)
- Trắc nghiệm Amoniac và muối amoni có đáp án (Nhận biết) (586 lượt thi)
- Trắc nghiệm Axit nitric và muối nitrat có đáp án (Nhận biết) (555 lượt thi)
- Trắc nghiệm Phân bón hóa học (có đáp án) Hóa học lớp 11 (540 lượt thi)
- Trắc nghiệm Axit nitric và muối nitrat (có đáp án) (530 lượt thi)
- Trắc nghiệm Luyện tập: Tính chất hóa học của nitơ, photpho và hợp chất của chúng (có đáp án) (484 lượt thi)
- Trắc nghiệm Axit nitric và muối nitrat có đáp án (Vận dụng) (454 lượt thi)
- Trắc nghiệm Axit photphoric và muối photphat (có đáp án) (443 lượt thi)
- Trắc nghiệm Photpho (có đáp án) (430 lượt thi)
