TOP 15 Đề thi Giữa Học kì 2 Hoá học 9 năm 2024 có đáp án
Bộ 15 Đề thi Giữa Học kì 2 Hoá học lớp 9 năm 2024 có đáp án chi tiết giúp học sinh ôn luyện để đạt điểm cao trong bài thi Hóa học 9 Giữa học kì 2. Mời các bạn cùng đón xem:
Chỉ từ 270k mua trọn bộ Đề thi Giữa kì 2 Hóa học 9 bản word có lời giải chi tiết:
B1: Gửi phí vào tài khoản 0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây để thông báo và nhận tài liệu.
Xem thử tài liệu tại đây: Link tài liệu
Đề thi Giữa Học kì 2 Hoá học lớp 9 năm 2023 - 2024 có đáp án
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 1
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P =31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Ở điều kiện thường, phi kim có thể tồn tại ở trạng thái
A. lỏng và khí.
B. rắn và lỏng.
C. rắn và khí
D. rắn, lỏng, khí.
Câu 2: Đốt cháy hoàn toàn 2,8 gam hỗn hợp cacbon và lưu huỳnh cần 3,36 lít O2 (đktc). Khối lượng mỗi chất trong hỗn hợp lần lượt là
A. 0,2 gam và 0,8 gam.
B. 1,2 gam và 1,6 gam.
C. 1,3 gam và 1,5 gam.
D. 1,0 gam và 1,8 gam.
Câu 3: Nước clo là dung dịch hỗn hợp các chất
A. HCl; HClO; H2O.
B. HCl; HClO2; Cl2; H2O.
C. NaCl; NaClO.
D. HCl; HClO; Cl2; H2O.
Câu 4: Cho 11,2 gam bột sắt tác dụng với khí clo dư. Sau phản ứng thu được 32,5 gam muối sắt. Khối lượng khí clo tham gia phản ứng là
A. 21,3 gam.
B. 20,50 gam.
C. 10,55 gam
D. 10,65 gam.
Câu 5: Do có tính hấp phụ, nên cacbon vô định hình được dùng làm
A. điện cực, chất khử.
B. trắng đường, mặt nạ phòng hơi độc.
C. ruột bút chì, chất bôi trơn.
D. mũi khoan, dao cắt kính.
Câu 6: Cho 1 mol Ba(OH)2 phản ứng với 1 mol CO2. Muối tạo thành là
A. BaCO3.
B. Ba(HCO3)2.
C. BaCO3 và Ba(HCO3)2.
D. BaCO3 và Ba(OH)2 dư.
Câu 7: Dãy gồm các chất bị phân hủy bởi nhiệt là
A. Na2CO3, Mg(OH)2, Ca(HCO3)2, BaCO3.
B. MgCO3, BaCO3, Ca(HCO3)2, NaHCO3.
C. K2CO3, KOH, MgCO3, Ca(HCO3)2.
D. NaHCO3, KHCO3, Na2CO3, K2CO3.
Câu 8: Nhận định nào sau đây về tính chất của silic là sai?
A. Silic là phi kim hoạt động hóa học yếu hơn cacbon, clo.
B. Ở nhiệt độ cao, silic phản ứng với oxi tạo thành silic đioxit
C. Silic là chất rắn, màu xám.
D. Silic dẫn điện tốt nên được dùng làm pin mặt trời.
Câu 9: Dãy các kim loại nào sau đây được sắp xếp theo chiều tính kim loại tăng dần?
A. K, Na, Li, Rb.
B. Li, K, Rb, Na.
C. Na, Li, Rb, K.
D. Li, Na, K, Rb.
Câu 10: Nguyên tử của nguyên tố X có 3 lớp electron, lớp electron ngoài cùng có 7 electron. Vị trí và tính chất cơ bản của nguyên tố X là
A. thuộc chu kỳ 3, nhóm VII là kim loại mạnh.
B. thuộc chu kỳ 7, nhóm III là kim loại yếu.
C. thuộc chu kỳ 3, nhóm VII là phi kim mạnh.
D. thuộc chu kỳ 3, nhóm VII là phi kim yếu.
Câu 11: Nguyên tử cacbon có thể liên kết trực tiếp với nhau tạo thành các dạng mạch cacbon là
A. mạch vòng.
B. mạch thẳng, mạch nhánh.
C. mạch vòng, mạch thẳng, mạch nhánh.
D. mạch nhánh.
Câu 12: Phản ứng hóa học đặc trưng của metan là
A. phản ứng cộng.
B. phản ứng thế.
C. phản ứng tách.
D. phản ứng trùng hợp.
Câu 13: Đốt cháy hoàn toàn 5,6 lít khí etilen ở đktc cần dùng lượng oxi (ở đktc) là
A. 11,2 lít.
B. 16,8 lít.
C. 22,4 lít.
D. 33,6 lít.
Câu 14: Dãy các chất nào sau đây đều làm mất màu dung dịch brom?
A. CH4; C6H6.
B. CH4; C2H6.
C. CH4; C2H4.
D. C2H4; C2H2.
Câu 15: Phản ứng đặc trưng của benzen là
A. phản ứng cháy.
B. phản ứng trùng hợp.
C. phản ứng thế với brom (có bột sắt xúc tác).
D. phản ứng hóa hợp với brom (có bột sắt xúc tác).
Câu 16: Để dập tắt đám cháy nhỏ do xăng, dầu người ta dùng biện pháp
A. phun nước vào ngọn lửa.
B. phủ cát vào ngọn lửa.
C. thổi oxi vào ngọn lửa.
D. phun dung dịch muối ăn vào ngọn lửa.
Câu 17: Thành phần chủ yếu của khí thiên nhiên là
A. hiđro.
B. metan.
C. etilen.
D. axetilen.
Câu 18: Khí nào sau đây khi cháy không gây ô nhiễm môi trường?
A. CH4.
B. H2.
C. C4H10.
D. CO.
Câu 19: Thể tích khí oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 1 kg than có chứa 4% tạp chất không cháy là
A. 1,792 m3.
B. 4,48 m3.
C. 3,36 m3.
D. 6,72 m3.
Câu 20: Khí tham gia phản ứng trùng hợp là
A. CH4.
B. C2H4.
C. C3H8.
D. C2H6.
Câu 21: Trùng hợp 14 gam etilen (với hiệu suất 100 %) ở điều kiện thích hợp thì thu được khối lượng polietilen là
A. 7 gam.
B. 14 gam.
C. 28 gam.
D. 56 gam.
Câu 22: Từ bột Fe và một hoá chất X có thể điều chế trực tiếp được FeCl3. Vậy X là
A. Dung dịch HCl.
B. Dung dịch CuCl2.
C. Khí clo.
D. Cả A, B, C đều được.
Câu 23: Khối lượng C cần dùng để khử hoàn toàn 8 gam CuO thành kim loại là
A. 3,6 gam.
B. 1,2 gam.
C. 2,4 gam.
D. 0,6 gam.
Câu 24: Khí CO dùng làm chất đốt trong công nghiệp có lẫn tạp chất là CO2 và SO2. Có thể làm sạch CO bằng
A. CuSO4 khan.
B. H2SO4 đặc.
C. dung dịch BaCl2.
D. dung dịch nước vôi trong.
Câu 25: Nhận xét nào sau đây không đúng?
A. Hợp chất hữu cơ có ở xung quanh ta.
B. Hợp chất hữu cơ là hợp chất của cacbon.
C. Khi đốt cháy các hợp chất hữu cơ đều thấy tạo ra CO2.
D. Đốt cháy hợp chất hữu cơ luôn thu được CO2 và H2O.
Câu 26: Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của axetilen trong hỗn hợp ban đầu lần lượt là
A. 20%.
B. 70%.
C. 40%.
D. 60%.
Câu 27: Số liên kết đơn trong phân tử C4H10 là
A. 10.
B. 13.
C. 14.
D. 12.
Câu 28: Axetilen tham gia phản ứng cộng H2O (xúc tác H2SO4) thu được sản phẩm là
A. C2H5OH
B. CH3COOH
C. CH3CHO
D. C2H4(OH)2
Câu 29: Khử hoàn toàn 2,4 gam đồng (II) oxit bằng khí CO. Thể tích khí CO cần dùng (đktc) là
A. 0,224 lít
B. 0,672 lít
C. 0,448 lít
D. 0,560 lít
Câu 30: Tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen, biết hiệu suất phản ứng đạt 80%.
A. 7,80 gam
B. 8,80 gam
C. 9,75 gam
D. 10,08 gam
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI ĐỀ 1
|
1D |
2B |
3D |
4A |
5B |
6A |
7B |
8D |
9D |
10C |
|
11C |
12B |
13B |
14D |
15C |
16B |
17B |
18B |
19A |
20B |
|
21B |
22C |
23D |
24D |
25D |
26B |
27B |
28C |
29B |
30C |
Câu 1:
Đáp án D
Ở điều kiện thường phi kim tồn tại ở cả ba trạng thái:
- Rắn: lưu huỳnh, photpho, cacbon,…
- Lỏng: brom
- Khí: oxi, clo, hiđro, nitơ
Câu 2:
Đáp án B
= 0,15 mol
Theo bài ra ta có hệ phương trình:
⇒⇒
⇒ mC = 0,1.12 = 1,2 gam
mS = 0,05.32 = 1,6 gam
Câu 3:
Đáp án D
Clo phản ứng với nước theo phương trình:
Cl2 + H2O ⇄ HCl + HClO
Nước clo là dung dịch hỗn hợp các chất: HCl; HClO; Cl2; H2O.
Câu 4:
Đáp án A
Áp dụng định luật bảo toàn khối lượng:
mFe + = m muối sắt
⇒ = 32,5 – 11,2 = 21,3 gam
Câu 5:
Đáp án B
Cacbon vô định hình (than gỗ, than xương,…) có tính hấp phụ (giữ trên bề mặt của chúng các chất khí, chất hơi, chất tan trong dung dịch). Nhờ tính chất này mà cacbon vô định hình được dùng để làm trắng đường, chế tạo mặt nạ phòng độc.
Câu 6:
Đáp án A
Phản ứng theo tỉ lệ 1 : 1
Ba(OH)2 + CO2 → BaCO3 + H2O
Câu 7:
Đáp án B
Lưu ý: Muối cacbonat dễ bị phân hủy bởi nhiệt (trừ muối cacbonat trung hòa của kim loại kiềm)
Dãy gồm các chất bị phân hủy bởi nhiệt là: MgCO3, BaCO3, Ca(HCO3)2, NaHCO3.
Câu 8:
Đáp án D
Silic dẫn điện kém. Tinh thể silic tinh khiết là chất bán dẫn nên silic được dùng làm vật liệu bán dẫn trong kỹ thuật điện tử và chế tạo pin mặt trời.
Câu 9:
Đáp án D
Trong một nhóm A, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân tính kim loại của các nguyên tố tăng dần.
Trong nhóm IA, sắp xếp theo chiều tính kim loại tăng dần là: Li, Na, K, Rb
Câu 10:
Đáp án C
X có 3 lớp electron ⇒ thuộc chu kì 3
X có 7 electron lớp ngoài cùng ⇒ thuộc nhóm VII là phi kim mạnh.
Câu 11:
Đáp án C
Có ba dạng mạch cacbon là: mạch vòng, mạch thẳng, mạch nhánh.
Câu 12:
Đáp án B
Phản ứng hóa học đặc trưng của metan là phản ứng thế.
Metan không có phản ứng cộng, phản ứng tách và phản ứng trùng hợp.
Câu 13:
Đáp án B
Ta có: netilen =
⇒ = 0,75.22,4 = 16,8 lít
Câu 14:
Đáp án D
Etilen (C2H4) và axetilen (C2H2) đều làm mất màu dung dịch brom.
Metan (CH4) không làm mất màu dung dịch brom
Câu 15:
Đáp án C
Tính chất hóa học đặc trưng của benzen là dễ thế, khó cộng.
Benzen tham gia phản ứng thế với brom theo phương trình:
C6H6 + Br2 C6H5Br + HBr
Câu 16:
Đáp án B
Để dập tắt đám cháy nhỏ do xăng, dầu người ta dùng biện pháp: phủ cát vào ngọn lửa
Mục địch là để ngăn cách ngọn lửa với oxi trong không khí.
Câu 17:
Đáp án B
Thành phần chủ yếu của khí thiên nhiên là metan (CH4)
Câu 18:
Đáp án B
Khí H2 khi cháy không gây ô nhiễm môi trường
2H2 + O22H2O
Các khí còn lại cháy đều tạo CO2 là khí gây hiệu ứng nhà kính.
Câu 19:
Đáp án A
Khối lượng cacbon có trong 1kg than trên là:
mC = 1.= 0,96 kg = 960 gam
⇒ nC = = 80 mol
C + O2 CO2
Theo phương trình: = 80 mol
⇒ = 80.22,4 = 1792 lít = 1,792 m3
Câu 20:
Đáp án B
Khí tham gia phản ứng trùng hợp là etilen (C2H4)
nCH2=CH2 (-CH2-CH2-)n
Câu 21:
Đáp án B
nCH2=CH2 (-CH2-CH2-)n
Bảo toàn khối lượng có:
mtrước = msau
⇒ mpoli etilen = metilen = 14 gam.
Câu 22:
Đáp án C
X là khí clo (Cl2)
2Fe + 3Cl22FeCl3
Câu 23:
Đáp án D
nCuO = = 0,1 mol
2CuO + C 2Cu + CO2
Theo phương trình: nC = nCuO = 0,05 mol
→ mC = 0,05.12 = 0,6 gam.
Câu 24:
Đáp án D
Cho hỗn hợp khí qua lượng dư nước vôi trong; CO2 và SO2 phản ứng với nước vôi trong bị giữ lại; CO không phản ứng thoát ra khỏi dung dịch thu được CO tinh khiết.
CO2 + Ca(OH)2 (dư) → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 (dư) → CaSO3 ↓ + H2O
Câu 25:
Đáp án D
Nhận xét không đúng: Đốt cháy hợp chất hữu cơ luôn thu được CO2 và H2O.
Giải thích: Hợp chất hữu cơ chắc chắn có cacbon nên đốt cháy luôn thu được CO2. Hợp chất hữu cơ có thể không có H (ví dụ như: CCl4, NaOOC-COONa)
Câu 26
Đáp án B
phản ứng = = 0,035 mol
Cho hỗn hợp khí qua dung dịch brom dư chỉ có axetilen phản ứng
%Vaxetilen =
Câu 27:
Đáp án B
Có 13 liên kết đơn trong phân tử C4H10
.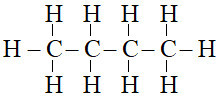
Câu 28:
Đáp án C
Phương trình phản ứng: C2H2 + H2O CH3CHO
Câu 29:
Đáp án B
Số mol CuO là: nCuO = 0,03 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: nCO = 0,03 mol
Thể tích khí CO cần dùng (đktc) là: VCO = 0,03.22,4 = 0,672 lít.
Câu 30:
Đáp án C
Số mol C6H5Br là: = 0,1 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,1 mol
Khối lượng benzen theo lý thuyết là: = 0,1.78 = 7,8 gam
Vì hiệu suất đạt 80% suy ra khối lượng benzen cần dùng là:
= =9,75 gam
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 2
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Chất nào tác dụng với khí oxi tạo thành oxit bazơ?
A. Photpho
B. Lưu huỳnh
C. Clo
D. Magie
Câu 2: Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là
A. H2SO3
B. HNO3
C. HCl đặc
D. H2SO4
Câu 3: Sục Cl2 vào nước, thu được nước clo màu vàng nhạt. Trong nước clo có chứa các chất là
A. Cl2, H2O
B. HCl, HClO
C. HCl, HClO, H2O
D. Cl2, HCl, HClO, H2O
Câu 4: Trong các dạng tồn tại của cacbon, dạng nào hoạt động hóa học mạnh nhất?
A. Tinh thể kim cương
B. Tinh thể than chì
C. Cacbon vô định hình
D. Các dạng đều hoạt động mạnh như nhau
Câu 5: Đốt cháy cacbon bởi O2, nếu dư thừa oxi thì sau phản ứng thu được khí nào?
A. CO2
B. O2
C. CO2 và CO dư
D. CO2 và O2 dư
Câu 6: Dạng thù hình của nguyên tố là
A. Các hợp chất khác nhau của một nguyên tố hóa học
B. Các đơn chất khác nhau do nguyên tố đó tạo nên
C. Các nguyên tố có hình dạng khác nhau
D. Các đơn chất có hình dạng khác nhau
Câu 7: Cho 19,5 gam kim loại M hóa trị II tác dụng với khí clo dư thì thu được 40,8 gam muối. Kim loại M là
A. Zn
B. Fe
C. Mg
D. Cu
Câu 8: Cho dung dịch NaOH 1M để tác dụng vừa đủ với 2,24 lít khí clo (đktc). Nồng độ mol của muối natri clorua thu được là
A. 2M
B. 1M
C. 0,5M
D. 1,5M
Câu 9: Khử hoàn toàn 6,4 gam Fe2O3 bằng khí CO dư. Sản phẩm khí thu được cho vào bình đựng nước vôi trong dư thu được m gam kết tủa màu trắng. Giá trị của m là
A. 10 gam
B. 11 gam
C. 12 gam
D. 14 gam
Câu 10: Sự tạo thành thạch nhũ trong các hang động của mỏ đá vôi là do có phản ứng:
A. CaCO3 + CO2 + H2O → Ca(HCO3)2.
B. Ca(OH)2 + Na2CO3 → CaCO3 + 2NaOH.
C. CaCO3 → CaO + H2O.
D. Ca(HCO3)2 → CaCO3 + CO2 + H2O.
Câu 11: Quá trình thổi khí CO2 vào dung dịch NaOH, muối tạo ra theo thứ tự là:
A. NaHCO3, Na2CO3
B. Na2CO3, NaHCO3
C. Na2CO3
D. Không đủ dữ liệu xác định
Câu 12: Nguyên tố phổ biến thứ hai ở vỏ trái đất là
A. oxi
B. cacbon
C. silic
D. sắt
Câu 13: Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo nguyên tắc:
A. Chiều nguyên tử khối tăng dần.
B. Chiều điện tích hạt nhân tăng dần.
C. Tính kim loại tăng dần.
D. Tính phi kim tăng dần.
Câu 14: Dãy nào sau đây thể hiện mức độ hoạt động hóa học của kim loại tăng dần:
A. Be, Fe, Ca, Cu.
B. Ca, K, Mg, Al.
C. Al, Zn, Co, Ca.
D. Ni, Mg, Li, Cs.
Câu 15: Dãy các chất sau là hiđrocacbon:
A. CH4, C2H2, C2H5Cl
B. C6H6, C3H4, HCHO
C. C2H2, C2H5OH, C6H12
D. C3H8, C3H4, C3H6
Câu 16: Hợp chất hữu cơ nào sau đây chỉ gồm liên kết đơn?
A. C3H8; C2H2.
B. C3H8; C4H10
C. C4H10; C2H2
D. C4H10; C6H6(benzen)
Câu 17: Chọn câu đúng trong các câu sau:
A. Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất có trong tự nhiên.
B. Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất của cacbon.
C. Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
D. Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các chất trong cơ thể sống.
Câu 18: Công thức đơn giản nhất của hợp chất hữu cơ A là CH2Cl. Biết MA = 99. Công thức phân tử của A là
A. CH2Cl2
B. C2H4Cl2
C. CHCl3
D. C2H2Cl3
Câu 19: Chọn câu đúng trong các câu sau:
A. Metan có nhiều trong khí quyển
B. Metan có nhiều trong mỏ khí, mỏ dầu, mỏ than
C. Metan có nhiều trong nước biển
D. Metan sinh ra trong quá trình thực vật bị phân hủy.
Câu 20: Những phát biểu nào sau đây không đúng?
1) Metan tác dụng với clo khi có ánh sáng.
2) Metan là chất khí, không màu, không mùi, nặng hơn không khí.
3) Metan cháy tỏa nhiều nhiệt nên được dùng làm nhiên liệu trong đời sống và trong sản xuất.
4) Hỗn hợp giữa metan và clo là hỗn hợp nổ.
5) Trong phân tử metan có bốn liên kết đơn C-H.
6) Metan tác dụng với clo ở điều kiện thường.
A. 1, 3, 5.
B. 1, 2, 6.
C. 2, 4, 6.
D. 2, 4, 5
Câu 21: Đốt cháy hoàn toàn 11,2 lít khí metan. Biết các thể tích khí đo ở điều kiện tiêu chuẩn. Thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành lần lượt là
A. 22,4 lít và 22,4 lít.
B. 11,2 lít và 22,4 lít.
C. 22,4 lít và 11,2 lít.
D. 11,2 lít và 22,4 lít.
Câu 22: Sản phẩm chủ yếu của một hợp chất hữu cơ khi cháy là
A. khí nitơ và hơi nước.
B. khí cacbonic và khí hiđro.
C. khí cacbonic và cacbon.
D. khí cacbonic và hơi nước.
Câu 23: Dẫn 5,6 lít (đktc) khí metan và etilen đi qua bình đựng dung dịch nước brom, đã làm mất màu hoàn toàn dung dịch có chứa 4 gam brom. Thể tích khí metan (đktc) trong hỗn hợp là
A. 0,56 lít.
B. 5,04 lít.
C. 0,28 lít.
D. 3,36 lít
Câu 24: Cho các hợp chất sau: CH4, C2H6, C2H4, H2. Có bao nhiêu chất tác dụng với dung dịch nước brom ở nhiệt độ thường?
A. 1
B. 2
C. 3
D. 4
Câu 25: Tính chất vật lí của etilen là
A. Chất lỏng, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
B. Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
C. Chất khí, không màu, không mùi, ít tan trong nước và nặng hơn không khí.
D. Chất khí, không màu, không mùi, tan tốt trong nước và nhẹ hơn không khí.
Câu 26: Liên kết C≡C trong phân tử axetilen có
A. một liên kết kém bền dễ đứt ra trong các phản ứng hóa học.
B. hai liên kết kém bền nhưng chỉ có một liên kết bị đứt ra trong phản ứng hóa học.
C. hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
D. ba liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 27: Khi đốt khí axetilen, số mol CO2 và H2O được tạo thành theo tỉ lệ là
A. 1 : 1.
B. 1 : 2
C. 1 : 3.
D. 2 : 1.
Câu 28: Tính chất nào không phải của benzen là
A. Dễ thế.
B. Khó cộng.
C. Bền với chất oxi hóa.
D. Kém bền với các chất oxi hóa.
Câu 29: Ở nông thôn có thể dùng phân gia súc, gia cầm, rác hữu cơ để ủ trong các hầm Bio-gas. Dưới ảnh hưởng của các vi sinh vật yếm khí, chất hữu cơ sẽ phân hủy tạo ra một loại phân bón chất lượng cao. Bio-gas dùng để đun nấu trong gia đình. Nên phát triển các hầm Bio-gas vì
A. Vốn đầu tư không lớn.
B. Đảm bảo vệ sinh môi trường và mầm các bệnh bị tiêu diệt
C. Có nguồn năng lượng sạch và thuận tiện.
D. Tất cả các lý do trên.
Câu 30: Phương pháp hiện đại để điều chế axetilen hiện nay là
A. Nhiệt phân metan ở nhiệt độ cao
B. Nhiệt phân canxi cacbua ở nhiệt độ cao
C. Nhiệt phân benzen ở nhiệt độ cao
D. Nhiệt phân etilen ở nhiệt độ cao
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI ĐỀ 2
|
1D |
2C |
3D |
4C |
5D |
6B |
7A |
8C |
9C |
10D |
|
11B |
12C |
13B |
14D |
15D |
16B |
17C |
18B |
19B |
20C |
|
21C |
22D |
23B |
24A |
25B |
26C |
27D |
28D |
29D |
30A |
Câu 1:
Đáp án D
Phương trình phản ứng:
2Mg + O2 2MgO
Câu 2:
Đáp án C
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là HCl đặc
MnO2(r) + 4HClđặc MnCl2 + Cl2(k) + 2H2O
Câu 3:
Đáp án D
Cl2 có phản ứng thuận nghịch với nước:
Vậy trong nước clo có chứa Cl2, HCl, HClO, H2O.
Câu 4:
Đáp án C
Trong các dạng tồn tại của cacbon, dạng hoạt động hóa học mạnh nhất là: Cacbon vô định hình.
Câu 5:
Đáp án D
Đốt cháy cacbon bởi O2, nếu dư thừa oxi thì sau phản ứng thu được hỗn hợp khí là
CO2 và O2 dư.
Câu 6:
Đáp án B
Dạng thù hình của một nguyên tố hóa học là những đơn chất khác nhau do nguyên tố đó tạo nên.
Câu 7:
Đáp án A
Phương trình phản ứng:
M + Cl2 → MCl2
Theo phương trình phản ứng ta có: nM =
Suy ra suy ra M = 65
Vậy M là Zn.
Câu 8:
Đáp án C
Số mol của Cl2 là: = 0,1mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: nNaOH = 0,2 mol
Suy ra VNaOH = = 0,2 lít
Nồng độ mol của NaCl là: CM = = 0,5M
Câu 9:
Đáp án C
Số mol của Fe2O3 là: = 0,04 mol
Phương trình phản ứng:
Số mol của CaCO3 là: = 0,12 mol
Vậy khối lượng CaCO3 là: m = 0,12.100 = 12 gam.
Câu 10:
Đáp án D
Thạch nhũ là CaCO3
Sự tạo thành thạch nhũ trong các hang động của mỏ đá vôi là do có phản ứng:
Ca(HCO3)2 → CaCO3 + CO2 + H2O
Câu 11:
Đáp án B
Ban đầu tạo muối NaCO3
CO2 + 2NaOH → Na2CO3 + H2O
Sau đó, CO2 dư tiếp tục xảy ra phản ứng:
CO2 + Na2CO3 + H2O → 2NaHCO3
Câu 12:
Đáp án C
Nguyên tố phổ biến thứ hai ở vỏ trái đất là silic
Câu 13:
Đáp án B
Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo chiều điện tích hạt nhân tăng dần.
Câu 14:
Đáp án D
Dãy thể hiện mức độ hoạt động hóa học của kim loại tăng dần là: Ni, Mg, Li, Cs.
Loại A vì Ca có tính kim loại mạnh hơn Cu.
Loại B vì Mg có tính kim loại mạnh hơn Al
Loại C vì Al có tính kim loại mạnh hơn Zn
Câu 15:
Đáp án D
+ Hi đrocacbon: Phân tử chỉ có hai nguyên tố cacbon và hiđro (CH4, C2H4, C6H6)
+ Dẫn xuất của hiđrocacbon: ngoài cacbon và hiđro, trong phân tử còn có các nguyên tố khác như oxi, clo, … (C2H6O, CH3Cl, …)
Dãy các chất sau là hiđrocacbon là: C3H8, C3H4, C3H6
Câu 16:
Đáp án B
Hợp chất hữu cơ chỉ gồm liên kết đơn là C3H8; C4H10
Cấu 17:
Đáp án C
Câu đúng là: Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ
Câu 18:
Đáp án B
Công thức đơn giản nhất (CTĐGN) là CH2Cl
⇒ Công thức phân tử (CTPT): (CH2Cl)n
Vì MA = 99 ⇒ (12 + 2 + 35,5).n = 99 ⇒ n = 2
⇒ CTPT: C2H4Cl2
Câu 19:
Đáp án B
Câu đúng là: Metan có nhiều trong mỏ khí, mỏ dầu, mỏ than
Câu 20:
Đáp án C
Các phát biểu không đúng: 2, 4, 6
2) Metan là chất khí, không màu, không mùi, nặng hơn không khí ⇒ Sai, khí metan nhẹ hơn không khí.
4) Hỗn hợp giữa Metan và Clo là hỗn hợp nổ ⇒ Sai.
6) Metan tác dụng với Clo ở điều kiện thường ⇒ Sai, phải có chiếu sáng thì phản ứng mới xảy ra
Câu 21:
Đáp án C
= 0,5 mol
⇒ = 1.22,4 = 22,4 lít
= 0,5.22,4 = 11,2 lít
Câu 22:
Đáp án D
Vì các hợp chất hữu cơ có chứa C và thường có H nên khi đốt cháy thì sản phẩm thu được chủ yếu là CO2 và H2O
Câu 23:
Đáp án B
Dẫn 2 khí qua dung dịch nước brom chỉ có C2H4 phản ứng
= 0,25 - 0,025 = 0,225 mol
⇒ = 0,225.22,4 = 5,04 lít
Câu 24:
Đáp án A
Chất tác dụng với dung dịch nước brom là C2H4 vì trong phân tử C2H4 có liên kết đôi
CH2 = CH2 + Br2 → CH2Br = CH2Br
Câu 25:
Đáp án B
Tính chất vật lí của etilen là: Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
Câu 26:
Đáp án C
Liên kết C≡C trong phân tử axetilen có hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 27:
Đáp án D
Phương trình đốt cháy axetilen: 2C2H2 + 5O2 4CO2 + 2H2O
⇒ CO2 và H2O tạo thành theo tỉ lệ 4 : 2 = 2 : 1
Câu 28:
Đáp án D
Tính chất nào không phải của benzen là kém bền với các chất oxi hóa.
Câu 29:
Đáp án D
Nên phát triển các hầm Bio-gas vì
- Vốn đầu tư không lớn
- Đảm bảo vệ sinh môi trường và mầm các bệnh bị tiêu diệt
- Có nguồn năng lượng sạch và thuận tiện
Câu 30:
Đáp án A
Phương pháp hiện đại để điều chế axetilen hiện nay là nhiệt phân metan ở nhiệt độ cao
Phương trình phản ứng:
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 3
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Hai phi kim tác dụng với nhau tạo sản phẩm không làm đổi màu giấy quỳ ẩm là
A. Hiđro và clo
B. Photpho và oxi
C. Lưu huỳnh và oxi
D. Hiđro và oxi
Câu 2: Phi kim có mức hoạt động hóa học yếu nhất là
A. Flo
B. Oxi
C. Clo
D. Silic
Câu 3: Khí clo không tác dụng với
A. Dung dịch NaOH
B. Khí O2
C. Dung dịch Ca(OH)2
D. H2O
Câu 4: Đốt cháy cacbon bởi O2, nếu dư thừa oxi thì sau phản ứng thu được khí nào?
A. CO2
B. O2
C. CO2 và CO dư
D. CO2 và O2 dư
Câu 5: Khử hoàn toàn 2,4 gam đồng (II) oxit bằng khí CO. Thể tích khí CO cần dùng (đktc) là
A. 0,224 lít
B. 0,672 lít
C. 0,448 lít
D. 0,560 lít
Câu 6: Khí CO không khử được oxit nào sau đây ở nhiệt độ cao?
A. CuO
B. ZnO
C. PbO
D. CaO
Câu 7: Ứng dụng của CO2 được dùng để
A. Chữa cháy
B. Bảo quản thực phẩm
C. Dùng trong sản xuất nước giải khát có gas, sản xuất sođa, phân đạm, …
D. A, B, C đều đúng
Câu 8: Điều nào sau đây không đúng cho phản ứng của CO và O2
A. Phản ứng tỏa nhiệt
B. Phản ứng thu nhiệt
C. Phản ứng không xảy ra ở điều kiện thường
D. Phản ứng kèm theo sự giảm thể tích
Câu 9: Chọn đáp án đúng nhất. Tất cả muối cacbonat đều
A. Không tan trong nước
B. Tan trong nước
C. Bị nhiệt phân tạo ra oxit kim loại và cacbon đioxit
D. Bị nhiệt phân trừ muối cacbonat của kim loại kiềm
Câu 10: Khối lượng kết tủa tạo ra, khi cho 5,3 gam Na2CO3 tác dụng vừa đủ với dung dịch Ca(OH)2 là
A. 4 gam
B. 5 gam
C. 6 gam
D. 7 gam
Câu 11: Dung dịch H2CO3 làm quỳ tím chuyển thành màu gì?
A. Đỏ
B. Xanh
C. Tím
D. Vàng
Câu 12: Công nghiệp silicat gồm
A. sản xuất đồ gốm
B. sản xuất thủy tinh
C. sản xuất xi măng
D. Cả A, B, C đều đúng
Câu 13: Thể tích của dung dịch KOH 1M ở điều kiện thường cần dùng để tác dụng hoàn toàn với 2,24 lít khí Cl2 (đktc) là
A. 0,2 lít
B. 0,3 lít
C. 0,4 lít
D. 0,5 lít
Câu 14: Trong một chu kỳ, theo chiều tăng dần của điện tích hạt nhân
A. Tính phi kim giảm dần
B. Tính kim loại không đổi
C. Tính phi kim tăng dần
D. Tính kim loại tăng dần
Câu 15: Nhiệt phân hoàn toàn 50 gam CaCO3 thu được V lít khí ở đktc. Biết hiệu suất phản ứng là H = 80%. Giá trị của V là
A. 7,89 lít
B. 8,96 lít
C. 9,06 lít
D. 10,01 lít
Câu 16: Hợp chất hữu cơ được chia thành mấy loại?
A. 1
B. 2
C. 3
D. 4
Câu 17: Hợp chất vô cơ và hợp chất hữu cơ khác nhau ở điểm nào?
A. Hợp chất hữu cơ kém bền hơn hợp chất vô cơ
B. Hợp chất hữu cơ thường có số lượng nhiều hơn hợp chất vô cơ
C. Hợp chất hữu cơ thường chứa C, H và có thể có O, Cl, …
D. Cả A, B, C đều đúng
Câu 18: Trong thành phần phân tử hợp chất hữu cơ nhất thiết phải có nguyên tố
A. Nitơ
B. Oxi
C. Hiđro
D. Cacbon
Câu 19: Liên kết hóa học trong phân tử chất hữu cơ chủ yếu là liên kết
A. Ion
B. Hiđro
C. Kim loại
D. Cộng hóa trị
Câu 20: Một hợp chất X chứa 2 nguyên tố C, H có tỉ lệ khối lượng là mC : mH = 6 : 1. Hợp chất X có khối lượng mol phân tử là 56. Công thức phân tử của hợp chất X là
A. C5H10
B. C3H6
C. C5H9
D. C4H8
Câu 21: Một hợp chất hữu cơ có công thức C3H7Cl, có số công thức cấu tạo là
A. 1
B. 2
C. 3
D. 4
Câu 22: Công thức cấu tạo dưới đây là của hợp chất nào?
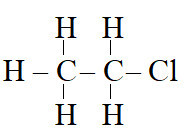
A. C2H5Cl
B. C3H6Cl
C. C4H8Cl
D. C2H6Cl
Câu 23: Thành phần phần trăm về khối lượng của các nguyên tố cacbon và hiđro trong CH4 lần lượt là
A. 40% và 60%
B. 80% và 20%
C. 75% và 25%
D. 50% và 50%
Câu 24: Đốt cháy 8,4 gam etilen bằng oxi, sau phản ứng thu được V lít khí CO2 ở đktc. Giá trị của V là
A. 10,08 lít
B. 13,44 lít
C. 11,56 lít
D. 12,56 lít
Câu 25: Cho 14 gam etilen vào dung dịch brom thấy dung dịch vừa đủ mất màu, khối lượng brom tham gia phản ứng là
A. 80 gam
B. 40 gam
C. 60 gam
D. 50 gam
Câu 26: Trong phòng thí nghiệm người ta thu khí axetilen bằng phương pháp nào là tốt nhất trong các phương pháp sau
A. Đẩy không khí
B. Đẩy nước
C. Đẩy nước brom
D. Cả A, B đều đúng
Câu 27: Tính thể tích dung dịch brom 2M cần để tác dụng với 0,448 lít khí axetilen?
A. 0,01 lít
B. 0,04 lít
C. 0,03 lít
D. 0,02 lít
Câu 28: Một hiđrocacbon ở thể khí thường được dùng làm nhiên liệu để hàn cắt kim loại đó là
A. Etan
B. Axetilen
C. Etilen
D. Metan
Câu 29: Đốt cháy benzene trong không khí tạo ra CO2 và H2O có tỉ lệ là
A. 1 : 2
B. 1 : 3
C. 3 : 1
D. 2 : 1
Câu 30: Đun nóng brom với 3,9 gam benzen (có bột sắt), người ta thu được 4,71 gam brombenzen. Hiệu suất của phản ứng là
A. 60%
B. 70%
C. 80%
D. 90%
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI ĐỀ 3
|
1D |
2D |
3B |
4D |
5B |
6D |
7D |
8B |
9D |
10B |
|
11A |
12D |
13A |
14C |
15B |
16B |
17D |
18D |
19D |
20D |
|
21B |
22A |
23C |
24B |
25A |
26D |
27D |
28B |
29D |
30A |
Câu 1:
Đáp án D
Phương trình phản ứng:
2H2 + O2 2H2O
Nước là môi trường trung tính nên không làm quỳ đổi màu.
Câu 2:
Đáp án D
Theo bảng tuần hoàn các nguyên tố hóa học thì thứ tự của các phi kim này là:
F > Cl > O > Si
Câu 3:
Đáp án B
Khí clo không tác dụng với khí O2
Khí clo tác dụng với: dung dịch NaOH, Ca(OH)2, H2O
Phương trình phản ứng:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Cl2 + Ca(OH)2 → CaOCl2 + H2O
Câu 4:
Đáp án D
Đốt cháy cacbon bởi O2, nếu dư thừa oxi thì sau phản ứng thu được hỗn hợp khí là
CO2 và O2 dư
Câu 5:
Đáp án B
Số mol CuO là: nCuO = 0,03 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: nCO = 0,03 mol
Thể tích khí CO cần dùng (đktc) là: VCO = 0,03.22,4 = 0,672 lít.
Câu 6:
Đáp án D
Ở nhiệt độ cao, khí CO không khử được oxit là: CaO
CO chỉ khử được những oxit của kim loại đứng sau Al trong dãy hoạt động hóa học.
Câu 7:
Đáp án D
Ứng dụng của CO2 được dùng để
+ Chữa cháy
+ Bảo quản thực phẩm
+ Dùng trong sản xuất nước giải khát có gas, sản xuất sođa, phân đạm, …
Câu 8:
Đáp án B
Điều không đúng cho phản ứng của CO và O2 là: Phản ứng thu nhiệt.
Câu 9:
Đáp án D
Tất cả muối cacbonat đều bị nhiệt phân trừ muối cacbonat của kim loại kiềm.
Câu 10:
Đáp án B
Số mol của Na2CO3 là: = 0,05 mol
Phương trình phản ứng:
Số mol của CaCO3 là: = 0,05 mol
Khối lượng CaCO3 là: = 0,05.100 = 5 gam
Câu 11:
Đáp án A
Dung dịch axit H2CO3 làm quỳ tím chuyển thành màu đỏ.
Câu 12:
Đáp án D
Công nghiệp silicat gồm
+ sản xuất đồ gốm
+ sản xuất thủy tinh
+ sản xuất xi măng
Công nghiệp silicat gồm sản xuất đồ gốm, thủy tinh, xi măng.
Câu 13:
Đáp án A
Số mol Cl2 là: = 0,1 mol
Phương trình phản ứng:
Thể tích của dung dịch KOH 1M là: VKOH = = 0,2 lít
Câu 14:
Đáp án C
Trong một chu kỳ, theo chiều tăng của điện tích hạt nhân thì năng lượng ion hóa, độ âm điện tăng dần đồng thời bán kính nguyên tử giảm dần làm cho khả năng nhận electron tăng nên tính phi kim tăng.
Câu 15:
Đáp án B
Số mol của CaCO3 phản ứng là: = 0,4 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,4 mol
Vậy thể tích khí CO2 là: V = 0,4.22,4 = 8,96 lít.
Câu 16:
Đáp án B
Hợp chất hữu cơ được chia thành 2 loại:
+ Hiđrocacbon: phân tử chỉ có 2 nguyên tố là cacbon và hiđro (CH4, C2H4, …)
+ Dẫn xuất của hiđrocacbon: ngoài cacbon và hiđro, trong phân tử còn có các nguyên tố khác như oxi, clo, … (C2H6O, CH3Cl, …)
Câu 17:
Đáp án D
Hợp chất vô cơ và hợp chất hữu cơ khác nhau ở điểm:
+ Hợp chất hữu cơ kém bền hơn hợp chất vô cơ
+ Hợp chất hữu cơ thường có số lượng nhiều hơn hợp chất vô cơ
+ Hợp chất hữu cơ thường chứa C, H và có thể có O, Cl, …
Câu 18:
Đáp án D
Trong thành phần phân tử hợp chất hữu cơ nhất thiết phải có nguyên tố cacbon.
Câu 19:
Đáp án D
Liên kết hóa học trong phân tử chất hữu cơ chủ yếu là liên kết cộng hóa trị.
Câu 20:
Đáp án D
Gọi công thức phân tử của hợp chất X là: CxHy
Ta có
Suy ra công thức đơn giản của hợp chất X là: CH2
Công thức phân tử của hợp chất X có dạng
MX = 56 = n.(12 + 2), suy ra n = 4
Vậy công thức phân tử của hợp chất X là: C4H8
Câu 21:
Đáp án B
Có hai công thức cấu tạo là:
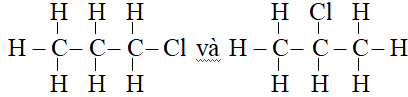
Câu 22:
Đáp án A
Công thức cấu tạo trên là của hợp chất: C2H5Cl
Câu 23:
Đáp án C
Ta có: %mC = = 75%
%mH = 100% - 75% = 25%
Câu 24:
Đáp án B
Số mol của C2H4 là: = 0,3 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,6 mol
Vậy thể tích khí CO2 thu được là: V = 0,6.22,4 = 13,44 lít.
Câu 25:
Đáp án A
Số mol của C2H4 là: = 0,5 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,5 mol
Vậy khối lượng brom tham gia phản ứng là: = 0,5.160 = 80 gam.
Câu 26:
Đáp án D
Trong phòng thí nghiệm người ta thu khí axetilen bằng phương pháp nào là tốt nhất trong các phương pháp sau
+ Đẩy không khí
+ Đẩy nước
Câu 27:
Đáp án D
Số mol C2H2 là: = 0,02 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có = 0,04 mol
Vậy thể tích dung dịch brom cần dùng là: V = = 0,02 lít.
Câu 28:
Đáp án B
Một hiđrocacbon ở thể khí thường được dùng làm nhiên liệu để hàn cắt kim loại đó là: Axetilen
Câu 29:
Đáp án D
Phương trình phản ứng: 2C6H6 + 15O2 12CO2 + 6H2O
Theo phương trình phản ứng ta có tỉ lệ CO2 : H2O = 12 : 6 = 2 : 1
Câu 30:
Đáp án A
Số mol của C6H6 là: = 0,05 mol
Phương trình phản ứng:
Theo phương trình phản ứng ta có: = 0,05 mol
Khối lượng C6H5Br trên lý thuyết là: = 0,05.157 = 7,85 gam
Hiệu suất của phản ứng là: H = = 60%
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 4
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca =40, P = 31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
I. TRẮC NGHIỆM (7 ĐIỂM)
Câu 1: Hỗn hợp khí X gồm O2, Cl2, CO2, SO2. Để thu được O2 tinh khiết, người ta dẫn X qua:
A. nước brom
B. dung dịch NaOH
C. dung dịch HCl
D. nước clo
Câu 2: Để phân biệt SO2 và CO2 có thể dùng một hóa chất nào sau đây?
A. Dung dịch BaCl2
B. Dung dịch NaOH
C. Dung dịch H2SO4
D. Dung dịch Brom.
Câu 3: Dung dịch hỗn hợp hai muối natri clorua và natri hipoclorit được gọi là gì?
A. Nước gia-ven
B. Nước muối
C. Nước axeton
D. Nước cất
Câu 4: Clo tác dụng với sắt dư, sau phản ứng thu được là:
A. FeCl3
B. FeCl2
C. Fe
D. Fe và FeCl3
Câu 5: Có 3 khí đựng riêng biệt trong 3 lọ là oxi, clo, hiđroclorua. Để phân biệt các khí đó có thể dùng một hóa chất là
A. quì tím ẩm
B. dung dịch NaOH
C. dung dịch AgNO3
D. dung dịch brom
Câu 6: Cho dung dịch NaOH 1M để tác dụng vừa đủ với 1,12 lít khí clo (đktc). Nồng độ mol của muối natri clorua thu được là
A. 0,05M.
B. 0,5M.
C. 1,0M.
D. 1,5M.
Câu 7: Dẫn luồng khí CO qua hỗn hợp Al2O3, CuO, MgO, Fe2O3 (nung nóng). Sau khi phản ứng xảy ra hoàn toàn thu được chất rắn là
A. Al2O3, Cu, MgO, Fe.
B. Al, Fe, Cu, Mg.
C. Al2O3, Cu, Mg, Fe.
D. Al2O3, Fe2O3, Cu, MgO.
Câu 8: “Nước đá khô” không nóng chảy mà thăng hoa nên được dùng để tạo môi trường lạnh và khô rất tiện cho việc bảo quản thực phẩm. Nước đá khô là
A. CO rắn.
B. SO2 rắn.
C. H2O rắn.
D. CO2 rắn.
Câu 9: Cho khí CO dư đi qua ống chứa 0,2 mol MgO và 0,2 mol CuO nung nóng đến phản ứng hoàn toàn, thu được x gam chất rắn. Giá trị của x là
A. 17,6
B. 4,8
C. 20,8
D. 24,0
Câu 10: Cho m gam hỗn hợp muối A2CO3 và MCO3 tác dụng hết với 300 ml dung dịch H2SO4 0,5M. Thể tích khí CO2 sinh ra ở đktc là
A. 2,24 lít
B. 4,48 lít
C. 3,36 lít
D. 6,72 lít
Câu 11: Phát biểu nào sau đây là không đúng:
A. Bảng tuần hoàn gồm có các ô nguyên tố, các chu kì và các nhóm
B. Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, sắp xếp theo Z tăng dần
C. Bảng tuần hoàn có 7 chu kì, số thứ tự của chu kì bằng số phân lớp electron trong nguyên tử
D. Bảng tuần hoàn có 8 nhóm A, 8 nhóm B, 18 cột trong đó nhóm A có 8 cột và nhóm B có 10 cột
Câu 12: Chất hữu cơ là:
A. hợp chất khó tan trong nước.
B. hợp chất của cacbon và một số nguyên tố khác trừ N, Cl, O
C. hợp chất của cacbon trừ CO, CO2, H2CO3, muối cacbonat, muối cacbua và xianua.
D. hợp chất có nhiệt độ sôi cao.
Câu 13: Số công thức cấu tạo mạch hở có thể có của C4H8 là
A. 3
B. 4
C. 5
D. 6
Câu 14: Vitamin A là một chất dinh dưỡng thiết yếu cho con người. Trong thực phẩm, vitamin A tồn tại ở dạng chính là retinol (chứa C, H, O) trong đó thành phần % khối lượng H và O tương ứng là 10,49% và 5,594%. Xác định công thức phân tử của retinol là:
A. C18H30O
B. C22H26O
C. C21H18O
D. C20H30O
Câu 15: Phản ứng của metan đặc trưng cho liên kết đơn là:
A. Phản ứng cháy
B. Phản ứng cộng
C. Phản ứng thế
D. Phản ứng trùng hợp
Câu 16: Chất nào sau đây vừa làm mất màu dung dịch brom, vừa tham gia phản ứng trùng hợp?
A. CH4.
B. CH3CH2OH.
C. CH3-CH3.
D. CH2=CH-CH3.
Câu 17: Cấu tạo phân tử axetilen gồm
A. hai liên kết đơn và một liên kết ba.
B. hai liên kết đơn và một liên kết đôi.
C. một liên kết ba và một liên kết đôi.
D. hai liên kết đôi và một liên kết ba.
Câu 18: Cấu tạo đặc biệt của phân tử benzen là:
A. Phân tử có vòng 6 cạnh
B. Phân tử có 3 vòng liên kết đôi
C. Phân tử có vòng 6 cạnh chứa 3 liên kết đôi xen kẽ 3 liên kết đơn
D. Phần tử có vòng 6 cạnh chứa liên kết đôi và liên kết đơn
Câu 19: Để sử dụng nhiên liệu có hiệu quả cần phải cung cấp không khí hoặc oxi:
A. Vừa đủ
B. Thiếu
C. Dư
D. Cả ba cách trên đều đúng.
Câu 20: Đốt cháy hòa toàn 15,6 gam benzen rồi hấp thụ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư. Khối lượng dung dịch tăng hay giảm bao nhiêu gam?
A. tăng 56,4 gam.
B. giảm 28,2 gam.
C. giảm 56,4 gam.
D. tăng 28,2 gam
II. TỰ LUẬN (3 ĐIỂM)
Câu 1: (1 điểm) Trình bày phương pháp hóa học để nhận biết các chất khí đựng trong các lọ khí riêng biệt sau: CH4; C2H2; CO2
Câu 2: (2 điểm) Dẫn 5,6 lít hỗn hợp khí metan CH4 và axetilen C2H2 (ở đktc) đi qua dung dịch brom dư, thấy có 32 gam brom phản ứng.
a) Viết phương trình phản ứng xảy ra.
b) Tính thành phần phần trăm theo thể tích các khí có trong hỗn hợp.
c) Tính thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn hỗn hợp trên.
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI ĐỀ 4
|
1B |
2D |
3A |
4D |
5A |
6B |
7A |
8D |
9C |
10C |
|
11C |
12C |
13A |
14D |
15C |
16D |
17A |
18C |
19A |
20C |
I. TRẮC NGHIỆM (7 ĐIỂM)
Câu 1:
Đáp án B
Để thu được O2 tinh khiết, người ta dẫn X qua dung dịch NaOH vì Cl2, CO2 và SO2 đều có phản ứng (dung dịch NaOH giữ lại Cl2, CO2 và SO2) còn O2 không có phản ứng.
2NaOH + Cl2 → NaCl + NaClO + H2O
CO2 + 2NaOH → Na2CO3 + H2O
SO2 + 2NaOH → Na2SO3 + H2O
Câu 2:
Đáp án D
Để phân biệt SO2 và CO2 có thể dùng dung dịch brom. SO2 làm mất màu dung dịch brom còn CO2 thì không.
SO2 + Br2 + 2H2O → 2HBr + H2SO4
Câu 3:
Đáp án A
Dung dịch hỗn hợp hai muối natri clorua (NaCl) và natri hipoclorit (NaClO) được gọi là nước gia-ven
Câu 4:
Đáp án D
Clo tác dụng với sắt xảy ra phản ứng:
3Cl2 + 2Fe 2FeCl3
Tuy Fe dư nhưng đây không phải trong dung dịch, do đó Fe không tiếp tục phản ứng với FeCl3 để tạo ra FeCl2
Vậy sau phản ứng thu được gồm Fe và FeCl3.
Câu 5:
Đáp án A
Để phân biệt 3 khí O2, Cl2 và HCl ta dùng giấy quỳ tím ẩm.
- O2 không làm đổi màu quỳ
- Cl2 làm mất màu quỳ tím ẩm (do HClO sinh ra có tính tẩy màu)
Cl2 + H2O ⇄ HCl + HClO
- HCl làm quỳ tím ẩm hóa đỏ (vì HCl tan vào nước tạo thành axit HCl)
Câu 6:
Đáp án B
⇒ VNaOH = lít
⇒ CM NaCl = = 0,5M
Câu 7:
Đáp án A
Khí CO chỉ khử được các oxit kim loại đứng sau Al ⇒ khử được CuO và Fe2O3
Câu 8:
Đáp án D
Nước đá khô là CO2 rắn
Câu 9:
Đáp án C
MgO không phản ứng với CO
Chất rắn gồm MgO và Cu
⇒ x = mMgO + mCu = 0,2.40 + 0,2.64 = 20,8 gam
Câu 10:
Đáp án C
= 0,3.0,5 = 0,15 mol =
Hỗn hợp muối cacbonat tác dụng với dung dịch H2SO4 thu được
= 0,15.22,4 = 3,36 lít
Câu 11:
Đáp án C
Phát biểu không đúng là: Bảng tuần hoàn có 7 chu kì, số thứ tự của chu kì bằng số phân lớp electron trong nguyên tử.
Số thứ tự của chu kì bằng số lớp electron trong nguyên tử
Câu 12:
Đáp án C
Chất hữu cơ là: hợp chất của cacbon trừ CO, CO2, H2CO3, muối cacbonat, muối cacbua và xianua.
Câu 13:
Đáp án A
có k = = ⇒ π = 1 (vì v = 0) ⇒ trong phân tử có 1 liên kết đôi
1. CH2=CH-CH2-CH3
2. CH3-CH=CH-CH3
3. CH3-C(CH3)=CH2
Câu 14:
Đáp án D
Vì A chỉ chứa C, H và O
⇒ %mC = 100% - %mH - %mO = 100% - 10,49% - 5,594% = 83,916%
⇒ x : y : z =
= 6,993 : 10,49 : 0,349 = 20 : 30 : 1
Vì renitol chứa một nguyên tử O ⇒ z = 1
⇒ x = 20 và y = 30
⇒ Công thức phân tử của retinol là C20H30O
Câu 15:
Đáp án C
Phản ứng của metan đặc trưng cho liên kết đơn là: phản ứng thế
Câu 16:
Đáp án D
Chất vừa làm mất màu dung dịch brom, vừa tham gia phản ứng trùng hợp là chất có liên kết đôi (giống etilen)
⇒ CH2 = CH-CH3
Câu 17:
Đáp án A
- Công thức cấu tạo của axetilen: H – C ≡ C – H.
⇒ cấu tạo phân tử axetilen gồm: và 2 liên kết đơn C – H.
+ Có 1 liên kết ba giữa 2 nguyên tử cacbon
+ Trong liên kết ba có 2 liên kết kém bền, dễ bị đứt lần lượt trong phản ứng hóa học
Câu 18:
Đáp án C
Cấu tạo đặc biệt của phân tử benzen là: Phân tử có vòng 6 cạnh chứa 3 liên kết đôi xen kẽ 3 liên kết đơn
Câu 19:
Đáp án A
Để sử dụng nhiên liệu có hiệu quả cần phải cung cấp không khí hoặc oxi vừa đủ.
Nếu dư hoặc thiếu oxi sẽ gây lãng phí nhiên liệu đồng thời dễ xảy ra cháy nổ.
Câu 20:
Đáp án C
Phương trình hóa học:
⇒ = 1,2.100 = 120g
= 1,2.44 + 0,6.18 = 63,6 gam <
⇒ Khối lượng dung dịch giảm là: 120 − 63,6 = 56,4 (g)
II. TỰ LUẬN (3 ĐIỂM)
Câu 1:
Dẫn lần lượt các khí đã cho vào dung dịch nước brom, khí nào làm mất màu dung dịch brom là C2H2, hai khí còn lại là CH4 và CO2
C2H2 + 2Br2 → C2H2Br4
Dẫn 2 khí còn lại vào dung dịch nước vôi trong Ca(OH)2 dư, khí làm đục nước vôi trong là CO2, còn lại là CH4
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 2:
a) Phương trình hóa học: C2H2 + 2Br2 → C2H2Br4
b) Theo phương trình ta có :
= 0,25 – 0,1 = 0,15 mol
= 0,1.22,4 = 2,24 lít
= 100% - 40% = 60%
c) Phương trình hóa học phản ứng đốt cháy hỗn hợp khí trên:
(1)
Từ (1) và (2) ta có: = 0,3 + 0,25 = 0,55 mol
= 0,55.22,4 = 12,32 lít
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 5
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
Câu 1: Dẫn khí Cl2 vào dung dịch KOH, tạo thành
A. dung dịch chỉ gồm một muối.
B. dung dịch hai muối.
C. dung dịch chỉ gồm một axit.
D. dung dịch gồm một axit và một muối.
Câu 2: Đốt cháy hoàn toàn 1,08 gam một kim loại hoá trị III trong khí clo. Sau phản ứng thu được 5,34 gam muối clorua. Kim loại đem đốt cháy là
A. Au.
B. Al.
C. Fe.
D. Ga.
Câu 3: Kim cương, than chì, cacbon vô định hình là các dạng thù hình của nguyên tố
A. photpho
B. silic
C. cacbon
D. lưu huỳnh
Câu 4: Đốt cháy hoàn toàn 1,2 gam C thì thể tích tối đa của khí CO2 thu được ở đktc là
A. 1,12 lít.
B. 11,2 lít.
C. 2,24 lít.
D. 22,4 lít.
Câu 5: Khối lượng C cần dùng để khử 8 gam CuO tạo thành CO2 là
A. 0,6 gam.
B. 1,2 gam.
C. 2,4 gam.
D. 3,6 gam.
Câu 6: Khi dẫn khí CO qua ống nghiệm đựng Fe2O3 nung nóng có thể xảy ra phản ứng nào sau đây. Chọn đáp án đúng nhất.
A. 8CO + 3Fe2O3 6Fe + 8CO2
B. 2CO + Fe2O3 2FeCO3
C. 3CO + Fe2O3 2Fe + 3CO2
D. 3CO + Fe2O3 3FeO + 3CO
Câu 7: Quá trình nào sau đây làm giảm CO2 trong khí quyển?
A. Sự hô hấp của động vật và con người.
B. Cây xanh quang hợp.
C. Đốt than và khí đốt.
D. Quá trình nung vôi.
Câu 8: Khí CO dùng làm chất đốt trong công nghiệp có lẫn tạp chất là CO2 và SO2. Có thể làm sạch CO bằng
A. dung dịch nước vôi trong.
B. H2SO4 đặc.
C. dung dịch BaCl2.
D. CuSO4 khan.
Câu 9: Dãy gồm các chất đều phản ứng với dung dịch HCl là
A. Na2CO3, CaCO3.
B. K2SO4, Na2CO3.
C. Na2SO4, MgCO3.
D. Na2SO3, KNO3.
Câu 10: Cặp chất nào sau đây có thể tác dụng được với nhau ?
A. HCl và KHCO3.
B. Na2CO3 và K2CO3.
C. K2CO3 và NaCl.
D. CaCO3 và NaHCO3.
Câu 11: Thí nghiệm nào sau đây có hiện tượng sinh ra kết tủa trắng và bọt khí thoát ra khỏi dung dịch ?
A. Nhỏ từng giọt dung dịch NaOH vào ống nghiệm đựng dung dịch CuCl2.
B. Nhỏ từ từ dung dịch H2SO4 vào ống nghiệm có sẵn một mẫu BaCO3.
C. Nhỏ từ từ dung dịch BaCl2 vào ống nghiệm đựng dung dịch AgNO3.
D. Nhỏ từ từ dung dịch HCl vào ống nghiệm đựng dung dịch Na2CO3.
Câu 12: Cho phương trình hóa học sau: X + NaOH Na2CO3 + H2O. X là
A. CO.
B. NaHCO3.
C. CO2.
D. KHCO3.
Câu 13: Dãy các kim loại nào sau đây được sắp xếp theo chiều tính kim loại tăng dần ?
A. K, Ba, Mg, Fe, Cu.
B. Ba, K, Fe, Cu, Mg.
C. Cu, Fe, Mg, Ba, K.
D. Fe, Cu, Ba, Mg, K.
Câu 14: Công nghiệp silicat là công nghiệp sản xuất
A. đá vôi, đất sét, thủy tinh.
B. đồ gốm, thủy tinh, xi măng.
C. hiđrocacbon, thạch anh, thủy tinh.
D. thạch anh, đất sét, đồ gốm.
Câu 15: Chất khí nào sau đây có thể gây chết người vì ngăn cản sự vận chuyển oxi trong máu?
A. CO
B. CO2
C. SO2
D. NO
Câu 16: Phương trình hóa học điều chế nước Gia - ven là
A. Cl2 + NaOH NaCl + HClO
B. Cl2 + NaOH NaClO + HCl
C. Cl2 + H2O HCl + HClO
D. Cl2 + 2NaOH NaCl + NaClO + H2O
Câu 17: Nung 150 kg CaCO3 thu được 67,2 kg CaO. Hiệu suất phản ứng là
A. 60%.
B. 40%.
C. 80%.
D. 50%.
Câu 18: Dãy các chất nào sau đây đều là dẫn xuất của hiđrocacbon ?
A. C2H6O, CH4, C2H2.
B. C2H4, C3H7Cl, CH4.
C. C2H6O, C3H7Cl, C2H5Cl.
D. C2H6O, C3H8, C2H2.
Câu 19: Trong công thức nào sau đây có chứa liên kết ba ?
A. C2H4 (etilen).
B. CH4 (metan).
C. C2H2 (axetilen).
D. C6H6 (benzen).
Câu 20: Chất có phần trăm khối lượng cacbon lớn nhất là
A. CH4.
B. CH3Cl.
C. CH2Cl2.
D. CHCl3.
Câu 21: Trong phân tử etilen có
A. 4 liên kết đơn C–H.
B. 1 liên kết đôi C=C và 4 liên kết đơn C–H.
C. 2 liên kết đơn C – H và 2 liên kết đôi C = H.
D. 1 liên kết đôi C=C và 3 liên kết đôi C = H.
Câu 22: Hoá chất nào sau đây dùng để phân biệt 2 chất CH4 và C2H4?
A. Dung dịch brom.
B. Dung dịch phenolphtalein.
C. Quì tím.
D. Dung dịch bari clorua.
Câu 23: Đốt cháy hoàn toàn 11,2 lít hỗn hợp khí gồm CH4 và H2 (đktc) thu được 16,2 gam nước. Thành phần phần trăm theo thể tích của khí CH4 và H2 trong hỗn hợp lần lượt là chương
A. 60% và 40%.
B. 80% và 20%.
C. 50% và 50%.
D. 30% và 70%.
Câu 24: Tính chất vật lý của khí etilen
A. là chất khí không màu, không mùi, tan trong nước, nhẹ hơn không khí.
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí màu vàng lục, không mùi, ít tan trong nước, nặng hơn không khí.
D. là chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Câu 25: Axetilen có tính chất vật lý
A. là chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
B. là chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí không màu, không mùi, tan trong nước, nhẹ hơn không khí
D. là chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Câu 26: Liên kết CC trong phân tử axetilen có đặc điểm
A. một liên kết kém bền dễ đứt ra trong các phản ứng hóa học.
B. hai liên kết kém bền nhưng chỉ có một liên kết bị đứt ra trong phản ứng hóa học.
C. hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
D. ba liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 27: Tính khối lượng benzen cần dùng để điều chế được 31,4 gam brombenzen? Biết hiệu suất phản ứng là 85%
A. 15,6 gam.
B. 13,26 gam.
C. 18,353 gam.
D. 32 gam.
Câu 28: Dẫn 2,8 lít hỗn hợp khí metan và etilen (đktc) qua bình đựng dung dịch brom đã làm mất màu một dung dịch có chứa 4 gam brom. Thể tích khí metan có trong hỗn hợp đó là:
A. 2,24 lít
B. 2,42 lít
C. 4,22 lít
D. 5.6 lít
Câu 29: Thành phần chính trong bình khí biogas là:
A. C2H2.
B. CH4.
C. C2H4.
D. C2H4O.
Câu 30: Hợp chất hữu cơ A có thành phần khối lượng các nguyên tố như sau: 85,7% C và 14,3% H. Biết phân tử khối của A là 28 đvC. Công thức hóa học của A là:
A. CH4.
B. C6H6.
C. C2H2.
D. C2H4.
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 6
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
(Cho C = 12, O = 16, H = 1, Na = 23, K = 39, Mg = 24, Ca = 40, P = 31, Cl = 35,5, F = 19, Si = 27, N = 14, S = 32)
I. TRẮC NGHIỆM (7 ĐIỂM)
Câu 1: Cho dung dịch Na2CO3 vào dung dịch HCl hiện tượng xảy ra là:
A. Xuất hiện kết tủa trắng.
B. Có bọt khí xảy ra trong ống nghiệm.
C. Không có hiện tượng gì.
D. Xuất hiện kết tủa trắng đồng thời có bọt khí thoát ra trong ống nghiệm.
Câu 2: Cho phát biểu đúng về hiđro clorua ở điều kiện thường:
A. Là chất khí tan nhiều trong nước
B. Là chất khí không tan trong nước
C. Là chất lỏng tan nhiều trong nước
D. Là chất lỏng không tan trong nước
Câu 3: Dãy các phi kim tác dụng với hiđro tạo thành hợp chất khí là
A. C, Br2, S, Cl2.
B. C, O2, S, Si.
C. Si, Br2, P, Cl2.
D. P, Si, Cl2, S.
Câu 4: Có một sơ đồ chuyển hoá sau:
MnO2 → X → FeCl3 → Fe(OH)3. X có thể là
A. Cl2.
B. HCl.
C. H2SO4.
D. H2.
Câu 5: Dãy oxit phản ứng với cacbon ở nhiệt độ cao tạo thành đơn chất kim loại là
A. CuO, CaO, Fe2O3.
B. PbO, CuO, ZnO.
C. Fe2O3, PbO, Al2O3.
D. Na2O, ZnO, Fe3O4.
Câu 6: Cho 1 mol Ca(OH)2 phản ứng với 1 mol CO2. Muối tạo thành là
A. CaCO3.
B. Ca(HCO3)2.
C. CaCO3 và Ca(HCO3)2.
D. CaCO3 và Ca(OH)2 dư.
Câu 7: Dãy các chất nào sau đây là muối axit?
A. KHCO3, CaCO3, Na2CO3.
B. Ba(HCO3)2, NaHCO3, Ca(HCO3)2.
C. Ca(HCO3)2, Ba(HCO3)2, BaCO3.
D. Mg(HCO3)2, Ba(HCO3)2, CaCO3.
Câu 8: Một hợp chất khí của R với hiđro có công thức RH3. Trong đó R chiếm 91,1765% theo khối lượng. Nguyên tố R thuộc chu kỳ mấy, nhóm mấy?
A. Chu kỳ 2, nhóm III.
B. Chu kỳ 3, nhóm V.
C. Chu kỳ 3, nhóm VI.
D. Chu kỳ 2, nhóm II.
Câu 9: Hàm lượng khí CO2 trong khí quyển của Trái Đất gần như không thay đổi vì:
A. CO2 không có khả năng tác dụng với các chất khí khác trong không khí.
B. Trong quá trình quang hợp cây xanh hấp thụ khí CO2, mặt khác, lượng CO2 được sinh ra do đốt nhiên liệu, sự hô hấp của người và động vật.
C. CO2 hòa tan trong nước mưa.
D. CO2 không bị phân hủy bởi nhiệt.
Câu 10: Để loại bỏ khí cacbonic trong hỗn hợp khí cacbonic và metan bằng cách sục hỗn hợp trên vào:
A. dung dịch HCl
B. dung dịch NaOH
C. Nước
D. dung dịch Ca(OH)2
Câu 11: Nguyên tử của nguyên tố X có 2 lớp electron, lớp ngoài cùng có 6 electron. Câu trả lời nào sau đây đúng?
A. X thuộc chu kì 6, nhóm 2, là một kim loại.
B. X thuộc chu kì 2, nhóm VI, là một phi kim.
C. X thuộc chu kì 6, nhóm 2, là một phi kim.
D. X thuộc chu kì 2, nhóm VI, là một kim loại.
Câu 12: Các hiđrocacbon đã học (trong chương trinh hóa lớp 9) đều có tính chất hóa học chung là:
A. Phản ứng cháy
B. Phản ứng thế
C. Phản ứng cộng
D. Phản ứng trùng hợp
Câu 13: Cặp muối nào sau đây phản ứng được với nhau:
A. Na2CO3 và K2CO3
B. K2CO3 và Ca(NO3)2
C. NaCl và CuCl2
D. NaHCO3 và FeSO4
Câu 14: Một thể tích của hợp chất A phản ứng hoàn toàn với hai thể tích oxi tạo ra một thể tích khí cacbonic. Vậy A là:
A. CH4
B. C2H4
C. C2H2
D. C3H8
Câu 15: Dãy các chất nào chỉ gồm các chất hữu cơ:
A. CH4, H2CO3, C2H6, C4H10
B. C3H6O2, C2H4Br2, C2H5ONa, C2H4O2
C. NaHCO3, CO2, C12H22O11, CH3NO2
D. C6H6, CaCO3, C2H2, C2H4O
Câu 16: Hợp chất nào sau đây vừa tham gia phản ứng cộng vừa tham gia phản ứng thế?
A. etan
B. axetilen
C. benzen
D. metan
Câu 17: Trong phân tử metan có
A. 4 liên kết đơn C–H.
B. 1 liên kết đôi C=H và 3 liên kết đơn C–H.
C. 2 liên kết đơn C–H và 2 liên kết đôi C=H.
D. 1 liên kết đơn C–H và 3 liên kết đôi C=H.
Câu 18: Để loại bỏ khí axetilen trong hỗn hợp với metan người ta dùng
A. nước.
B. khí hiđro.
C. dung dịch brom.
D. khí oxi.
Câu 19: Câu nào đúng nhất trong các câu sau đây?
A. Benzen là một hiđrocacbon
B. Benzen là một hiđrocacbon no
C. Benzen là một hiđrocacbon không no
D. Benzen là một hiđrocacbon thơm
Câu 20: Hãy chọn câu đúng trong những câu sau đây:
A. Chất nào làm mất màu dung dịch brom chất đó là etilen và axetilen.
B. Hiđrocacbon có liên kết đôi hoặc liên kết ba trong phân tử tương tự như etilen hoặc axetilen làm mất màu dung dịch brom.
C. Hiđrocacbon có liên kết đôi trong phân tử làm mất màu dung dịch brom.
D. Những chất có công thức cấu tạo giống metan dễ làm mất màu dung dịch brom.
III. TỰ LUẬN (3 điểm)
Câu 1: Dùng phương pháp hóa học để nhận biết các chất khí sau bị mất nhãn: Metan, etilen, cacbon đioxit.
Câu 2: Viết phương trình hóa học thực hiện dãy biến hóa
CaC2 C2H2 C2H4 C2H6 C2H5Cl
Câu 3: Đốt cháy hoàn toàn 4,48 lít khí etilen (đktc). Tính
a) Thể tích oxi cần dùng
b) Khối lượng nước tạo thành
c) Toàn bộ sản phẩm cháy dẫn vào bình đựng dung dịch nước vôi trong dư. Tính khối lương kết tủa thu được
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 7
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
A – Phần trắc nghiệm (3 điểm)
Câu 1: Dãy gồm các phi kim thể khí ở điều kiện thường là
A. S, P, N2, Cl2. B. C, S, Br2, Cl2.
C. Cl2, H2, N2, O2. D. Br2, Cl2, N2, O2.
Câu 2: Chất nào sau đây khi cháy tạo ra oxit ở thể khí ?
A. Canxi. B. Silic.
C. Cacbon. D. Magie.
Câu 3: Nguyên tử của nguyên tố X có 2 lớp electron, lớp electron ngoài cùng có 7 electron. Vị trí và tính chất cơ bản của nguyên tố X là
A. thuộc chu kỳ 2, nhóm VII là kim loại mạnh.
B. thuộc chu kỳ 7, nhóm III là kim loại yếu.
C. thuộc chu kỳ 2, nhóm VII là phi kim mạnh.
D. thuộc chu kỳ 2, nhóm VII là phi kim yếu.
Câu 4: Chất hữu cơ nào sau đây, khi cháy tạo thành số mol khí CO2 nhỏ hơn số mol hơi nước ?
A. CH4 B. C2H4
C. C2H2 D. C6H6
Câu 5: Hiđrocacbon X có thành phần phần trăm về khối lượng nguyên tố cacbon trong hợp chất là 85,7 %. X là
A. CH4. B. CH3Cl.
C. C2H4. D. C2H6.
Câu 6: Dãy các chất nào sau đây đều làm mất màu dung dịch brom?
A. CH4; C6H6. B. C2H4; CH4.
C. CH4; C2H4. D. C2H4; C2H2.
Câu 7: Đốt cháy hoàn toàn 1 mol khí axetilen thì cần bao nhiêu lít không khí (các khí đo ở đktc, biết rằng oxi chiếm 20% thể tích không khí) ?
A. 300 lít. B. 280 lít.
C. 240 lít. D. 120 lít.
Câu 8: Trong các hiđrocacbon sau khi đốt hiđrocacbon nào sinh ra nhiều muội than ?
A. C2H6 B. CH4
C. C2H4 D. C6H6
Câu 9: Trong các loại than dưới đây, loại than trẻ nhất có hàm lượng cacbon thấp nhất là
A. than gầy. B. than mỡ.
C. than non. D. than bùn.
Câu 10: Khí tham gia phản ứng trùng hợp là
A. CH4. B. C2H4.
C. C3H8. D. C2H6.
B – Phần II: Tự luận (7 điểm)
Câu 1 : (2,0 điểm) Dẫn 11,2 lít hỗn hợp khí gồm C2H4; C2H2 vào lượng dư dung dịch Br2 thấy có 0,7 mol Br2 tham gia phản ứng. Tính phần trăm thể tích của mỗi khí trong hỗn hợp ban đầu (biết thể tích các khí đều đo ở đktc)
Câu 2 (2 điểm). Nêu phương pháp làm sạch khí C2H2 bị lẫn các khí CO2 và SO2. Viết các phương trình phản ứng hoá học xảy ra (nếu có).
Câu 3 (3 điểm): Khi đốt hoàn toàn 3 gam một hợp chất hữu cơ A thu được 8,8 gam CO2 và 5,4 gam H2O
a) Trong A có chứa những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Xác định công thức phân tử của A?
c) A có làm mất màu dung dịch brom không?
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI:
Phần A – Trắc nghiệm
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
C |
C |
A |
C |
D |
B |
D |
D |
B |
Câu 3:
Nguyên tử của nguyên tố X có 2 lớp electron → X thuộc chu kỳ 2;
Lớp ngoài cùng của X có 7 electron → X thuộc nhóm VII;
X thuộc chu kì 2; nhóm VII nên là phi kim mạnh.
Câu 4:
CH4 + 2O2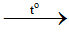 CO2 + 2H2O
CO2 + 2H2O
1 → 1 2 mol
Vậy đốt cháy metan thu được số mol CO2 nhỏ hơn số mol nước.
Câu 5:
Đặt X có dạng CxHy
Theo bài ra, ta có:
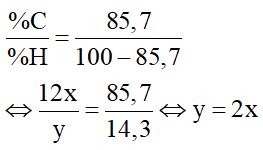
Trong 4 đáp án chỉ có C2H4 thỏa mãn.
Câu 7.
2C2H2 + 5O2 4CO2 + 2H2O
4CO2 + 2H2O
1 → 2,5 mol
→ Voxi = 2,5.22,4 = 56 lít
→ Vkhông khí = 56.5 = 280 lít.
Phần B – Tự luận
Câu 1:
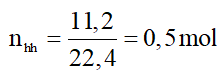
Đặt số mol của C2H4 và C2H2 trong hỗn hợp lần lượt là x và y (mol);
Ta có: x + y = 0,5 (1)
Phương trình hóa học:
C2H4 + Br2 → C2H4Br2
x → x mol
C2H2 + 2Br2 → C2H2Br4
y → 2y mol
Từ các PTHH có: x + 2y = 0,7 (2)
Từ (1) và (2) có x = 0,3 và y = 0,2
Do các khí ở cùng điều kiện nên tỉ lệ về thể tích cũng là tỉ lệ về số mol;
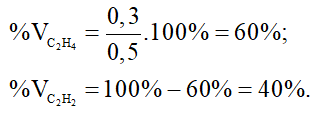
Câu 2:
Dẫn hỗn hợp khí qua bình đựng nước vôi trong; dư.
Khí CO2; SO2 phản ứng bị giữ lại; khí C2H2 không phản ứng thoát ra khỏi dung dịch thu được C2H2 tinh khiết.
Phương trình hóa học:
CO2 + Ca(OH)2→ CaCO3 + H2O
SO2 + Ca(OH)2 → CaSO3 + H2O
Câu 3:
a)
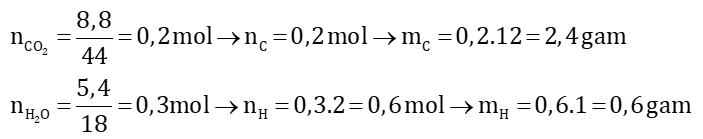
→ mO = 3 – (mC + mH) = 3 – 2,4 – 0,6 = 0
→ A chỉ chứa 2 nguyên tố C và H
b)
nC : nH = 0,2 : 0,6 = 1 : 3
→ Công thức đơn giản nhất của A: (CH3)n
MA < 40 → 15n < 40 → n < 2,67 → n chỉ có thể là 1 hoặc 2
TH 1: n = 1 → Công thức phân tử của A là CH3 ( Loại)
TH 2: n = 2 → Công thức phân tử của A là C2H6 ( thỏa mãn)
c) C2H6 có công thức cấu tạo:
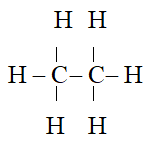
Phân tử chỉ chưa liên kết đơn nên không làm mất màu dung dịch brom.
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 8
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Câu 1: Ở điều kiện thường, phi kim có thể tồn tại ở trạng thái
A. Lỏng và khí. B. Rắn và lỏng.
C. Rắn và khí. D. Rắn, lỏng, khí.
Câu 2: Dãy hợp chất nào sau đây chỉ chứa các chất hữu cơ?
A. CH4, C2H6, CO2. B. C6H6, CH4, C2H5OH.
C. CH4, C2H2, CO. D. C2H2, C2H6O, CaCO3.
Câu 3: Hoá trị của cacbon, oxi, hiđro trong hợp chất hữu cơ lần lượt là
A. IV, II, II. B. IV, III, I.
C. II, IV, I. D. IV, II, I.
Câu 4: Nguyên tử cacbon có thể liên kết trực tiếp với nhau tạo thành các dạng mạch cacbon là
A. Mạch vòng.
B. Mạch thẳng, mạch nhánh.
C. Mạch vòng, mạch thẳng, mạch nhánh.
D. Mạch nhánh.
Câu 5: Hiđrocacbon A có phân tử khối là 30 đvC. Công thức phân tử của A là
A. CH4. B. C2H6. C. C3H8. D. C2H4.
Câu 6: Tính chất vật lí cơ bản của metan là
A. Chất lỏng, không màu, tan nhiều trong nước.
B. Chất khí, không màu, tan nhiều trong nước.
C. Chất khí, không màu, không mùi, nặng hơn không khí, ít tan trong nước.
D. Chất khí, không màu, không mùi, nhẹ hơn không khí, ít tan trong nước.
Câu 7: Phản ứng đặc trưng của metan là
A. Phản ứng cộng. B. Phản ứng thế.
C. Phản ứng trùng hợp. D. Phản ứng cháy
Câu 8: Trong phân tử etilen giữa hai nguyên tử cacbon có
A. Một liên kết đơn. B. Một liên kết đôi.
C. Hai liên kết đôi. D. Một liên kết ba.
Câu 9: Khí etilen không có tính chất hóa học nào sau đây?
A. Phản ứng cháy với khí oxi.
B. Phản ứng trùng hợp.
C. Phản ứng cộng với dung dịch brom.
D. Phản ứng thế với clo ngoài ánh sáng.
Câu 10: Liên kết C≡C trong phân tử axetilen có đặc điểm
A. Một liên kết kém bền dễ đứt ra trong các phản ứng hóa học.
B. Hai liên kết kém bền nhưng chỉ có một liên kết bị đứt ra trong phản ứng hóa học.
C. Hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
D. Ba liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 11: Dẫn 0,1 mol khí axetilen qua dung dịch nước brom dư. Khối lượng brom tham gia phản ứng là
A. 16,0 gam. B. 20,0 gam. C. 26,0 gam. D. 32,0 gam.
Câu 12: Hoá chất nào sau đây dùng để phân biệt 2 chất CH4 và C2H4?
A. Dung dịch brom. B. Dung dịch phenolphtalein.
C. Qùy tím. D. Dung dịch bari clorua.
Câu 13: Cho khí metan tác dụng với khí oxi theo phản ứng sau:
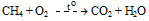
Tổng hệ số cân bằng trong phương trình hoá học là (biết hệ số cân bằng là các số nguyên tối giản)
A. 5. B. 6. C. 7. D. 8.
Câu 13:
CH4 + 2O2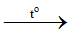 CO2 + 2H2O
CO2 + 2H2O
Tổng hệ số cân bằng: 1 + 2 + 1 + 2 = 6.
Câu 14: Hợp chất hữu cơ không có khả năng tham gia phản ứng cộng là
A. metan. B. benzen. C. etilen. D. axetilen.
Câu 15: Trong các chất sau: CH4, CO2, C2H4, Na2CO3, C2H5ONa có
A. 1 hợp chất hữu cơ và 4 hợp chất vô cơ.
B. 2 hợp chất hữu cơ và 3 hợp chất vô cơ.
C. 4 hợp chất hữu cơ và 1 hợp chất vơ cơ.
D. 3 hợp chất hữu cơ và 2 hợp chất vô cơ.
Câu 16: Dãy các chất nào sau đây đều là hiđrocacbon?
A. C2H6, C4H10, C2H4. B. CH4, C2H2, C3H7Cl.
C. C2H4, CH4, C2H5Cl. D. C2H6O, C3H8, C2H2.
Câu 17: Phương trình hóa học điều chế nước Gia - ven là
A. Cl2 + NaOH → NaCl + HClO
B. Cl2 + NaOH → NaClO + HCl
C. Cl2 + H2O → HCl + HClO
D. Cl2 + 2NaOH → NaCl + NaClO + H2O
Câu 18: Chất khí nào sau đây có thể gây chết người vì ngăn cản sự vận chuyển oxi trong máu?
A. CO. B. CO2. C. SO2. D. NO.
Câu 19: Cho 11,2 lít khí etilen (đktc) phản ứng vừa đủ với dung dịch brom 5%. Khối lượng dung dịch brom tham gia phản ứng là
A. 160 gam. B. 1600 gam.
C. 320 gam. D. 3200 gam.
Câu 20: Một hiđrocacbon ở thể khí thường được dùng làm nhiên liệu để hàn cắt kim loại, đó là
A. metan. B. etilen.
C. axetilen. D. etan.
Câu 21: Khi đốt khí axetilen, số mol CO2 và H2O được tạo thành theo tỉ lệ là
A. 2 : 1. B. 1 : 2.
C. 1 : 3. D. 1 : 1.
Câu 22: Khí X có tỉ khối đối với oxi là 0,8125. Khí X là
A. C2H2. B. C2H4.
C. C2H6. D. CH4.
Câu 23: Phân tử nào sau đây có cấu tạo là mạch vòng sáu cạnh đều, có ba liên kết đơn xen kẽ ba liên kết đôi?
A. Axetilen. B. Propan.
C. Benzen. D. Xiclohexan.
Câu 24: Cho 7,8 gam benzen phản ứng với brom dư (có bột sắt xúc tác) hiệu suất phản ứng là 80%. Khối lượng brombenzen thu được là
A. 12,56 gam. B. 15,70 gam.
C. 19,62 gam. D. 23,80 gam.
Câu 25: Thành phần chính của khí đồng hành là
A. C2H2. B. CH4.
C. C2H4. D. H2.
Câu 26: Trên mũi khoan để khai thác dầu mỏ người ta có gắn
A. thép tốt. B. đá thạch anh.
C. kim cương. D. đá hoa cương.
Câu 27: Trong các loại than dưới đây, loại than già nhất có hàm lượng cacbon trên 90% là
A. than gầy. B. than mỡ.
C. than non. D. than bùn.
Câu 28: Chất làm mất màu dung dịch brom là
A. CH4. B. CH2 = CH – CH3.
C. CH3 – CH3. D. CH3 – CH2 – CH3.
Câu 29: Các trái cây, trong quá trình chín sẽ thoát ra một lượng nhỏ chất khí là
A. metan. B. etan.
C. etilen. D. axetilen.
Câu 30: Khí CH4 và C2H4 có tính chất hóa học giống nhau là
A. tham gia phản ứng cộng với dung dịch brom.
B. tham gia phản ứng cộng với khí hiđro.
C. tham gia phản ứng trùng hợp.
D. tham gia phản ứng cháy với khí oxi sinh ra khí cacbonic và nước.
ĐÁP ÁN ĐỀ THI GIỮA HỌC KÌ 2 MÔN HÓA HỌC LỚP 9
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
D |
B |
D |
C |
B |
D |
B |
B |
D |
C |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
D |
A |
B |
B |
D |
A |
D |
A |
B |
C |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
A |
A |
C |
A |
B |
C |
A |
B |
C |
D |
Câu 2:
Hợp chất hữu cơ là hợp chất của cacbon trừ CO; CO2; muối cacbonat; axit cacbonic → chọn B.
Câu 5.
Loại A do phân tử khối của CH4 là 16 đvC.
Loại C do phân tử khối của C3H8 là 44 đvC.
Loại D do phân tử khối của C2H4 là 28 đvC.
Câu 11:
C2H2 + 2Br2 → C2H2Br4
0,1 → 0,2 mol
Khối lượng brom phản ứng: m = 0,2.160 = 32 gam.
Câu 12:
Sử dụng dung dịch brom: C2H4 làm mất màu dung dịch brom còn CH4 thì không.
Câu 15:
Các hợp chất hữu cơ: CH4; C2H4; C2H5ONa
Các hợp chất vô cơ: CO2; Na2CO3.
Câu 19.
C2H4 + Br2 → C2H4Br2
0,5 → 0,5 mol
Khối lượng dung dịch brom 5% tham gia phản ứng là:
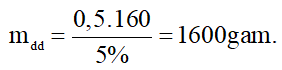
Câu 21.
C2H2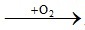 2CO2 + H2O
2CO2 + H2O
2 1 mol
Câu 22:
MX = 0,8125.32 = 26.
Vậy khí X là C2H2.
Câu 24:
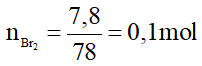

Do hiệu suất của phản ứng là 80% nên:
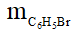 = 0,1.157.80% = 12,56 gam.
= 0,1.157.80% = 12,56 gam.
Câu 28:
CH2 = CH – CH3 có liên kết đôi, nên làm mất màu dung dịch brom.
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 9
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Câu 1. Clo tác dụng với natri hiđroxit
A. tạo thành muối natri clorua và nước.
B. tạo thành nước giaven.
C. tạo thành hỗn hợp các axit.
D. tạo muối natri hipoclorit và nước.
Câu 2. Nhóm nào sau đây gồm các chất khí đều phản ứng với dung dịch NaOH ở điều kiện thường:
Câu 3. Nguyên tử của nguyên tố X có 3 lớp electron, lớp ngoài cùng có 1 electron.
Câu trả lời nào sau đây đúng?
A. X thuộc chu kỳ 1, nhóm III, là một kim loại.
B. X thuộc chu kì 3, nhóm IV,là một phi kim.
C. X thuộc chu kì 3, nhóm IV,là một khí hiếm.
D. X thuộc chu kì 3, nhóm I, là một kim loại.
Câu 4. Dãy chất gồm toàn hợp chất hữu cơ là:
Câu 5. Biết 0,01 lít hiđrocacbon X có thể tác dụng tối đa với 100ml dung dịch brom 0,1M. X là:
Câu 6. Phản ứng đặc trưng của các chất chứa liên kết đôi, liên kết ba là
Câu 7. Tính chất vật lí chung của metan, etilen, axetilen là
A. Chất khí, không màu, mùi hắc, nhẹ hơn không khí;
B. Chất khí, không màu, tan trong nước, nặng hơn không khí;
C. Chất khí, nặng hơn không khí;
D. Chất khí, không màu, ít tan trong nước, nhẹ hơn không khí.
Câu 8. Một hợp chất hiđrocacbon có chứa 85,7% C và 14,3% H theo khối lượng.
Công thức nào sau đây là phù hợp với hiđrocacbon đó?
Câu 9. Sản phẩm chủ yếu của một hợp chất hữu cơ khi cháy là
A. khí nitơ và hơi nước. B. khí cacbonic và khí hiđro.
C. khí cacbonic và cacbon. D. khí cacbonic và hơi nước.
Câu 10. Cho các chất sau: H2O, HCl, Cl2, O2, CO2. Khí metan phản ứng được với
A. H2O, HCl. B. Cl2, O2. C. HCl, Cl2. D. O2, CO2
Câu 11. Dãy các nguyên tố được sắp xếp theo chiều tính phi kim tăng dần là:
Câu 12. Hiđrocacbon nào sau đây phản ứng cộng với dd brom?
Câu 13. Đốt cháy hoàn toàn 1,17g hợp chất hữu cơ A thu được 2,016 lít CO2 đktc và 0,81g H2O. Biết rằng số mol của A bằng số mol của 0,336 lít H2 (ở đktc). Công thức phân tử A là
Câu 14. Khối lượng khí etilen cần dùng để phản ứng hết 8g brom trong dung dịch là
Câu 15. Dẫn 1,3 gam khí axetilen qua bình đựng dung dịch brom dư. Khối lượng sản phẩm thu được sau phản ứng là:
Câu 16. Nhỏ từ từ dung dịch axit HCl vào cốc đựng một mẩu đá vôi nhỏ cho đến dư axit. Hiện tượng nào sau đây có thể quan sát được?
Câu 17. Trong các công thức hoá học sau, công thức hoá học của chất hữu cơ là
Câu 18. Đốt cháy 32g khí metan, thể tích CO2 sinh ra (ở đktc) là
Câu 19. Dẫn 1mol khí axetilen vào dung dịch chứa 2 mol brom. Hiện tượng nào sau đây đúng?
A. Không có hiện tượng gì xảy ra.
B. Màu da cam của dung dịch brom nhạt hơn so với ban đầu.
C. Màu da cam của dung dịch brom đậm hơn so với ban đầu.
D. Màu da cam của dung dịch brom chuyển thành không màu.
Câu 20. Cho 11,2 lít etilen (đktc) tác dụng với nước có axit sunfuric (H2SO4) làm xúc tác, thu được 9,2 gam rượu etylic. Hiệu suất phản ứng là:
Câu 21. Để làm khô khí CO2 cần dẫn khí này qua:
Câu 22. Trong các hợp chất hữu cơ, cacbon luôn có hoá trị là
Câu 23. Đốt cháy m gam hiđrocacbon A thu được 2,688 lít CO2 (đktc) và 4,32 g H2O. Giá trị của m là
Câu 24. Một hiđrocacbon (X) ở thể khí có phân tử khối nặng gấp đôi phân tử khối trung bình của không khí. Công thức phân tử của (X) là
Câu 25. Chất làm mất màu dung dịch nước brom là:
Câu 26. Thể tích không khí (VKK = 5VO2 ) cần dùng để đốt cháy hoàn toàn 1 lít khí etilen ở đktc là
Câu 27. Trong các phản ứng sau phản ứng hóa học đúng là
A. C6H6 +Br → C6H5Br + H
B. C6H6 + Br2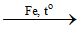 C6H5Br + HBr
C6H5Br + HBr
C. C6H6 + Br2 → C6H6Br2
D. C6H6 +2Br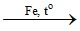 C6H5Br + HBr
C6H5Br + HBr
Câu 28. Hợp chất hữu cơ không có khả năng tham gia phản ứng cộng là
Câu 29. Khí axetilen không có tính chất hóa học nào sau đây?
Câu 30. Cho sơ đồ chuyển hóa sau:
X + H2O → Y + Z
Y + O2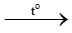 T +H2O
T +H2O
T + Ca(OH)2 → CaCO3↓ +H2O
X, Y, Z, T lần lượt là
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
B |
B |
D |
B |
B |
D |
D |
B |
D |
B |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
D |
C |
D |
D |
B |
D |
D |
D |
D |
A |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
A |
B |
A |
A |
D |
D |
B |
A |
D |
C |
Câu 2.
CO2 + 2NaOH → Na2CO3 + H2O
Cl2 + 2NaOH → NaCl + NaClO + H2O
Câu 3.
Nguyên tử X có 3 lớp electron → X thuộc chu kì 3;
Lớp ngoài cùng của X có 1 electron → X thuộc nhóm I.
Câu 4.
Loại A do CaCO3 là chất vô cơ;
Loại C do CO2 là chất vô cơ;
Loại D do CaO là chất vô cơ.
Câu 5:
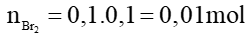
Có nX = nbrom; vậy X là C2H4.
Câu 8:
Đặt công thức của hiđrocacbon là CxHy;
Ta có:
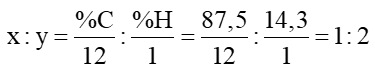
Trong 4 đáp án chỉ có C2H4 thỏa mãn.
Câu 10:
CH4 + Cl2 CH3Cl + HCl
CH3Cl + HCl
CH4 + 2O2 CO2 + 2H2O
CO2 + 2H2O
Câu 11:
Ta có Si; P; S; Cl thuộc cùng một chu kì trong bảng tuần hoàn.
Trong một chu kì, theo chiều tăng của điện tích hạt nhân, tính phi kim tăng dần.
Vậy dãy sắp xếp theo chiều tăng dần tính phi kim là: Si; P; S; Cl.
Câu 13:
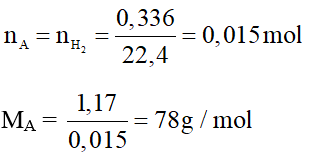
Đốt cháy A thu được CO2; H2O nên trong A có C; H và có thể có O
Có:
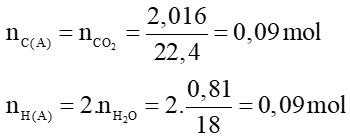
→ mC(A) + mH(A) = 0,09.12 + 0,09 = 1,17 gam = mA
Vậy trong A không có O
Đặt công thức phân tử của A có dạng: CxHy
Ta có: x : y = nC(A) : nH(A) = 0,09 : 0,09 = 1 : 1
Vậy A có dạng: (CH)n
Lại có MA = 78 → 13n = 78 → n = 6
Vậy A là C6H6.
Câu 14:
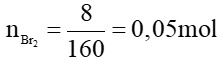
C2H4 + Br2 → C2H4Br2
0,05 ← 0,05 mol
→ metilen = 0,05.28 =1,4 gam.
Câu 15.
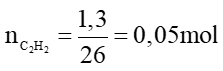
C2H2 + 2Br2 → C2H2Br4
0,05 → 0,05 mol
→ m sản phẩm = 0,05.346 = 17,3 gam.
Câu 16.
Đá vôi: CaCO3
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
Hiện tượng: Sủi bọt khí; đá vôi tan dần và tan hết.
Câu 17.
Hợp chất hữu cơ là hợp chất của cacbon trừ CO2; CO; muối cacbonat; axit cacbonic …Vậy CH3Cl là hợp chất hữu cơ.
Câu 18:
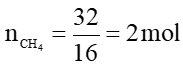
CH4 + 2O2 → CO2 + 2H2O
2 → 2 mol
Vkhí CO2 = 2.22,4 = 44,8 lít.
Câu 19:
C2H2 + 2Br2(cam) → C2H2Br4 (không màu)
1 → 2 mol
Câu 20.
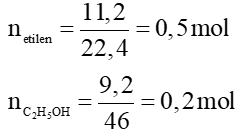
C2H4 + H2O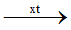 C2H5OH
C2H5OH
0,5 → 0,5 mol
Hiệu suất phản ứng:
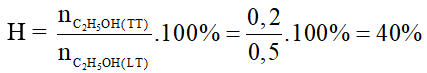
Câu 23:
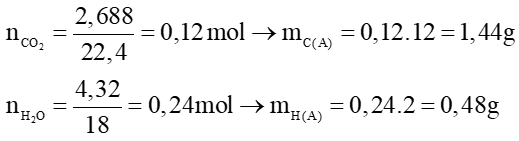
→ mA = mC(A) + mH(A) = 1,44 + 0,48 = 1,92 gam.
Câu 24:
MX = 29.2 = 58 đvC. Vậy X là C4H10.
Câu 26.
C2H4 + 3O2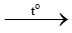 2CO2 + 2H2O
2CO2 + 2H2O
1 → 3 lít
→ VKK = 5.3 = 15 lít.
Câu 30:
CaC2 (X) + 2H2O → Ca(OH)2 (Z) + C2H2 (Y)
2C2H2 + 5O2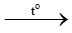 4CO2 (T) + 2H2O
4CO2 (T) + 2H2O
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 10
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Phần I: Trắc nghiệm khách quan (3 điểm)
Câu 1: Metan có nhiều trong
A. nước ao. B. các mỏ (khí, dầu, than).
C. nước biển. D. khí quyển.
Câu 2: Hiđrocacbon nào sau đây chỉ có liên kết đơn?
A. Metan. B. Axetilen. C. Etilen. D. Etan.
Câu 3: Dãy chất nào sau đây đều là hiđrocacbon:
A. C2H4, C3H8, C2H4O2, CH3Cl.
B. C3H8, C2H5O, CH3CH2COOH, CaCO3.
C. C2H6, C4H10, CH3NO2, C2H5Cl.
D. CH4, C4H10, C2H2, C2H6.
Câu 4: Phản ứng nào sau đây thuộc loại phản ứng trùng hợp:
A. C2H4 + 3O2 → 2CO2 + 2H2O
B. CH2 = CH2 + Br2 → BrCH2 - CH2Br
C. nCH2 = CH2 → (-CH2-CH2-)n
D. CH4 + Cl2 → CH3Cl + HCl
Câu 5: Đốt cháy hoàn toàn 0,224 lit khí metan ở điều kiện tiêu chuẩn thu được lượng khí CO2 ở cùng điều kiện là:
A. 2,24 lit B. 0,672 lit C. 0,224 lit. D. 0,112 lit
Câu 6: Trong những chất sau, những chất nào đều là chất hữu cơ:
A. C2H6, C2H5OH, NaHCO3.
B. C3H8, C2H5O, Na2CO3.
C. C2H6 , C2H5OH, CaCO3.
D. C2H6 , C4H10, C2H5OH.
Câu 7: Chất có liên kết ba trong phân tử là:
A. CH4. B. C2H4. C. C2H2. D. C2H6.
Câu 8: Cấu tạo phân tử axetilen gồm:
A. hai liên kết đơn và một liên kết ba.
B. hai liên kết đơn và một liên kết đôi.
C. một liên kết ba và một liên kết đôi.
D. hai liên kết đôi và một liên kết ba.
Câu 9: Chất dùng để kích thích cho quả mau chín là:
A. CH4. B. C2H4. C. C2H2. D. C6H6.
Câu 10: Khí metan phản ứng được với:
A. HCl, H2O. B. HCl, Cl2. C. Cl2, O2. D. O2, CO2.
Câu 11: Hóa chất dùng để loại bỏ khí etilen có lẫn trong khí metan để thu được khí metan tinh khiết là
A. dung dịch brom.
B. dung dịch phenolphtalein.
C. dung dịch axit clohidric.
D. dung dịch nước vôi trong.
Câu 12: Dãy chất nào sau đây đều là dẫn xuất của hiđrocacbon?
A. C2H6O, C2H4O2, C6H12O6 . B. C2H4O2, Na2CO3, C2H4.
C. CH4, C2H2, C6H6. D. CO2, CH4, C2H4O2.
Câu 13: Nhóm gồm các chất khí đều khử được CuO ở nhiệt độ cao là
A. CO, H2. B. Cl2, CO2.
C. CO, CO2. D. Cl2, CO.
Câu 14: Cho 21 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M. Thể tích dung dịch HCl đã dùng là
A. 0,50 lít. B. 0,25 lít.
C. 0,75 lít. D. 0,15 lít.
Câu 15: Biết X có cấu tạo nguyên tử như sau: điện tích hạt nhân là 13+, có 3 lớp electron, lớp ngoài cùng có 3 electron. Vị trí của X trong bảng tuần hoàn là
A. chu kỳ 3, nhóm II. B. chu kỳ 3, nhóm III.
C. chu kỳ 2, nhóm II. D. chu kỳ 2, nhóm III.
B. Tự luận: (7,0 điểm)
Câu 1: (2,0 điểm) Viết các phương trình hóa học xảy ra trong các trường hợp sau:
a/ Metan tác dụng với clo khi có ánh sáng.
b/ Đốt cháy axetilen.
c/ Cho axetilen tác dụng với lượng dư dung dịch brom.
d/ Trùng hợp etilen.
Câu 2: (2,0 điểm) Đốt cháy hoàn toàn 5,6 lít etilen. Hãy tính thể tích khí oxi và thể tích không khí cần dùng cho phản ứng, biết rằng oxi chiếm 20% thể tích không khí (các thể tích khí đo ở đktc).
Câu 3: (3,0 điểm) Khi cho hỗn hợp khí metan và etilen ở (đktc) đi qua bình đựng dung dịch brom, thì lượng brom tham gia phản ứng là 8g.
a/ Khí nào ở trên đã phản ứng với dung dịch brom?
b/ Khối lượng khí đó đã phản ứng là bao nhiêu?
ĐÁP ÁN ĐỀ KIỂM TRA GIỮA HỌC KÌ 2 MÔN HÓA HỌC LỚP 9
Phần I. Trắc nghiệm khách quan (3,0 điểm)
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
Đáp án |
B |
A |
D |
C |
C |
D |
C |
A |
B |
C |
A |
A |
A |
B |
B |
Câu 5.
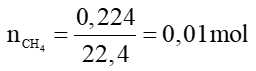
CH4 + 2O2 CO2 + 2H2O
CO2 + 2H2O
0,01 0,01 mol
VCO2 = 0,01.22,4 = 0,224 lít.
Câu 6:
Loại A, B, C do các chất NaHCO3; Na2CO3; CaCO3 đều là muối cabonat (thuộc loại hợp chất vô cơ).
Câu 11:
Sử dụng một lượng dư dung dịch brom, khí etilen phản ứng bị giữ lại, còn metan không phản ứng thoát ra khỏi dung dịch thu được metan tinh khiết.
C2H4 + Br2 → C2H4Br2.
Câu 13:
CO + CuO  Cu + CO2
Cu + CO2
H2 + CuO  Cu + H2O
Cu + H2O
Câu 14:
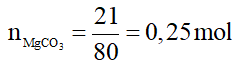
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
0,25 → 0,5 mol
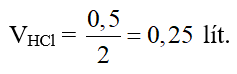
Câu 15:
X có 3 lớp electron → X thuộc chu kì 3;
Lớp ngoài cùng của X có 3 electron → X thuộc nhóm III.
Phần II. Tự luận (7,0 điểm)
Câu 1:
a/ CH4 + Cl2 CH3Cl + HCl
CH3Cl + HCl
b/ 2C2H2 + 5O2 4CO2 + 2H2O
4CO2 + 2H2O
c/ CH ≡ CH + 2Br2 → Br2CH – CHBr2
d/ nCH2 = CH2 ( − CH2 − CH2 − )n
( − CH2 − CH2 − )n
Câu 2:
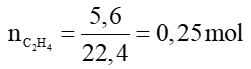
C2H4 + 3O2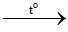 2CO2+ 2H2O
2CO2+ 2H2O
0,25 → 0,75 mol
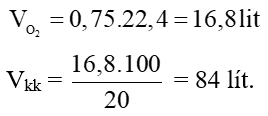
Câu 3:
a/ Khi cho hỗn hợp metan và etilen qua bình đựng dung dịch brom chỉ có etilen phản ứng.
b/ 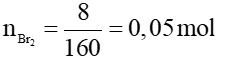
Phương trình hóa học:
C2H4 + Br2 → C2H4Br2
0,05 ← 0,05 mol
Khối lượng etilen: m = 0,05.28 = 1,4 gam.
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 11
I. TRẮC NGHIỆM (2 điểm): Hãy chọn đáp án đúng sau đó ghi vào bảng bên dưới
Câu 1: : Sản phẩm giữa rượu etylic và axitaxetic gọi là
A. ete.
B. este.
C. hợp chất vô cơ.
D. axit.
Câu 2: Số ml nước có trong 100ml rượu 450 là
A. 100ml.
B. 45ml.
C. 55 ml.
D. 145 ml.
Câu 3: Để tác dụng được với kim loại Zn và giải phóng khí hidro thì chất đó là
A. C6H6.
B.CH3COOH.
C. C2H5OH.
D. C2H4.
Câu 4: Để trung hòa 10ml dung dịch CH3COOH cần 15,2 ml dung dịch NaOH 0,2M. Vậy nồng độ của dung dịch CH3COOH là
A. 0,05 M.
B. 0,10 M.
C. 0,304 M.
D. 0,215 M.
Câu 5: Công thức của chất béo là
A. RCOOC3H5.
B. (RCOO)3C3H5 .
C. C3H5(OH)3.
D. R-COOH.
Câu 6: Cho các chất: Mg, CuO, CaCO3, C2H5OH, NaOH, Cu. Số chất tác dụng với axitaxetic là
A. 3.
B.2.
C. 5.
D. 4.
Câu 7: CH3COOC2H5 có tên gọi là:
A.natri axetat .
B.etyl axetat.
C. metyl axetat.
D. axit axetic.
Câu 8: Số ml Rượu Etylic có trong 200ml rượu Etylic 450 là
A. 90ml.
B.225ml.
C. 200ml.
D. 45ml.
II. TỰ LUẬN (8 điểm)
Câu 9: (2 điểm): Độ rượu là gì?
Áp dụng: Tính độ rượu khi hòa tan 50ml rượu etylic vào 250ml nước?
Câu 10: (2 điểm): Hoàn thành chuỗi phản ứng sau và ghi điều kiện phản ứng nếu có?
C2H4 →C2H5OH →CH3COOH →CH3COOC2H5 →CH3COOH
Câu 11: (2 điểm): Hoàn thành phương trình phản ứng sau:
a. C2H5OH + ? →? + H2
b. CH3COOH + →?(CH3COO)2Mg + ?
c. Etyl axetat + NaOH →
d. (RCOO)3 →C3H5+ H2O
Câu 12: (2 điểm): Cho 19,5 gam Zn vào 150g dung dịch axitaxetic12%.
a. Tính thể tích khí hiđro thu được ở ĐKTC?
b. Tính khối lượng chất rắn còn lại sau phản ứng?
(Cho biết Zn = 65; C = 12; H= 1; O = 16)
Đáp án đề kiểm tra giữa kì 2 Hóa 9
I. TRẮC NGHIỆM: (2 điểm)Mỗi câu đúng 0,25 điểm
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Đáp án | B | B | B | C | B | C | B | A |
II. TỰ LUẬN : (8 điểm)
| Câu | Trả lời | Điểm |
|
9 (2 điểm) |
Độ rượu là số ml rượu nguyên chất có trong 100ml hỗn hợp rượu và nước. Hỗn hợp rượu và nước= 50 ml + 250ml = 300ml Trong 300ml hỗn hợp rượu và nước có 50ml rượu nguyên chất Trong 100ml hỗn hợp rượu và nước có rượu nguyên chất Vậy độ rượu là 16,66 |
1 đ
1đ |
|
10 (2 điểm) |
1. C2H4 + H2O →C2H5OH 2. C2H5OH + O2 →CH3COOH + H2O 3. CH3COOH + C2H5OH →CH3COOC2H5 + H2O 4. CH3COOC2H5 + H2O →2CH3COOH + C2H5OH - Mỗi phương trình đạt 0,5 điểm - Không cân bằng hoặc cân bằng sai trừ 0,25 số điểm của mỗi câu. - Viết công thức sai không tính điểm cho câu đó. - Viết phương trình khác nếu đúng đạt điểm tối đa |
0,5 điểm 0,5 điểm
0,5 điểm
0,5 điểm |
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 12
A. Trắc nghiệm khách quan: (4,0 điểm)
Câu 1. Phản ứng hóa học đặc trưng của metan là:
A. Phản ứng thế.
B. Phản ứng cộng
C. Phản ứng oxi hóa – khử.
D. Phản ứng phân hủy.
Câu 2. Điều kiện để phản ứng giữa Metan và Clo xảy ra là:
A. Có bột sắt làm xúc tác
B. Có axit làm xúc tác
C. Có nhiệt độ
D. Có ánh sáng
Câu 3. Dãy chất nào sau đây đều là hidrocacbon:
A. C2H4, C3H8, C2H4O2, CH3Br
B. C3H8, C2H5O, CH3CH2COOH, CaCO3
C. C2H6, C4H10, CH3NO2, C2H5Cl
D. CH4, C5H12, C2H2, C2H6
Câu 4. Phản ứng nào sau đây thuộc loại phản ứng trùng hợp:
A. C2H4 + 3O2 → 2CO2 + 2H2O
B. CH2 = CH2 + Br2 → BrCH2 - CH2Br
C. nCH2 = CH2 → (-CH2-CH2-)n
D. CH4 + Cl2 → CH3Cl + HCl
Câu 5. Chất nào sau đây có chứa liên kết ba trong phân tử
A. Metan.
B. Etilen.
C. Axetilen.
D. Propan.
Câu 6. Khi cho etilen tác dụng với nước (có xúc tác) thu được
A. Ancol etylic (C2H5OH)
B. Etan (C2H6)
C. Axit axetic (CH3COOH)
D. Etilen oxit (C2H4O)
Câu 7. Khí axetilen không có tính chất hóa học nào sau đây?
A. Phản ứng cộng với dung dịch brom
B. Phản ứng cháy với oxi.
C. Phản ứng cộng với hiđro.
D. Phản ứng thế với clo ngoài ánh sáng.
Câu 8. Đốt cháy một hỗn hợp hiđrocacbon ta thu được 2,24 lít CO2 (đktc) và 2,7 gam H2O thì thể tích O2 đã tham gia phản ứng cháy (đktc) là:
A. 3,92 lít.
B. 2,8 lít.
C. 4,48 lít.
D. 5,6 lít.
Câu 9. Trong phòng thí nghiệm, etilen thường được điều chế bằng cách.
A. nung nóng etan để tách hidro
B. tách từ khí mỏ dầu
C. tách nước của ancol etylic
D. Cracking dầu mỏ
Câu 10: Chất nào sau đây làm mất màu dung dịch Brom
A. metylpropan
B. cacbon đioxit
C. butan
D. but-1-en
Câu 11: Để làm sạch Etilen có lẫn Axetilen ta cho hỗn hợp đi qua dung dịch nào sau đây
A. dung dịch KMnO4 dư.
B. dung dịch brom dư.
C. dung dịch AgNO3/NH3 dư.
D. các cách trên đều đúng.
Câu 12. Đốt cháy V lít etilen thu được 3,6g hơi nước. Biết rằng oxi chiếm 20% thể tích không khí. Vậy thể tích không khí ở đktc cần dùng là:
A. 336 lít
B. 3,36 lít.
C. 33,6 lít
D. 0,336 lít.
B. Tự luận: (7,0 điểm)
Câu 1. (2,0 điểm)
Hoàn thành chuỗi phản ứng hóa học sau:
CH4 → C2H2 → C2H4 → C2H6 → C2H5Cl
Câu 2. (2,5 điểm)
Đốt cháy hoàn toàn 5,75 gam hợp chất hữu cơ X (chứa C, H, O) thu được 11,0 gam CO2 và 6,75 gam H2O.
a) Tính thành phần phần trăm của các nguyên tố trong X.
b) Lập công thức đơn giản nhất của X.
c) Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với khí hiđro bằng 23.
Câu 3. (1,5 điểm)
Cho 5,6 lít hỗn hợp khí X (đktc) gồm CH4 và C2H4 có tỉ lệ thể tích là 3 : 2 qua dung dịch chứa m gam dung dịch brom 40%. Tìm giá trị m.
Đáp án đề thi giữa kì 2 Hóa 9
A. Trắc nghiệm khách quan (3,0 điểm)
| 1A | 2D | 3D | 4B | 5C | 6A |
| 7D | 8A | 9C | 10D | 11C | 12C |
B. Tự luận (7,0 điểm)
Câu 1.
2CH4 C2H2 + 3H2
C2H2+ H2 C2H4
C2H4 + H2 C2H6
C2H6 + Cl2 → C2H5Cl + HCl
Câu 2.
nC= nCO2 = 0,25 => %C = (0,25 . 12/5,75).100 = 52,17%
nH = 2nH2O = 0,75 => %H = (0,75 .1/5,75). 100 = 13,04%
=> %O = 34,79%
nO = ( mX - mC - mH )/16 = 0,125
X là CxHyOz
=> x : y : z = nC : nH : nO= 0,25 : 0,75 : 0,125 = 2 : 6 : 1
Công thức đơn giản nhất: C2H6O
Công thức phân tử: (C2H6O )n
=> MX = 46n = 23,2
=> n = 1
X là C2H6O
Câu 3.
Gọi số mol CH4 và C2H4 lần lượt là 3a và 2a.
=> nX = 5a = 5,6/22,4 = 0,25 ⟹ a = 0,05 (mol).
Phương trình hóa học phản ứng xảy ra
C2H4 + Br2 ⟶ C2H4Br2
Theo phương trình hóa học ta có:
nBr2 = nC2H4 = 0,05.2 = 0,1 mol.
=> mBr2 = 0,1.160 = 16 gam.
Vậy m = (16.100%)/40% = 40 gam.
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 13
Phần I: Trắc nghiệm khách quan (3 điểm)
Câu 1: Metan có nhiều trong
A. nước ao.
B. các mỏ (khí, dầu, than).
C. nước biển.
D. khí quyển.
Câu 2: Hiđrocacbon nào sau đây chỉ có liên kết đơn?
A. Metan.
B. Axetilen.
C. Etilen.
D. Etan.
Câu 3: Dãy chất nào sau đây đều là hiđrocacbon:
A. C2H4, C3H8, C2H4O2, CH3Cl.
B. C3H8, C2H5O, CH3CH2COOH, CaCO3.
C. C2H6, C4H10, CH3NO2, C2H5Cl.
D. CH4, C4H10, C2H2, C2H6.
Câu 4: Phản ứng nào sau đây thuộc loại phản ứng trùng hợp:
A. C2H4 + 3O2 → 2CO2 + 2H2O
B. CH2 = CH2 + Br2 → BrCH2 - CH2Br
C. nCH2 = CH2 → (-CH2-CH2-)n
D. CH4 + Cl2 → CH3Cl + HCl
Câu 5: Đốt cháy hoàn toàn 0,224 lit khí metan ở điều kiện tiêu chuẩn thu được lượng khí CO2 ở cùng điều kiện là:
A. 2,24 lit
B. 0,672 lit
C. 0,224 lit.
D. 0,112 lit
Câu 6: Trong những chất sau, những chất nào đều là chất hữu cơ:
A. C2H6, C2H5OH, NaHCO3.
B. C3H8, C2H5O, Na2CO3.
C. C2H6 , C2H5OH, CaCO3.
D. C2H6 , C4H10, C2H5OH.
Câu 7: Chất có liên kết ba trong phân tử là:
A. CH4.
B. C2H4.
C. C2H2.
D. C2H6.
Câu 8: Cấu tạo phân tử axetilen gồm:
A. hai liên kết đơn và một liên kết ba.
B. hai liên kết đơn và một liên kết đôi.
C. một liên kết ba và một liên kết đôi.
D. hai liên kết đôi và một liên kết ba.
Câu 9: Chất dùng để kích thích cho quả mau chín là:
A. CH4.
B. C2H4.
C. C2H2.
D. C6H6.
Câu 10: Khí metan phản ứng được với:
A. HCl, H2O.
B. HCl, Cl2.
C. Cl2, O2.
D. O2, CO2.
Câu 11: Hóa chất dùng để loại bỏ khí etilen có lẫn trong khí metan để thu được khí metan tinh khiết là
A. dung dịch brom.
B. dung dịch phenolphtalein.
C. dung dịch axit clohidric.
D. dung dịch nước vôi trong.
Câu 12: Dãy chất nào sau đây đều là dẫn xuất của hiđrocacbon?
A. C2H6O, C2H4O2, C6H12O6 .
B. C2H4O2, Na2CO3, C2H4.
C. CH4, C2H2, C6H6.
D. CO2, CH4, C2H4O2.
Câu 13: Nhóm gồm các chất khí đều khử được CuO ở nhiệt độ cao là
A. CO, H2.
B. Cl2, CO2.
C. CO, CO2.
D. Cl2, CO.
Câu 14: Cho 21 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M. Thể tích dung dịch HCl đã dùng là
A. 0,50 lít.
B. 0,25 lít.
C. 0,75 lít.
D. 0,15 lít.
Câu 15: Biết X có cấu tạo nguyên tử như sau: điện tích hạt nhân là 13+, có 3 lớp electron, lớp ngoài cùng có 3 electron. Vị trí của X trong bảng tuần hoàn là
A. chu kỳ 3, nhóm II.
B. chu kỳ 3, nhóm III.
C. chu kỳ 2, nhóm II.
D. chu kỳ 2, nhóm III.
B. Tự luận: (7,0 điểm)
Câu 1: (2,0 điểm) Viết các phương trình hóa học xảy ra trong các trường hợp sau:
a/ Metan tác dụng với clo khi có ánh sáng.
b/ Đốt cháy axetilen.
c/ Cho axetilen tác dụng với lượng dư dung dịch brom.
d/ Trùng hợp etilen.
Câu 2: (2,0 điểm) Đốt cháy hoàn toàn 5,6 lít etilen. Hãy tính thể tích khí oxi và thể tích không khí cần dùng cho phản ứng, biết rằng oxi chiếm 20% thể tích không khí (các thể tích khí đo ở đktc).
Câu 3: (3,0 điểm) Khi cho hỗn hợp khí metan và etilen ở (đktc) đi qua bình đựng dung dịch brom, thì lượng brom tham gia phản ứng là 8g.
a/ Khí nào ở trên đã phản ứng với dung dịch brom?
b/ Khối lượng khí đó đã phản ứng là bao nhiêu?
Đáp án chi tiết
Phần I. Trắc nghiệm khách quan (3,0 điểm)
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
Đáp án |
B |
A |
D |
C |
C |
D |
C |
A |
B |
C |
A |
A |
A |
B |
B |
Câu 5.
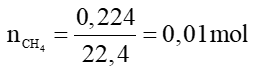
CH4 + 2O2 CO2 + 2H2O
CO2 + 2H2O
0,01 0,01 mol
VCO2 = 0,01.22,4 = 0,224 lít.
Câu 6:
Loại A, B, C do các chất NaHCO3; Na2CO3; CaCO3 đều là muối cabonat (thuộc loại hợp chất vô cơ).
Câu 11:
Sử dụng một lượng dư dung dịch brom, khí etilen phản ứng bị giữ lại, còn metan không phản ứng thoát ra khỏi dung dịch thu được metan tinh khiết.
C2H4 + Br2 → C2H4Br2.
Câu 13:
CO + CuO  Cu + CO2
Cu + CO2
H2 + CuO  Cu + H2O
Cu + H2O
Câu 14:
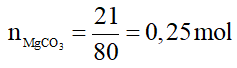
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
0,25 → 0,5 mol
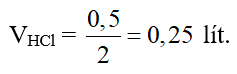
Câu 15:
X có 3 lớp electron → X thuộc chu kì 3;
Lớp ngoài cùng của X có 3 electron → X thuộc nhóm III.
Phần II. Tự luận (7,0 điểm)
Câu 1:
a/ CH4 + Cl2 CH3Cl + HCl
CH3Cl + HCl
b/ 2C2H2 + 5O2 4CO2 + 2H2O
4CO2 + 2H2O
c/ CH ≡ CH + 2Br2 → Br2CH – CHBr2
d/ nCH2 = CH2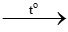 ( − CH2 − CH2 − )n
( − CH2 − CH2 − )n
Câu 2:
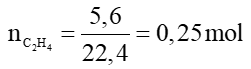
C2H4 + 3O2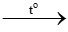 2CO2+ 2H2O
2CO2+ 2H2O
0,25 → 0,75 mol
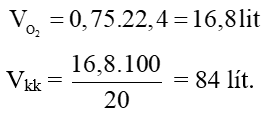
Câu 3:
a/ Khi cho hỗn hợp metan và etilen qua bình đựng dung dịch brom chỉ có etilen phản ứng.
b/ 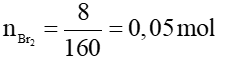
Phương trình hóa học:
C2H4 + Br2 → C2H4Br2
0,05 ← 0,05 mol
Khối lượng etilen: m = 0,05.28 = 1,4 gam.
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 14
A – Phần trắc nghiệm (3 điểm)
Câu 1: Dãy gồm các phi kim thể khí ở điều kiện thường là
A. S, P, N2, Cl2.
B. C, S, Br2, Cl2.
C. Cl2, H2, N2, O2.
D. Br2, Cl2, N2, O2.
Câu 2: Chất nào sau đây khi cháy tạo ra oxit ở thể khí ?
A. Canxi.
B. Silic.
C. Cacbon.
D. Magie.
Câu 3: Nguyên tử của nguyên tố X có 2 lớp electron, lớp electron ngoài cùng có 7 electron. Vị trí và tính chất cơ bản của nguyên tố X là
A. thuộc chu kỳ 2, nhóm VII là kim loại mạnh.
B. thuộc chu kỳ 7, nhóm III là kim loại yếu.
C. thuộc chu kỳ 2, nhóm VII là phi kim mạnh.
D. thuộc chu kỳ 2, nhóm VII là phi kim yếu.
Câu 4: Chất hữu cơ nào sau đây, khi cháy tạo thành số mol khí CO2 nhỏ hơn số mol hơi nước ?
A. CH4
B. C2H4
C. C2H2
D. C6H6
Câu 5: Hiđrocacbon X có thành phần phần trăm về khối lượng nguyên tố cacbon trong hợp chất là 85,7 %. X là
A. CH4.
B. CH3Cl.
C. C2H4.
D. C2H6.
Câu 6: Dãy các chất nào sau đây đều làm mất màu dung dịch brom?
A. CH4; C6H6.
B. C2H4; CH4.
C. CH4; C2H4.
D. C2H4; C2H2.
Câu 7: Đốt cháy hoàn toàn 1 mol khí axetilen thì cần bao nhiêu lít không khí (các khí đo ở đktc, biết rằng oxi chiếm 20% thể tích không khí) ?
A. 300 lít.
B. 280 lít.
C. 240 lít.
D. 120 lít.
Câu 8: Trong các hiđrocacbon sau khi đốt hiđrocacbon nào sinh ra nhiều muội than ?
A. C2H6
B. CH4
C. C2H4
D. C6H6
Câu 9: Trong các loại than dưới đây, loại than trẻ nhất có hàm lượng cacbon thấp nhất là
A. than gầy.
B. than mỡ.
C. than non.
D. than bùn.
Câu 10: Khí tham gia phản ứng trùng hợp là
A. CH4.
B. C2H4.
C. C3H8.
D. C2H6.
B – Phần II: Tự luận (7 điểm)
Câu 1 : (2,0 điểm) Dẫn 11,2 lít hỗn hợp khí gồm C2H4; C2H2 vào lượng dư dung dịch Br2 thấy có 0,7 mol Br2 tham gia phản ứng. Tính phần trăm thể tích của mỗi khí trong hỗn hợp ban đầu (biết thể tích các khí đều đo ở đktc)
Câu 2 (2 điểm). Nêu phương pháp làm sạch khí C2H2 bị lẫn các khí CO2 và SO2. Viết các phương trình phản ứng hoá học xảy ra (nếu có).
Câu 3 (3 điểm): Khi đốt hoàn toàn 3 gam một hợp chất hữu cơ A thu được 8,8 gam CO2 và 5,4 gam H2O
a) Trong A có chứa những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Xác định công thức phân tử của A?
c) A có làm mất màu dung dịch brom không?
Đáp án chi tiết:
Phần A – Trắc nghiệm
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
C |
C |
A |
C |
D |
B |
D |
D |
B |
Câu 3:
Nguyên tử của nguyên tố X có 2 lớp electron → X thuộc chu kỳ 2;
Lớp ngoài cùng của X có 7 electron → X thuộc nhóm VII;
X thuộc chu kì 2; nhóm VII nên là phi kim mạnh.
Câu 4:
CH4 + 2O2 CO2 + 2H2O
CO2 + 2H2O
1 → 1 2 mol
Vậy đốt cháy metan thu được số mol CO2 nhỏ hơn số mol nước.
Câu 5:
Đặt X có dạng CxHy
Theo bài ra, ta có:
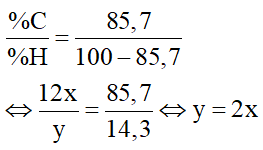
Trong 4 đáp án chỉ có C2H4 thỏa mãn.
Câu 7.
2C2H2 + 5O2 4CO2 + 2H2O
4CO2 + 2H2O
1 → 2,5 mol
→ Voxi = 2,5.22,4 = 56 lít
→ Vkhông khí = 56.5 = 280 lít.
Phần B – Tự luận
Câu 1:
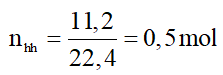
Đặt số mol của C2H4 và C2H2 trong hỗn hợp lần lượt là x và y (mol);
Ta có: x + y = 0,5 (1)
Phương trình hóa học:
C2H4 + Br2 → C2H4Br2
x → x mol
C2H2 + 2Br2 → C2H2Br4
y → 2y mol
Từ các PTHH có: x + 2y = 0,7 (2)
Từ (1) và (2) có x = 0,3 và y = 0,2
Do các khí ở cùng điều kiện nên tỉ lệ về thể tích cũng là tỉ lệ về số mol;
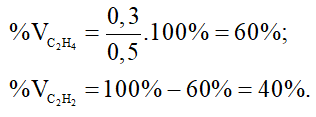
Câu 2:
Dẫn hỗn hợp khí qua bình đựng nước vôi trong; dư.
Khí CO2; SO2 phản ứng bị giữ lại; khí C2H2 không phản ứng thoát ra khỏi dung dịch thu được C2H2 tinh khiết.
Phương trình hóa học:
CO2 + Ca(OH)2→ CaCO3 + H2O
SO2 + Ca(OH)2 → CaSO3 + H2O
Câu 3:
a)
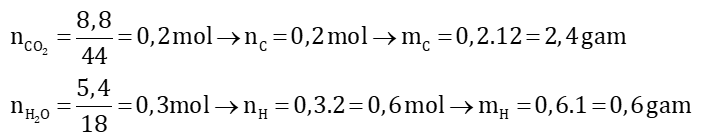
→ mO = 3 – (mC + mH) = 3 – 2,4 – 0,6 = 0
→ A chỉ chứa 2 nguyên tố C và H
b)
nC : nH = 0,2 : 0,6 = 1 : 3
→ Công thức đơn giản nhất của A: (CH3)n
MA < 40 → 15n < 40 → n < 2,67 → n chỉ có thể là 1 hoặc 2
TH 1: n = 1 → Công thức phân tử của A là CH3 ( Loại)
TH 2: n = 2 → Công thức phân tử của A là C2H6 ( thỏa mãn)
c) C2H6 có công thức cấu tạo:
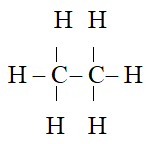
Phân tử chỉ chưa liên kết đơn nên không làm mất màu dung dịch brom.
Phòng Giáo dục và Đào tạo .....
Đề khảo sát chất lượng Giữa Học kì 2
Năm học ...
Môn: Hóa học 9
Thời gian làm bài: 45 phút
Đề thi Giữa Học kì 2 Hoá học lớp 9 có đáp án đề số 15
Câu 1: Ở điều kiện thường, phi kim có thể tồn tại ở trạng thái
A. Lỏng và khí.
B. Rắn và lỏng.
C. Rắn và khí.
D. Rắn, lỏng, khí.
Câu 2: Dãy hợp chất nào sau đây chỉ chứa các chất hữu cơ?
A. CH4, C2H6, CO2.
B. C6H6, CH4, C2H5OH.
C. CH4, C2H2, CO.
D. C2H2, C2H6O, CaCO3.
Câu 3: Hoá trị của cacbon, oxi, hiđro trong hợp chất hữu cơ lần lượt là
A. IV, II, II. B. IV, III, I.
C. II, IV, I. D. IV, II, I.
Câu 4: Nguyên tử cacbon có thể liên kết trực tiếp với nhau tạo thành các dạng mạch cacbon là
A. Mạch vòng.
B. Mạch thẳng, mạch nhánh.
C. Mạch vòng, mạch thẳng, mạch nhánh.
D. Mạch nhánh.
Câu 5: Hiđrocacbon A có phân tử khối là 30 đvC. Công thức phân tử của A là
A. CH4.
B. C2H6.
C. C3H8.
D. C2H4.
Câu 6: Tính chất vật lí cơ bản của metan là
A. Chất lỏng, không màu, tan nhiều trong nước.
B. Chất khí, không màu, tan nhiều trong nước.
C. Chất khí, không màu, không mùi, nặng hơn không khí, ít tan trong nước.
D. Chất khí, không màu, không mùi, nhẹ hơn không khí, ít tan trong nước.
Câu 7: Phản ứng đặc trưng của metan là
A. Phản ứng cộng.
B. Phản ứng thế.
C. Phản ứng trùng hợp.
D. Phản ứng cháy
Câu 8: Trong phân tử etilen giữa hai nguyên tử cacbon có
A. Một liên kết đơn.
B. Một liên kết đôi.
C. Hai liên kết đôi.
D. Một liên kết ba.
Câu 9: Khí etilen không có tính chất hóa học nào sau đây?
A. Phản ứng cháy với khí oxi.
B. Phản ứng trùng hợp.
C. Phản ứng cộng với dung dịch brom.
D. Phản ứng thế với clo ngoài ánh sáng.
Câu 10: Liên kết C≡C trong phân tử axetilen có đặc điểm
A. Một liên kết kém bền dễ đứt ra trong các phản ứng hóa học.
B. Hai liên kết kém bền nhưng chỉ có một liên kết bị đứt ra trong phản ứng hóa học.
C. Hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
D. Ba liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 11: Dẫn 0,1 mol khí axetilen qua dung dịch nước brom dư. Khối lượng brom tham gia phản ứng là
A. 16,0 gam.
B. 20,0 gam.
C. 26,0 gam.
D. 32,0 gam.
Câu 12: Hoá chất nào sau đây dùng để phân biệt 2 chất CH4 và C2H4?
A. Dung dịch brom.
B. Dung dịch phenolphtalein.
C. Qùy tím.
D. Dung dịch bari clorua.
Câu 13: Cho khí metan tác dụng với khí oxi theo phản ứng sau:
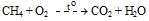
Tổng hệ số cân bằng trong phương trình hoá học là (biết hệ số cân bằng là các số nguyên tối giản)
A. 5.
B. 6.
C. 7.
D. 8.
Câu 13:
CH4 + 2O2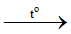 CO2 + 2H2O
CO2 + 2H2O
Tổng hệ số cân bằng: 1 + 2 + 1 + 2 = 6.
Câu 14: Hợp chất hữu cơ không có khả năng tham gia phản ứng cộng là
A. metan.
B. benzen.
C. etilen.
D. axetilen.
Câu 15: Trong các chất sau: CH4, CO2, C2H4, Na2CO3, C2H5ONa có
A. 1 hợp chất hữu cơ và 4 hợp chất vô cơ.
B. 2 hợp chất hữu cơ và 3 hợp chất vô cơ.
C. 4 hợp chất hữu cơ và 1 hợp chất vơ cơ.
D. 3 hợp chất hữu cơ và 2 hợp chất vô cơ.
Câu 16: Dãy các chất nào sau đây đều là hiđrocacbon?
A. C2H6, C4H10, C2H4.
B. CH4, C2H2, C3H7Cl.
C. C2H4, CH4, C2H5Cl.
D. C2H6O, C3H8, C2H2.
Câu 17: Phương trình hóa học điều chế nước Gia - ven là
A. Cl2 + NaOH → NaCl + HClO
B. Cl2 + NaOH → NaClO + HCl
C. Cl2 + H2O → HCl + HClO
D. Cl2 + 2NaOH → NaCl + NaClO + H2O
Câu 18: Chất khí nào sau đây có thể gây chết người vì ngăn cản sự vận chuyển oxi trong máu?
A. CO.
B. CO2.
C. SO2.
D. NO.
Câu 19: Cho 11,2 lít khí etilen (đktc) phản ứng vừa đủ với dung dịch brom 5%. Khối lượng dung dịch brom tham gia phản ứng là
A. 160 gam.
B. 1600 gam.
C. 320 gam.
D. 3200 gam.
Câu 20: Một hiđrocacbon ở thể khí thường được dùng làm nhiên liệu để hàn cắt kim loại, đó là
A. metan.
B. etilen.
C. axetilen.
D. etan.
Câu 21: Khi đốt khí axetilen, số mol CO2 và H2O được tạo thành theo tỉ lệ là
A. 2 : 1.
B. 1 : 2.
C. 1 : 3.
D. 1 : 1.
Câu 22: Khí X có tỉ khối đối với oxi là 0,8125. Khí X là
A. C2H2.
B. C2H4.
C. C2H6.
D. CH4.
Câu 23: Phân tử nào sau đây có cấu tạo là mạch vòng sáu cạnh đều, có ba liên kết đơn xen kẽ ba liên kết đôi?
A. Axetilen.
B. Propan.
C. Benzen.
D. Xiclohexan.
Câu 24: Cho 7,8 gam benzen phản ứng với brom dư (có bột sắt xúc tác) hiệu suất phản ứng là 80%. Khối lượng brombenzen thu được là
A. 12,56 gam.
B. 15,70 gam.
C. 19,62 gam.
D. 23,80 gam.
Câu 25: Thành phần chính của khí đồng hành là
A. C2H2.
B. CH4.
C. C2H4.
D. H2.
Câu 26: Trên mũi khoan để khai thác dầu mỏ người ta có gắn
A. thép tốt.
B. đá thạch anh.
C. kim cương.
D. đá hoa cương.
Câu 27: Trong các loại than dưới đây, loại than già nhất có hàm lượng cacbon trên 90% là
A. than gầy.
B. than mỡ.
C. than non.
D. than bùn.
Câu 28: Chất làm mất màu dung dịch brom là
A. CH4.
B. CH2 = CH – CH3.
C. CH3 – CH3.
D. CH3 – CH2 – CH3.
Câu 29: Các trái cây, trong quá trình chín sẽ thoát ra một lượng nhỏ chất khí là
A. metan.
B. etan.
C. etilen.
D. axetilen.
Câu 30: Khí CH4 và C2H4 có tính chất hóa học giống nhau là
A. tham gia phản ứng cộng với dung dịch brom.
B. tham gia phản ứng cộng với khí hiđro.
C. tham gia phản ứng trùng hợp.
D. tham gia phản ứng cháy với khí oxi sinh ra khí cacbonic và nước.
Đáp án chi tiết:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
D |
B |
D |
C |
B |
D |
B |
B |
D |
C |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
D |
A |
B |
B |
D |
A |
D |
A |
B |
C |
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
30 |
|
A |
A |
C |
A |
B |
C |
A |
B |
C |
D |
Câu 2:
Hợp chất hữu cơ là hợp chất của cacbon trừ CO; CO2; muối cacbonat; axit cacbonic → chọn B.
Câu 5.
Loại A do phân tử khối của CH4 là 16 đvC.
Loại C do phân tử khối của C3H8 là 44 đvC.
Loại D do phân tử khối của C2H4 là 28 đvC.
Câu 11:
C2H2 + 2Br2 → C2H2Br4
0,1 → 0,2 mol
Khối lượng brom phản ứng: m = 0,2.160 = 32 gam.
Câu 12:
Sử dụng dung dịch brom: C2H4 làm mất màu dung dịch brom còn CH4 thì không.
Câu 15:
Các hợp chất hữu cơ: CH4; C2H4; C2H5ONa
Các hợp chất vô cơ: CO2; Na2CO3.
Câu 19.
C2H4 + Br2 → C2H4Br2
0,5 → 0,5 mol
Khối lượng dung dịch brom 5% tham gia phản ứng là:
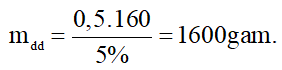
Câu 21.
C2H2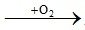 2CO2 + H2O
2CO2 + H2O
2 1 mol
Câu 22:
MX = 0,8125.32 = 26.
Vậy khí X là C2H2.
Câu 24:
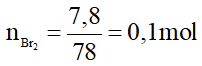
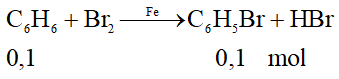
Do hiệu suất của phản ứng là 80% nên:
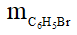 = 0,1.157.80% = 12,56 gam.
= 0,1.157.80% = 12,56 gam.
Câu 28:
CH2 = CH – CH3 có liên kết đôi, nên làm mất màu dung dịch brom.
Để xem trọn bộ Đề thi Hóa học 9 có đáp án, Thầy/ cô vui lòng Tải xuống!
Xem thêm các bộ đề thi lớp 9 chọn lọc, hay khác:
Đề thi Giữa Học kì 2 Sinh học lớp 9 năm 2022 - 2023 có đáp án
Đề thi Giữa học kì 2 Ngữ văn lớp 9 năm 2022 - 2023 có đáp án
Đề thi Giữa học kì 2 Địa Lí lớp 9 năm 2022 - 2023 có đáp án
Đề thi Giữa Học kì 2 Vật lí lớp 9 năm 2022 - 2023 có đáp án
Đề thi giữa học kì 2 Lịch sử lớp 9 năm 2022 - 2023 có đáp án
Đề thi Giữa Học kì 2 Toán lớp 9 năm 2022 - 2023 có đáp án
Đề thi Giữa Học kì 2 Tiếng Anh lớp 9 năm 2022 - 2023 có đáp án
Xem thêm các chương trình khác:
- Góp ý sgk lớp 9 tất cả các môn năm 2024 - 2025 (3 bộ sách)
- Đề thi vào 10 môn Toán | Tuyển tập đề thi thử, đề chính thức vào lớp 10 môn Toán mới nhất
- Đề thi vào 10 môn Địa lí
- Đề thi vào 10 môn Văn | Tuyển tập đề thi thử, đề chính thức vào lớp 10 môn Ngữ Văn mới nhất
- Đề thi vào 10 môn Tiếng Anh | Tuyển tập đề thi thử, đề chính thức vào lớp 10 môn Tiếng Anh mới nhất
