Lý thuyết Hóa học 10 Bài 3 (Cánh diều): Nguyên tố hóa học
Tóm tắt lý thuyết Hóa học 10 Bài 3: Nguyên tố hóa học ngắn gọn, chi tiết sách Cánh diều sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Hóa học 10.
Lý thuyết Hóa học 10 Bài 3: Nguyên tố hóa học
A. Lý thuyết Nguyên tố hóa học
I. Nguyên tố hóa học
1. Khái niệm nguyên tố hóa học
- Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
Ví dụ: Ba loại nguyên tử trong hình dưới đây đều có một proton (hạt màu xanh) trong hạt nhân nên thuộc cùng một nguyên tố hóa học, nguyên tố hydrogen (H).
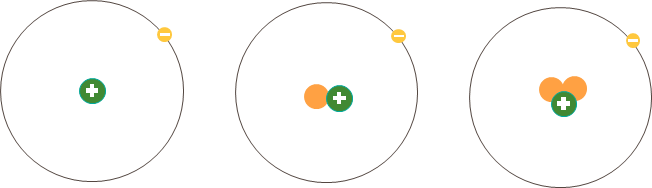
Hình 3.1. Minh họa cấu tạo một số loại nguyên tử của nguyên tố hydrogen
2. Số hiệu nguyên tử, số khối, kí hiệu nguyên tử
- Số proton trong một hạt nhân nguyên tử được gọi là số hiệu nguyên tử, kí hiệu là Z.
Ví dụ: Hạt nhân nguyên tử lithium (Li) có 3 proton, vậy số hiệu nguyên tử của Li là 3 (ZLi = 3).
- Tổng số proton (Z) và neutron (N) trong một hạt nhân nguyên tử được gọi là số khối, kí hiệu là A.
A = Z + N
Như vậy, số khối chính bằng tổng số hạt có trong hạt nhân nguyên tử. Giá trị này xấp xỉ bằng giá trị khối lượng nguyên tử (tính theo đơn vị amu).
Ví dụ: Một loại nguyên tử sodium (Na) có 11 hạt proton, 11 electron và 12 hạt neutron. Số khối của nguyên tử Na = Z + N = P + N = 11 + 12 = 23 (amu)
- Kí hiệu nguyên tử cho biết kí hiệu hóa học của nguyên tố (X), số hiệu nguyên tử (Z) và số khối (A).

Hình 3.2. Kí hiệu nguyên tử của helium
Lưu ý: Đôi khi, người ta viết tắt kí hiệu nguyên tử.
Ví dụ: Sử dụng 4He thay cho , bởi kí hiệu He đã cho biết đây là nguyên tử nguyên tố helium, hạt nhân có 2 proton.
II. Đồng vị, nguyên tử khối trung bình
1. Đồng vị
- Các nguyên tử của cùng một nguyên tố hóa học có số neutron khác nhau là đồng vị của nhau.
Do đó, đồng vị của cùng một nguyên tố hóa học (có cùng số proton) khác nhau về số khối do đó số neutron khác nhau.
Ví dụ: Helium có hai đồng vị bền là và .
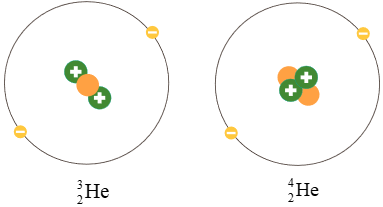
Hình 3.3. Minh họa cấu tạo nguyên tử hai đồng vị của nguyên tố helium
- Tất cả các nguyên tố hóa học đều có nhiều đồng vị.
Ví dụ: Hydrogen có ba đồng vị là (kí hiệu là H), (kí hiệu là D), (kí hiệu là T), oxygen có 17 đồng vị bắt đầu từ và kết thúc là , ...
2. Nguyên tử khối trung bình
a) Nguyên tử khối
- Nguyên tử khối là khối lượng tương đối của một nguyên tử, cho biết khối lượng của một nguyên tử nặng gấp bao nhiêu lần 1 amu.
Ví dụ: Nguyên tử khối của 16O là 16 do khối lượng của một nguyên tử 16O là 16 amu.
b) Nguyên tử khối trung bình
- Mỗi nguyên tố hóa học đều có nhiều đồng vị.
- Trong tự nhiên, một nguyên tố hóa học dù ở dạng đơn chất hay hợp chất thì tỉ lệ giữa các đồng vị của nguyên tố này là không đổi.
- Nguyên tử khối của nguyên tố hóa học có nhiều đồng vị là nguyên tử khối trung bình của các đồng vị (kí hiệu là ![]() ), có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng (xác định từ phổ khối lượng).
), có tính đến tỉ lệ số nguyên tử các đồng vị tương ứng (xác định từ phổ khối lượng).
- Công thức tính nguyên tử khối trung bình như sau:
=
Trong đó:
+ X, Y, Z, ... lần lượt là số khối của các đồng vị.
+ x, y, z, ... là phần trăm số nguyên tử các đồng vị tương ứng.
Ví dụ: Trong tự nhiên, đồng có hai đồng vị bền là 63Cu và 65Cu chiếm tương ứng khoảng 73% và 27% về số nguyên tử. Nguyên tử khối trung bình của đồng là:
= = 63,64
Lưu ý: Nguyên tử khối của một nguyên tố hóa học ghi trong bảng tuần hoàn là nguyên tử khối trung bình của các đồng vị trong tự nhiên.
B. Trắc nghiệm Nguyên tố hóa học
Câu 1. Nguyên tố hóa học là
A. tập hợp các nguyên tử có cùng số hạt neutron;
B. tập hợp các nguyên tử có cùng số hạt proton;
C. tập hợp các nguyên tử có cùng số hạt neutron và proton;
D. tập hợp các nguyên tử có cùng số số lớp electron.
Đáp án: B
Giải thích: Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
Câu 2. Cho các nguyên tử X, Y, Z biết:
Nguyên tử X có 6 electron; 6 proton và 6 neutron.
Nguyên tử Y có 6 electron; 6 proton và 7 neutron.
Nguyên tử Z có 7 electron; 7 proton và 7 neutron.
Các nguyên tử cùng thuộc một nguyên tố hóa học là:
A. X và Y;
B. Y và Z;
C. X và Z;
D. X, Y và Z.
Đáp án: A
Giải thích:
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
Mà nguyên tử X và Y đều có cùng số proton là 6. Nên X và Y cùng thuộc một nguyên tố hóa học.
Câu 3. Số hiệu nguyên tử là
A. số neutron trong một hạt nhân nguyên tử, kí hiệu là Z;
B. số proton trong một hạt nhân nguyên tử, kí hiệu là Z;
C. tổng số proton và neutron trong một hạt nhân nguyên tử, kí hiệu là Z;
D. tổng số proton và electron trong một nguyên tử, kí hiệu là Z.
Đáp án: B
Giải thích: Số hiệu nguyên tử là số proton trong một hạt nhân nguyên tử, kí hiệu là Z.
Câu 4. Nguyên tử potassium (K) có 19 electron; 19 proton và 20 neutron. Số hiệu nguyên tử của K là
A. ZK = 20;
B. ZK = 19;
C. ZK = 39;
D. ZK = 38.
Đáp án: B
Giải thích:
Số hiệu nguyên tử là số proton trong một hạt nhân nguyên tử, kí hiệu là Z.
Nên ZK = 19.
Câu 5. Số khối là
A. tổng số proton (Z) và neutron (N) trong một hạt nhân nguyên tử, kí hiệu là A;
B. tổng số proton (Z) và electron (E) trong một hạt nhân nguyên tử, kí hiệu là A;
C. số proton trong một hạt nhân nguyên tử, kí hiệu là Z;
D. số neutron trong một hạt nhân nguyên tử, kí hiệu là N.
Đáp án: A
Giải thích:
Số khối là tổng số proton (Z) và electron (E) trong một hạt nhân nguyên tử, kí hiệu là A.
A = Z + N
Câu 6. Kí hiệu nguyên tử cho biết
A. kí hiệu hóa học của nguyên tố (X);
B. số hiệu nguyên tử (Z);
C. số khối (A);
D. Cả A, B và C đều đúng.
Đáp án: D
Giải thích: Kí hiệu nguyên tử cho biết kí hiệu hóa học của nguyên tố (X); số hiệu nguyên tử (Z); số khối (A).
Câu 7. Cho kí hiệu nguyên tử . Khẳng định nào sau đây sai?
A. Kí hiệu hóa học của nguyên tố là O;
B. Số hiệu nguyên tử là 16;
C. Số proton trong một hạt nhân nguyên tử là 8;
D. Số neutron trong một hạt nhân nguyên tử là 8.
Đáp án: B
Giải thích:
Kí hiệu nguyên tử cho biết:
- Kí hiệu hóa học của nguyên tố là O;
- Số hiệu nguyên tử Z = 8 ⇒ số proton là 8.
- Số khối A = 16 mà A = Z + N ⇒ N = A – Z = 16 – 8 = 8 ⇒ số neutron là 8.
Vậy khẳng định: Số hiệu nguyên tử là 16 là khẳng định sai.
Câu 8. Một nguyên tử sodium (Na) có 11 e; 11p và 12n. Kí hiệu của nguyên tử này là
A. ;
B.
C. ;
D. .
Đáp án: C
Giải thích:
Một nguyên tử sodium (Na) có:
- Số hiệu nguyên tử Z = số p = 11
- Số khối A = Z + N = số p + số n = 11 + 12 = 23
Kí hiệu nguyên tử là .
Câu 9. Cho nguyên tử iron (Fe) có kí hiệu nguyên tử là . Số hạt electron, proton, neutron trong một nguyên tử này lần lượt là
A. 26; 26; 56
B. 26; 26; 30
C. 30; 30; 26
D. 30; 26; 26
Đáp án: B
Giải thích:
Kí hiệu nguyên tử là
Ta có: số e = số p = Z = 26
Số n = N = A – Z = 56 – 26 = 30
Vậy số e, p, n lần lượt là: 26; 26; 30
Câu 10. Phát biểu nào sau đây là đúng?
A. Những nguyên tử có cùng số electron thuộc cùng một nguyên tố hóa học;
B. Hai nguyên tử A và B đều có số khối là 14. Vậy hai nguyên tử này thuộc cùng một nguyên tố hóa học;
C. Những nguyên tử có cùng số neutron thuộc cùng một nguyên tố hóa học;
D. Cả A, B và C đều sai.
Đáp án: A
Giải thích:
Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton.
Mà trong nguyên tử số p = số e.
Nên những nguyên tử có cùng số electron thuộc cùng một nguyên tố hóa học là phát biểu đúng.
Xem thêm tóm tắt lý thuyết Hóa học 10 sách Cánh diều hay, chi tiết khác:
Lý thuyết Bài 4: Mô hình nguyên tử và orbital nguyên tử
Lý thuyết Bài 5: Lớp, phân lớp và cấu hình electron
Lý thuyết Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Lý thuyết Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Xem thêm các chương trình khác:
- Soạn văn lớp 10 (hay nhất) – Cánh Diều
- Tác giả tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Tóm tắt tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Bố cục tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Nội dung chính tác phẩm Ngữ văn lớp 10 – Cánh Diều
- Soạn văn lớp 10 (ngắn nhất) – Cánh Diều
- Giải sbt Ngữ văn lớp 10 – Cánh Diều
- Văn mẫu lớp 10 – Cánh Diều
- Giải Chuyên đề học tập Ngữ văn 10 – Cánh diều
- Giải sgk Toán 10 – Cánh Diều
- Giải Chuyên đề Toán 10 – Cánh Diều
- Lý thuyết Toán 10 – Cánh Diều
- Giải sbt Toán 10 – Cánh Diều
- Chuyên đề dạy thêm Toán 10 Cánh diều (2024 có đáp án)
- Giải sgk Tiếng Anh 10 – Explore new worlds
- Giải sgk Tiếng Anh 10 – ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 10 ilearn Smart World đầy đủ nhất
- Ngữ pháp Tiếng Anh 10 i-learn Smart World
- Giải sbt Tiếng Anh 10 - iLearn Smart World
- Giải sgk Vật lí 10 – Cánh Diều
- Giải sbt Vật lí 10 – Cánh Diều
- Lý thuyết Vật lí 10 – Cánh Diều
- Giải Chuyên đề Vật lí 10 – Cánh Diều
- Giải sgk Sinh học 10 – Cánh Diều
- Giải sbt Sinh học 10 – Cánh Diều
- Lý thuyết Sinh học 10 – Cánh Diều
- Giải Chuyên đề Sinh học 10 – Cánh diều
- Giải sgk Lịch sử 10 – Cánh Diều
- Giải sbt Lịch sử 10 – Cánh Diều
- Giải Chuyên đề Lịch sử 10 – Cánh Diều
- Lý thuyết Lịch sử 10 – Cánh diều
- Giải sgk Địa lí 10 – Cánh Diều
- Lý thuyết Địa Lí 10 – Cánh Diều
- Giải sbt Địa lí 10 – Cánh Diều
- Giải Chuyên đề Địa lí 10 – Cánh Diều
- Lý thuyết Công nghệ 10 – Cánh Diều
- Giải sgk Công nghệ 10 – Cánh Diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải sbt Giáo dục Kinh tế và Pháp luật 10 – Cánh Diều
- Giải Chuyên đề Kinh tế pháp luật 10 – Cánh diều
- Lý thuyết KTPL 10 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 10 – Cánh Diều
- Giải sgk Giáo dục quốc phòng - an ninh 10 – Cánh diều
- Giải sbt Giáo dục quốc phòng - an ninh 10 – Cánh Diều
- Giải sgk Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sbt Hoạt động trải nghiệm 10 – Cánh Diều
- Giải sgk Tin học 10 – Cánh Diều
- Giải sbt Tin học 10 – Cánh Diều
- Giải Chuyên đề Tin học 10 – Cánh diều
- Lý thuyết Tin học 10 - Cánh diều
- Giải sgk Giáo dục thể chất 10 – Cánh Diều
