Trắc nghiệm Sắt (có đáp án) Hóa học lớp 12
Trắc nghiệm Bài 31: Sắt
-
530 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Tính chất vật lý của sắt:
- Có màu trắng hơi xám.
- Dẻo, dễ rèn, nóng chảy ở nhiệt độ 1540oC
- Là kim loại nặng, có khối lượng riêng d = 7,9 g/cm3
- Dẫn điện, dẫn nhiệt tốt.
- Là kim loại có từ tính, bị nam châm hút.
→ Khẳng định sắt có màu vàng nâu là sai.
Câu 2:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án A
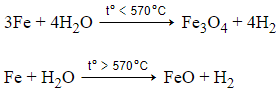
Câu 3:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Trong hợp chất FeO số oxi hóa của Fe là +2 → Fe có thể tăng số oxi hóa lên +3 hoặc giảm số oxi hóa về 0. Nên FeO vừa có tính khử, vừa có tính oxi hóa.
Câu 4:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Đốt cháy sắt trong không khí tạo thành Fe3O4
Câu 5:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Fe thụ động trong dung dịch HNO3 đặc, nguội và H2SO4 đặc, nguội.
Câu 6:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
A. 2Fe + 3Cl2 → 2FeCl3
B. Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
C. Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư→ Fe(NO3)3 + Ag
D. Fe + 2HCl → FeCl2 + H2
Câu 7:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Fe + S FeS
nFeS = nS = nFe phản ứng = 0,2 mol
→ nFe dư = 0,3 – 0,2 = 0,1 mol
→ Chất rắn A gồm Fe dư: 0,1 mol và FeS: 0,2 mol
→ A phản ứng với HCl thu được khí gồm H2: 0,1 mol và H2S: 0,2 mol
Mkhí =
→ Tỉ khối của A với không khí là 0,8045.
Câu 8:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Áp dụng định luật bảo toàn khối lượng
mFe + mO = m oxit
→ 2,24 + mO = 3,04
→ mO = 0,8 gam
→ nO = 0,05 mol
Áp dụng bảo toàn nguyên tố
Oxit + HCl muối clorua + H2O
nHCl = nH (axit) = 2.nO
= 2.0,05 = 0,1 mol
→ Vdd HCl 2M = = 0,05 lít = 50 ml
Câu 9:
14/07/2024 Xem đáp án
Xem đáp án
Đáp án C
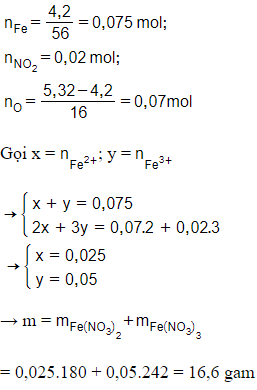
Câu 10:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
= 0,8.0,2 = 0,16 mol
= 0,8.0,25 = 0,2 mol
Do sau phản ứng còn dư hỗn hợp bột kim loại
→ Fe còn dư, Cu2+ hết, thu muối Fe2+
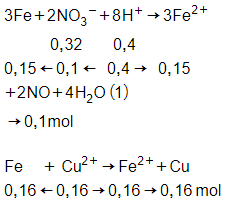
VNO = 0,1.22,4 = 2,24 lít
m – (0,15 + 0,16).56 + 0,16.64 = 0,6m
→ m = 17,8 gam
Câu 11:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án D
+) Fe đơn chất có số oxi hóa bằng 0 → có khả nhường 2e hoặc 3e → chỉ có tính khử → X là Fe
+) Fe2+ có khả năng nhường 1e để thành Fe3+ → có tính khử
Fe2+ có khả năng nhận 2e để thành Fe đơn chất → có tính oxi hóa
→ Z là Fe2+
+) Fe3+ chỉ có khả năng nhận 1e để trở nhà Fe2+ hoặc nhận 3e để thành Fe đơn chất → Fe3+ chỉ có tính oxi hóa → Y là Fe3+
Câu 12:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
B. Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Câu 13:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Kim loại X là Fe
Phần 1: 2Fe (X) + 3Cl2 2FeCl3 (Y)
Phần 2: Fe (X) + 2HCl → FeCl2 (Z) + H2
Fe (X) + 2FeCl3 (Y) → 3FeCl2 (Z)
Câu 14:
23/07/2024Hoà tan hết cùng một lượng Fe trong dung dịch H2SO4 loãng (dư) và dung dịch H2SO4 đặc, nóng (dư) thì các thế tích khí sinh ra lần lượt là V1 và V2 (đo ở cùng điều kiện). Liên hệ giữa V1 và V2 là
 Xem đáp án
Xem đáp án
Đáp án C
Gọi số mol Fe là a mol
Áp dụng định luật bảo toàn số mol electron
Cho Fe vào H2SO4 loãng:
2 = 2nFe
→ = nFe = a mol
Cho Fe vào H2SO4 đặc, nóng:
3nFe = 2
→ = 1,5nFe = 1,5a mol
Ở cùng điều kiện, tỉ lệ về thể tích cũng là tỉ lệ về số mol
→ V2 = 1,5V1.
Câu 15:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án A
nFe = 0,04 mol;
nHCl = 0,3.0,4 = 0,12 mol
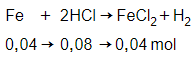
Dung dịch X gồm:
HCl dư = 0,12 – 0,08 = 0,04 mol và FeCl2: 0,04 mol
Cho AgNO3 dư vào X có phản ứng:
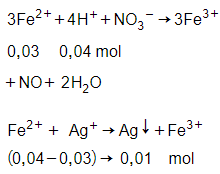
→ m = 0,01.108 + 0,12.143,5
= 18,3 gam.
Câu 16:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
N2: Khí không màu, nhẹ hơn không khí
N2O: Khí không màu, nặng hơn không khí.
NO: Khí không màu, hóa nâu ngoài không khí.
NO2: Khí màu nâu đỏ
Câu 17:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
Khối lượng kim loại phản ứng là:
mKL = = 0,84 gam
= 0,336 : 22,4 = 0,015 mol
2M + 2nHCl → 2MCln + nH2
Số mol của M là:
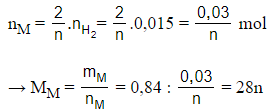
Với n = 1 → MM = 28 loại
n = 2 → MM = 56 (Fe) Thỏa mãn
n = 3 → MM = 84 loại.
Vậy kim loại cần tìm là Fe
Câu 18:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Áp dụng định luật bảo toàn electron:
2.nFe = 2.
→ = nFe = 0,2 mol
→ V = 0,2.22,4 = 4,48 lít
Câu 19:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án B
nFe = 6 : 56 = 0,107 mol
= 0,1.1 = 0,1 mol
Fe + CuSO4 → FeSO4 + Cu
→ Fe còn dư
→ nCu = nFe phản ứng
= = 0,1 mol
Khối lượng hỗn hợp kim loại thu được là:
m = 6 – 0,1.56 + 0,1.64 = 6,8 gam
Câu 20:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Bảo toàn số mol electron
→ 3nFe = 3nNO
→ nNO = nFe = 0,1
→ V = 2,24 lít
Câu 21:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án B
nFe = 0,15 mol; = 0,39 mol
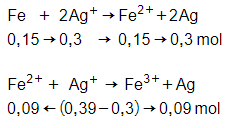
→ m = mAg = 0,39.108 = 42,12 gam
Câu 22:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án D
= 0,15 mol
Chỉ có Fe phản ứng với dung dịch HCl
Bảo toàn electron ta có:
2.nFe = 2.
→ = nFe = 0,15 mol
→ mFe = 0,15.56 = 8,4 gam
→ mCu = 10 – 8,4 = 1,6 gam
Câu 23:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
= 6,5 : 162,5 = 0,04 mol
Bảo toàn nguyên tố Fe:
nFe = = 0,04 mol
→ mFe = 0,04.56 = 2,24 gam
Câu 24:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Đặt công thức phân tử của oxit sắt là FexOy
nFe = 16,8 : 56 = 0,3 mol
= 4,48 : 22,4 = 0,2 mol
→ nO = 0,2.2 = 0,4 mol
→ x : y = nFe : nO = 0,3 : 0,4 = 3 : 4
→ Công thức phân tử của oxit sắt là: Fe3O4
Câu 25:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Cấu hình electron của Fe là [Ar]3d64s2
Câu 26:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án D
Cấu hình electron của Fe là [Ar]3d64s2
Fe nhường 2e lớp ngoài cùng để trở thành Fe2+
→ Cấu hình electron của Fe2+ là [Ar]3d6
Câu 27:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án B
mFe + mCu = 3,04
→ 56.nFe + 64.nCu = 3,04 (1)
Bảo toàn electron:
3.nFe + 2.nCu = 3.nNO
→ 3.nFe + 2.nCu = 3.= 0,12 mol (2)
Từ (1) và (2) → nFe = 0,02 mol;
nCu = 0,03 mol
→ %mFe = = 36,8%
Câu 28:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án A
Phương trình phản ứng xảy ra:
(1) Fe + 2FeCl3 → 3FeCl2
(2) Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
(3) Fe + CuSO4 → FeSO4 + Cu
(4) Fe + 2HCl → FeCl2 + H2
(5) Fe không phản ứng với HNO3 đặc nguội.
(6) 2Fe + 6H2SO4 đặc, nóng, dư → Fe2(SO4)3 + 3SO2 + 6H2O
(7) Fe + H2SO4 loãng → FeSO4 + H2
(8) Fe + 4HNO3 loãng → Fe(NO3)3 + NO + 2H2O
→ Có 3 trường hợp tạo muối sắt(III)
Câu 29:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án D
A. Đúng
Fe + 2HCl → FeCl2 + H2
B. Đúng
Fe + 2FeCl3 → 3FeCl2
C. Đúng. Fe không phản ứng với H2SO4 đặc nguội, HNO3 đặc nguội.
D. Sai, ion Fe2+ ở mức oxi hóa trung gian nên có thể tăng hoặc giảm số oxi hóa → thể hiện cả tính khử, cả tính oxi hóa.
Câu 30:
20/07/2024 Xem đáp án
Xem đáp án
Đáp án C
Quy đổi hỗn hợp X về hỗn hợp gồm (Fe, O)
nFe = 16,8 : 56 = 0,3 mol
Bảo toàn electron cho phản ứng hòa tan X và dung dịch H2SO4
→ 3.nFe = 2.nO + 2.
→ 3.0,3 = 2.nO + 2.0,25
→ nO = 0,2 mol
→ mX = 56.0,3 + 16.0,2 = 20 gam
Có thể bạn quan tâm
- Trắc nghiệm Sắt (có đáp án) Hóa học lớp 12 (529 lượt thi)
- 16 câu trắc nghiệm Sắt (Fe) cực hay có đáp án (197 lượt thi)
Các bài thi hot trong chương
- 150 câu trắc nghiệm Crom - Sắt - Đồng nâng cao (1154 lượt thi)
- 150 câu trắc nghiệm Crom - Sắt - Đồng cơ bản (925 lượt thi)
- Trắc nghiệm Hợp kim của sắt (có đáp án) (550 lượt thi)
- Trắc nghiệm Hợp chất của sắt (có đáp án) (457 lượt thi)
- Trắc nghiệm Crom và hợp chất của crom (có đáp án) (413 lượt thi)
- Trắc nghiệm Sơ lược về niken, kẽm, chì, thiếc (có đáp án) (382 lượt thi)
- Trắc nghiệm Đồng và hợp chất của đồng (có đáp án) (345 lượt thi)
- Trắc nghiệm Luyện tập: Tính chất của sắt và hợp chất của sắt (có đáp án) (332 lượt thi)
- 15 Câu trắc nghiệm hợp chất của sắt có đáp án (308 lượt thi)
- 7 Câu trắc nghiệm luyện tập tính chất hóa học của crom và hợp chất của crom có đáp án (261 lượt thi)
