Đề thi Học kì 2 Hóa học 10 cực hay có đáp án
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 6)
-
3353 lượt thi
-
30 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
23/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Số oxi hoá có thể có của lưu huỳnh trong hợp chất là -2, +4, +6.
Câu 2:
03/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cấu tạo một phân tử halogen gồm 2 nguyên tử
Câu 3:
11/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Trong hợp chất, nguyên tố flo chỉ có số oxi hoá là -1
Câu 4:
10/07/2024(a) Được dùng để sát trùng, làm sạch nước sinh hoạt.
(b) Được dùng để chữa sâu răng.
(c) Được dùng để tẩy trắng tinh bột, dầu ăn.
(d) Được dùng để bảo quản trái cây chín.
Số ứng dụng trên của ozon là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Cả 4 ứng dụng trên đều là ứng dụng của ozon.
Câu 5:
04/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Trong công nghiệp, người ta điều chế nước Giaven bằng cách điện phân dung dịch NaCl không có màng ngăn.
Phản ứng hóa học minh họa:
2NaCl + 2H2O  2NaOH + Cl2+ H2
2NaOH + Cl2+ H2
Do không có màng ngăn:
Cl2+ 2NaOH → NaCl + NaClO + H2O (nước Gia – ven)
Câu 6:
03/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dung dịch HF không được đựng bằng lọ thuỷ tinh vì HF có khả năng ăn mòn thuỷ tinh.
4HF + SiO2→ SiF4+ 2H2O
Câu 7:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Ở điều kiện thường, lưu huỳnh tồn tại ở trạng thái rắn.
Câu 8:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dùng thuốc thử là dung dịch AgNO3
+ Không hiện tượng: NaF
NaF + AgNO3→ Không phản ứng
+ Xuất hiện kết tủa trắng: NaCl
NaCl + AgNO3→ NaNO3+ AgCl↓
+ Xuất hiện kết tủa vàng: NaBr
NaBr + AgNO3→ NaNO3+ AgBr↓
+ Xuất hiện kết tủa vàng đậm: NaI
NaI + AgNO3→ NaNO3+ AgI↓
Câu 9:
14/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Sự dịch chuyển cân bằng hoá học là sự di chuyển từ trạng thái cân bằng hoá học nàysang trạng thái cân bằng hoá học khác do tác động của các yếu tố từ bên ngoài tác động lên cân bằng.
Câu 10:
18/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Để vận chuyển axit sunfuric đặc, nguội có thể đựng trong bình chứa làm bằng Fe
Câu 11:
09/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
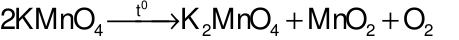
Câu 12:
20/07/2024 (mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là
(mỗi mũi tên ứng với một phản ứng). Hai chất X, Y lần lượt là Xem đáp án
Xem đáp án
Đáp án đúng là: B
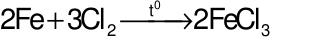
FeCl
3+ 3NaOH → Fe(OH)3↓ + 3NaClCâu 13:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
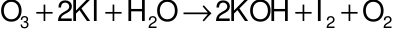
I
2sinh ra tác dụng với hồ tinh bột thấy xuất hiện màu xanh đậm.Câu 14:
15/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khi đốt cháy axetilen để hàn, cắt kim loại, nhiệt lượng giải phóng ra lớn nhất khi axetilen cháy trong khí oxi nguyên chất
Câu 15:
03/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Dung dịch H2SO4đậm đặc có thể dùng để làm khô khí Cl2ẩm. Do H2SO4đặc hút ẩm và Cl2không tác dụng với H2SO4đặc.
Câu 16:
04/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Tính chất hoá học của dung dịch axit sunfuric loãng là tính axit mạnh.
Câu 17:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 18:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Trong phản ứng: 3H2S + 2KMnO4→ 2MnO2 +2KOH + 3S↓ +2H2O
Số oxi hóa của S tăng từ -2 lên 0, do đó H2S đóng vai trò là chất khử.
Câu 19:
03/07/2024(a) N2(k) + 3H2(k) ⇄ 2NH3(k)
(b) H2(k) + I2(k) ⇄ 2HI (k)
(c) 2SO2(k) + O2(k) ⇄ 2SO3(k)
(d) 2NO2(k) ⇄ N2O4(k)
Khi thay đổi áp suất những số cân bằng hóa học bị chuyển dịch là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khi thay đổi áp suất, những cân bằng hoá học bị dịch chuyển là: (a), (c), (d). Đây là các cân bằng có tổng số mol khí ở hai vế là khác nhau.
Câu 20:
03/07/2024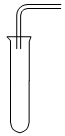
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Vì ống nghiệm ngửa nên khí thu được nặng hơn không khí
→ chọn Cl2
Câu 21:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: B
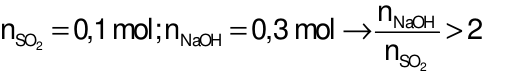
→
phản ứng sinh ra muối Na2SO3và NaOH dưCâu 22:
16/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
CaCO3tác dụng với H2SO4đặc hay loãng đều thu được sản phẩm giống nhau.
CaCO3+ H2SO4→ CaSO4+ CO2↑ + H2O
Câu 23:
02/11/2024Việc sản xuất amoniac trong công nghiệp dựa trên phản ứng :
N2 (k) + 3H2 (k) ⇄ 2NH3 (k) 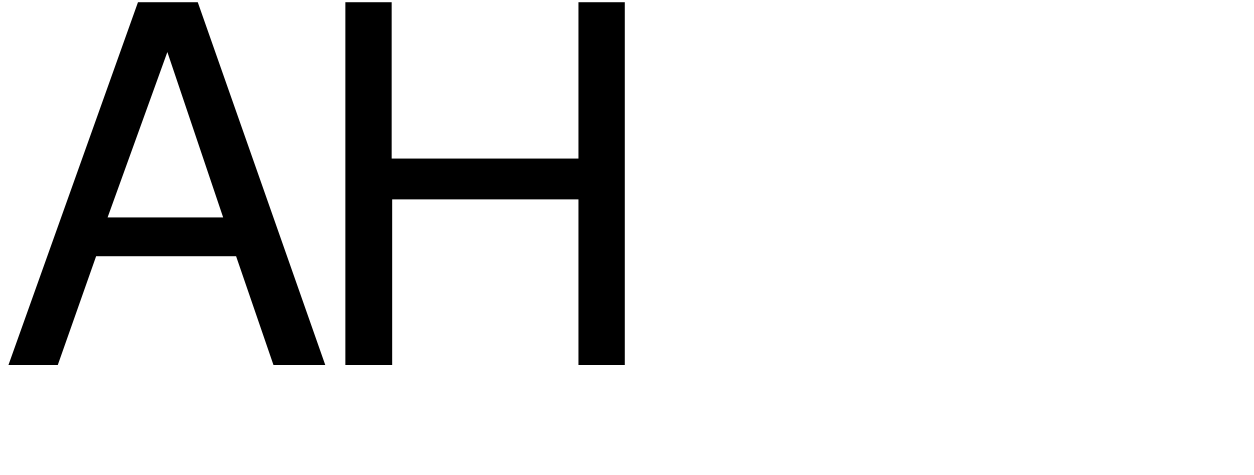 < 0.
< 0.
Muốn sản xuất amoniac đạt hiệu quả cao, người ta phải thay đổi các yếu tố nào sau đây ?
</>
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
- Muốn sản xuất amoniac đạt hiệu quả cao, người ta phải thay đổi các yếu tố Tăng áp suất, giảm nhiệt độ và lấy NH3ra khỏi phản ứng.
Khi tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm áp suất (chiều thuận)
Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều làm tăng nhiệt độ (chiều thuận)
Lấy NH3ra khỏi phản ứng, cân bằng chuyền dịch theo chiều làm tăng NH3(chiều thuận).
→ D đúng.A,B,C sai.
* Phản ứng một chiều
- Phản ứng một chiều là phản ứng chỉ xảy ra theo một chiều từ trái sang phải (tức các sản phẩm phản ứng không tác dụng được với nhau để tạo ra các chất tham gia phản ứng).
- Ví dụ phản ứng một chiều:
2KClO3 2KCl + 3O2 ↑
Cũng điều kiện đó O2 tạo ra không tác dụng được với KCl để tạo thành KClO3.
2. Phản ứng thuận nghịch
- Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều trái ngược nhau (tức là các chất tham gia phản ứng tác dụng với nhau để tạo thành sản phẩm đồng thời các sản phẩm phản ứng được với nhau để tạo ra các chất tham gia phản ứng).
Ví dụ phản ứng thuận nghịch:
3H2 + N2 2NH3
NH3 được tạo thành đồng thời lại bị phân hủy sinh ra H2 và N2 là các chất tham gia phản ứng.
3. Cân bằng hóa học
- Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ của phản ứng nghịch.
- Cân bằng hóa học là cân bằng động, vì ở trạng thái cân bằng, phản ứng không dừng lại mà phản ứng thuận và phản ứng nghịch vẫn diễn ra, nhưng với tốc độ bằng nhau.
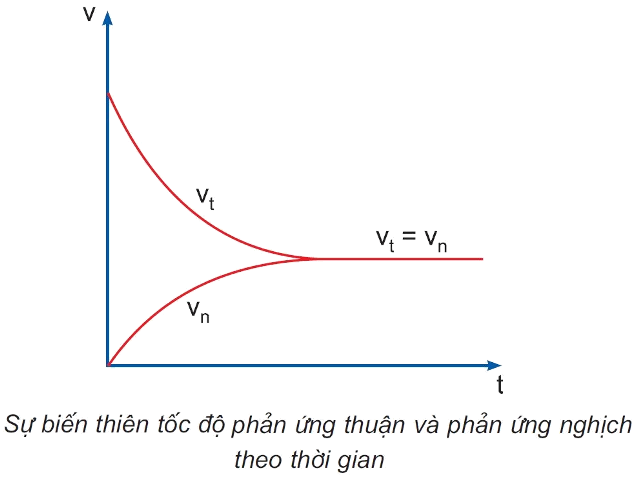
II. Sự chuyển dịch cân bằng hóa học
- Sự chuyển dịch cân bằng hóa học là sự chuyển từ trạng thái cân bằng này sang trạng thái cân bằng khác do tác động của các yếu tố từ bên ngoài lên cân bằng.
III. Các yếu tố ảnh hưởng đến cân bằng hóa học
1. Ảnh hưởng của nồng độ
- Khi tăng hoặc giảm nồng độ của một chất trong cân bằng thì cân bằng chuyển dịch theo chiểu làm giảm tác dụng của việc tăng hoặc giảm nồng độ của chất đó.
- Lưu ý: Đối với hệ cân bằng có chất rắn thì việc thêm hay bớt lượng chất rắn không ảnh hưởng đến cân bằng, nghĩa là cân bằng không chuyển dịch.
2. Ảnh hưởng của áp suất
- Khi tăng hoặc giảm áp suất chung của hệ cân bằng thì cân bằng chuyển dịch theo chiều làm giảm tác dụng của việc tăng hoặc giảm áp suất đó.
- Lưu ý: Khi hệ cân bằng có số mol khí ở 2 về bằng nhau hoặc trong hệ không có chất khí thì việc tăng, giảm áp suất chung của hệ không làm cho cân bằng chuyển dịch.
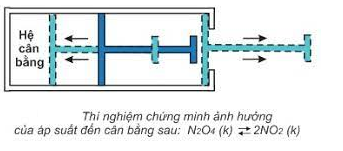
3. Ảnh hưởng của nhiệt độ
- Khi tăng nhiệt độ thì cân bằng chuyền dịch theo chiều phản ứng thu nhiệt, nghĩa là làm giảm tác dụng của việc tăng nhiệt độ.
- Còn khi giảm nhiệt độ thì cân bằng chuyển dịch theo chiều phản ứng tỏa nhiệt, nghĩa là làm giảm tác dụng của việc giảm nhiệt độ.
Kết luận: Nguyên lí chuyển dịch cân bằng (Nguyên lí Lơ Sa-tơ-li-ê): "Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động bên ngoài, như biến đổi nồng độ, áp suất, nhiệt độ sẽ chuyển dịch cân bằng theo chiều làm giảm tác động bên ngoài đó”.
4. Vai trò của chất xúc tác
- Chất xúc tác không ảnh hưởng đến cân bằng vì chất xúc tác làm tăng tốc độ phản ứng thuận và tốc độ phản ứng nghịch với số lần bằng nhau.
V. Ý nghĩa của tốc độ phản ứng và cân bằng hóa học trong sản xuất hóa học
Trong công nghiệp và sản xuất việc vận dụng các yếu tố làm tăng tốc độ phản ứng và chuyển dịch cân bằng giúp phản ứng thực hiện nhanh và đạt hiệu suất cao.
Xem thêm các bài viết liên quan,chi tiết khác:
Câu 24:
19/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Gọi số mol Al và Mg lần lượt là x và y mol
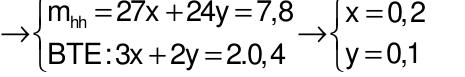
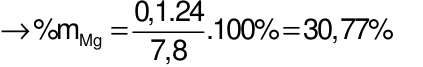
Câu 25:
22/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Loại B, C và D do: Các chất CuSO4, Cu, H2SO4không tác dụng với HCl
Câu 26:
13/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Bảo toàn nguyên tố S: 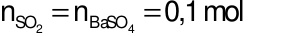
→ V = 2,24 lít
Câu 27:
21/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Gọi số mol khí Cl2và O2lần lượt là x và y mol
→ x + y = 0,25 (1)
Bảo toàn khối lượng: mR+ mkhí= mrắn
→ mkhí= 23 – 7,2 = 15,8
→ 71x + 32y = 15,8 (2)
Từ (1) và (2) 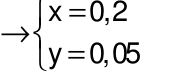
Bảo toàn e: 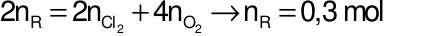
→ MR= 24 (Mg)
Câu 28:
17/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là:
Gọi số mol của Fe và FeO lần lượt là x và y mol
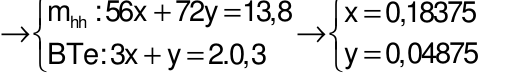
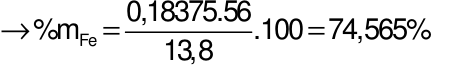
Câu 29:
13/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Quy đổi hỗn hợp X thành Fe (a mol), O (b mol) và Cu (c mol)
→ 56a + 16b + 64c = 2,44 (1)
Bảo toàn e: 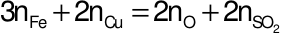
→ 3a + 2c = 2b + 0,045 (2)
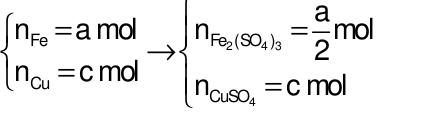
→ 200a + 160c = 6,6 (3)
Từ (1), (2), (3) → a = b = 0,025; c = 0,01 mol
→ %mCu= 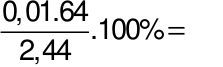 26,23%
26,23%
Câu 30:
04/07/2024 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn nguyên tố C: 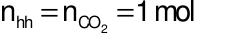
→ m = 1.100 =100 gam
Chú ý: Có phân tử khối của KHCO3và CaCO3 đều là 100 đvC.
----------- HẾT ----------
Bài thi liên quan
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 1)
-
30 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 2)
-
12 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 3)
-
20 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 3)
-
10 câu hỏi
-
30 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 4)
-
10 câu hỏi
-
30 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 5)
-
14 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 5)
-
12 câu hỏi
-
30 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 7)
-
30 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 8)
-
28 câu hỏi
-
40 phút
-
-
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 9)
-
27 câu hỏi
-
40 phút
-
Có thể bạn quan tâm
- Đề thi Học kì 2 Hóa 10 cực hay có đáp án (866 lượt thi)
- Đề thi giữa kì 2 Hóa 10 cực hay có đáp án (410 lượt thi)
- Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (3352 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 1) (623 lượt thi)
- Đề kiểm tra 15 phút - Trắc nghiệm + Tự luận (704 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 1) (908 lượt thi)
- Đề kiểm tra 15p Hóa 10 Học kì 2 (Bài số 2) (1302 lượt thi)
- Đề thi giữa kì 2 Hóa 10 (Bài số 2) (720 lượt thi)
- Đề thi Hóa 10 Học kì 2 (Bài kiểm tra học kì) (688 lượt thi)
Các bài thi hot trong chương
- Đề kiểm tra 15 phút Hóa học 10 Học kì 1 có đáp án (Bài số 1) (2644 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 1) (790 lượt thi)
- Đề thi giữa kì 1 Hóa học 10 có đáp án (Bài số 2) (755 lượt thi)
- Đề kiểm tra 15 phút Hóa 10 Học kì 1 có đáp án (Bài số 2 - Đề 1) (643 lượt thi)
- Đề thi Hóa 10 Học kì 1 (581 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 năm 2020 - 2021 có đáp án (535 lượt thi)
- Đề thi Hóa học 10 Giữa học kì 1 biên soạn (486 lượt thi)
- Đề thi Học kì 1 Hóa 10 có đáp án (344 lượt thi)
- Đề thi giữa kì 1 Hóa 10 cực hay có đáp án (Bài kiểm tra số 2) (315 lượt thi)
