Đề thi Hóa Học 12 giữa kì 2 có đáp án
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 6)
-
2825 lượt thi
-
30 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
22/07/2024Hấp thụ hết 3,584 lít khí CO2 (đktc) vào dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là (Cho H = 1, C = 12, O = 16, Ca = 40)
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Vì Ca(OH)2 dư nên
→ m = 16g
Câu 2:
15/07/2024Muối nào sau đây khi bị nhiệt phân đến khối lượng không đổi sinh ra oxit bazơ?
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Câu 3:
21/07/2024Điện phân nóng chảy muối clorua của một kim loại kiềm, thu được 0,672 lít khí ở anot và 1,38 gam kim loại ở catot. Công thức phân tử của muối kim loại kiềm là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Gọi công thức phân tử của muối là MCl
Theo phương trình:
→ M = 23 (Na)
Vậy công thức của muối là NaCl
Câu 4:
13/07/2024Hiđroxit nào sau đây dễ tan trong nước ở điều kiện thường?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
NaOH dễ tan trong nước ở điều kiện thường.
Câu 5:
21/07/2024Ở nhiệt độ cao, khí CO khử được oxit nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Khí CO khử được oxit của các kim loại đứng sau Al.
FeO + CO Fe + CO2
Câu 6:
17/07/2024Cặp chất nào sau đây gây nên tính cứng vĩnh cửu của nước?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Nước cứng vĩnh cửu là nước cứng do các muối CaCl2; MgCl2; CaSO4; MgSO4 gây ra.
Câu 7:
13/07/2024Phèn chua được dùng trong ngành công nghiệp thuộc da, công nghiệp giấy, chất cấm màu trong ngành nhuộm vải, chất làm trong nước. Công thức hoá học của phèn chua là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Công thức hóa học của phèn chua là: K2SO4.Al2(SO4)3.24H2O.
Câu 8:
21/07/2024Hòa tan hoàn toàn m gam hỗn hợp gồm Ba và BaO vào nước dư, thu được dung dịch X và 1,12 lít khí H2. Dẫn từ từ đến dư khí CO2 vào dung dịch X, sự phụ thuộc của khối lượng kết tủa (y gam) vào thể tích khí CO2 tham gia phản ứng (x lít) được biểu diễn như đồ thị:
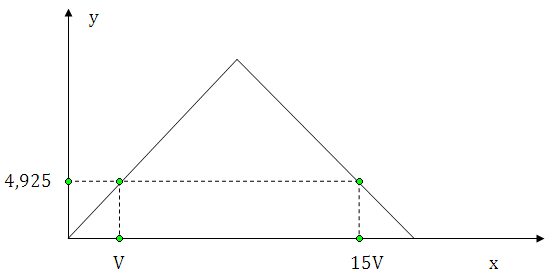
Giá trị của m là (Cho H = 1, C = 12, O = 16, Ba = 137)
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Tại
Tại
Bảo toàn C:
Bảo toàn Ba:
Mà
→ m = 29,80g
Câu 9:
13/07/2024Phát biểu nào dưới đây không đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Ăn mòn hóa học không phát sinh dòng điện.
Câu 10:
22/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
2K + 2H2O → 2KOH + H2
Câu 11:
13/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Để bảo vệ vỏ tàu biển bằng thép, người ta gắn vào vỏ tàu (phần ngâm dưới nước) một miếng kim loại Zn
Câu 12:
13/07/2024Trong các chất sau, chất nào là hidroxit lưỡng tính?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Al(OH)3 là hiđroxit lưỡng tính
Câu 13:
23/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Gọi
→ mdung dịch còn lại = 267,5 – 375x gam
→ x = 0,12
→ m = 45 gam
Câu 14:
13/07/2024Thạch cao nung được dùng để nặn tượng, đúc khuôn, bó bột khi gãy xương,... Thạch cao nung có công thức là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Công thức hóa học của thạch cao nung là CaSO4.H2O
Câu 15:
23/07/2024Hòa tan 4,7 gam K2O vào 195,3 ml nước. Nồng độ phần trăm của dung dịch thu được là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
→ mKOH = 5,6 gam
Mà mdung dịch = 4,7 + 195,3 = 200 gam
Câu 16:
22/07/2024Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Al được điều chế bằng phương pháp điện phân nóng chảy Al2O3.
Câu 17:
15/07/2024Kim loại đứng đầu về độ phổ biến trong lớp vỏ Trái Đất là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Kim loại Al phổ biến nhất trong vỏ trái đất.
Câu 18:
23/07/2024Sản phẩm của phản ứng giữa kim loại Mg với khí oxi là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
2Mg + O2 → 2MgO
Câu 19:
19/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Kim loại kiềm thổ thuộc nhóm IIA trong bảng tuần hoàn.
Câu 20:
19/07/2024Trong công nghiệp, quặng boxit dùng để sản xuất kim loại nhôm. Thành phần chính của quặng boxit là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Thành phần chính của quặng boxit là: Al2O3.2H2O
Câu 21:
13/07/2024Phản ứng nào sau đây là phản ứng nhiệt nhôm ?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Phản ứng nhiệt nhôm là phản ứng giữa Al với oxit kim loại sau Al.
Câu 22:
20/07/2024Natri hiđrocacbonat được dùng làm thuốc giảm đau dạ dày do thừa axit. Công thức của natri hiđrocacbonat là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Natri hiđrocacbonat có công thức là NaHCO3
Câu 23:
14/07/2024Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Thí nghiệm nhúng thanh Zn vào dung dịch H2SO4 loãng chỉ xảy ra ăn mòn hóa học.
Câu 24:
21/07/2024Cho các kim loại sau: Na, Zn, Al và Ag. Số kim loại điều chế được bằng phương pháp điện phân dung dịch (điện cực trơ) là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Kim loại điều chế được bằng phương pháp điện phân dung dịch là: Zn và Ag.
Câu 25:
15/07/2024Kim loại nào sau đây là kim loại kiềm thổ?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Các kim loại kiềm thổ là: Be, Mg, Ca, Ba, Sr.
Câu 26:
22/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Ca(HCO3)2 CaCO3↓ + CO2↑ + H2O
Câu 27:
16/07/2024 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
→ m = 0,12. 133,5 = 16,02g
Câu 28:
16/07/2024Đốt cháy hoàn toàn m gam Al trong khi O2 lấy dư, thu được 20,4 gam Al2O3. Giá trị của m là (Cho O = 16, Al = 27)
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
→ m = 0,4.27 = 10,8 gam.
Câu 29:
23/07/2024Cho mẫu Na vào dung dịch CuSO4 thì quan sát được hiện tượng là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
2Na + 2H2O → 2NaOH + H2↑
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
Câu 30:
21/07/2024Nung 38,4 gam hỗn hợp X gồm Al, Fe2O3, Fe3O4 ở nhiệt độ cao trong điều kiện không có oxi, thu được chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư thì có 0,4 mol NaOH đã phản ứng, sau phản ứng thu được V lít khí H2 và chất rắn Z. Cho Z tác dụng với dung dịch HCl dư, thu được 3,5V lít khí H2. Thể tích các khí đo ở cùng điều kiện và các phản ứng xảy ra hoàn toàn. Thành phần % theo khối lượng của Fe2O3 trong X là (Cho H = 1, O = 16, Na =23, Al = 27, Fe =56, Cl =35,5)
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Ta có: nAl ban đầu = nNaOH = 0,4 mol
Gọi nAl dư = a mol
Đặt b và c là số mol Fe2O3 và Fe3O4
→ mX = 0,4.27 + 160b + 232c = 38,4
Bảo toàn Fe → 2b + 3c = 5,25a
Bảo toàn e → 3(0,4 - a) = 6b + 8c
Bài thi liên quan
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 1)
-
40 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 2)
-
40 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 3)
-
40 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 4)
-
40 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 5)
-
32 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 7)
-
40 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 8)
-
32 câu hỏi
-
90 phút
-
-
Đề thi Hóa Học 12 giữa kì 2 có đáp án (đề 9)
-
29 câu hỏi
-
90 phút
-
Có thể bạn quan tâm
- Đề thi Hóa Học 12 giữa kì 2 có đáp án (2824 lượt thi)
- 30 Câu trắc nghiệm bài thi giữa kì 2 có đáp án (306 lượt thi)
- 40 câu trắc nghiệm bài thi học kì 2 có đáp án (300 lượt thi)
- Top 12 Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 1) (2197 lượt thi)
- Top 9 Đề thi giữa kì 2 Hóa 12 có đáp án (Bài số 1) (1644 lượt thi)
- Top 8 Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 2) (1237 lượt thi)
- Top 9 Đề thi giữa kì 2 Hóa 12 có đáp án (Bài số 2) (3622 lượt thi)
- Top 9 Đề thi Hóa học 12 Học kì 2 có đáp án (1817 lượt thi)
- Đề thi cuối kì 2 Hóa 12 có đáp án (3185 lượt thi)
Các bài thi hot trong chương
- Top 4 Đề kiểm tra 15 phút Hóa 12 Học kì 1 có đáp án (Lần 1) (1134 lượt thi)
- Top 4 Đề thi Hóa học 12 Học kì 1 có đáp án (961 lượt thi)
- Top 4 Đề thi giữa kì 1 Hóa 12 có đáp án (Lần 1) (808 lượt thi)
- Top 4 Đề thi giữa kì 1 Hóa 12 có đáp án (Lần 2) (806 lượt thi)
- Top 4 Đề thi Hóa học 12 Học kì 1 chọn lọc, có đáp án (739 lượt thi)
- Đề kiểm tra 1 tiết Hóa học 12 có đáp án (Bài kiểm tra số 1) (367 lượt thi)
- Đề kiểm tra 1 tiết Hóa học 12 có đáp án (Bài kiểm tra số 2) (327 lượt thi)
- 40 Câu trắc nghiệm bài thi giữa kì 2 có đáp án (303 lượt thi)
