Sách bài tập Hóa 11 Bài 6 (Cánh diều): Sulfur và sulfur dioxide
Với giải sách bài tập Hóa 11 Bài 6: Sulfur và sulfur dioxide sách Cánh diều hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa 11 Bài 6.
Giải SBT Hóa 11 Bài 6: Sulfur và sulfur dioxide
Bài 6.1 trang 20 SBT Hoá học 11: Những phát biểu nào sau đây là đúng?
(a) Trong tự nhiên, sulfur tồn tại chủ yếu ở dạng muối sulfide và muối sulfate của một số kim loại.
(b) Là một phi kim khá hoạt động nên trong tự nhiên không tìm thấy sulfur đơn chất.
(c) Trứng gà ung có mùi thối đặc trưng một phần là do các hợp chất của sulfur có trong trứng phân huỷ gây ra.
(d) Nguyên tố sulfur có mặt trong một số loại thực vật, đặc biệt là các loại rau quả có mùi mạnh như hành tây, sầu riêng,…
(e) Thành phần chính của quặng pyrite là hợp chất của sulfur và chì (lead, Pb).
Lời giải:
Đáp án đúng là: (a), (c), (d).
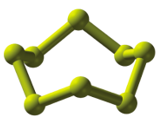
Bài 6.2 trang 20 SBT Hoá học 11: Phân tử sulfur, S8, có cấu tạo như Hình 6.
a) Giải thích vì sao phân tử này không phân cực.
b) Những phát biểu nào dưới đây là phù hợp với tính không phân cực của sulfur?
|
(b1) Hầu như không tan trong nước. |
Hình 6 |
|
(b2) Tan nhiều trong dung môi ethanol |
|
|
(b3) Tan tốt trong dung môi không phân cực như carbon disulfide (CS2). |
|
|
(b4) Có tính sát khuẩn |
Lời giải:
a) Các liên kết S−S trong S8 đều là liên kết cộng hóa trị không cực nên hợp chất S8 cũng là hợp chất không phân cực.
b) (b1), (b3).
Khi sử dụng khí thiên nhiên hoặc than làm nhiên liệu đều thải vào không khí các chất khí gây ô nhiễm. Giải thích.
Lời giải:
Khí thiên nhiên và than khi cháy sẽ toả rất nhiều nhiệt, tạo điều kiện cho các hợp chất như hydrogen sulfide và các hợp chất chứa S, N bị oxi hoá sinh ra các khí độc gây ô nhiễm như SO2, NO, NO2,…, các khí này là nguyên nhân gây mưa acid. Ví dụ: 2H2S(g) + 3O2(g) 2SO2(g) + 2H2O(l)
Bài 6.4 trang 21 SBT Hoá học 11: Những ý kiến nào sau đây về sulfur dioxide (SO2) là đúng?
(a) Có độc tính đối với con người.
(b) Phản ứng được với đá vôi.
(c) Khí này được tạo thành từ hoạt động của núi lửa trong tự nhiên, từ quá trình đốt cháy nhiên liệu hoá thạch của con người,…
(d) Là oxide lưỡng tính.
Lời giải:
|
Cột A |
Cột B |
|
a) Sulfur
|
1. Là chất khí ở điều kiện thường. |
|
2. Ở điều kiện thường, phân tử có 8 nguyên tử. |
|
|
3. Dễ tan trong nước. |
|
|
b) Sulfur dioxide
|
4. Hòa tan trong dung môi phù hợp để làm thuốc trị bệnh ngoài da. |
|
5. Dùng để tẩy trắng vải, sợi. |
|
|
6. Có tính khử và tính oxi hóa. |
Lời giải:
Đáp án đúng là: a – 2, 4, 6; b – 1, 3, 5, 6.
a) Tan trong nước tạo thành acid yếu H2SO3.
b) Phản ứng với dung dịch base tạo muối và nước.
c) Phản ứng với oxide base (basic oxide) tạo muối.
Lời giải:
a) SO2 + H2O ⇌ H2SO3
b) SO2 + 2NaOH ⟶ Na2SO3 + H2O
c) SO2 + CaO ⟶ CaSO3
Tính giá trị biến thiên enthalpy chuẩn của phản ứng sau:
SO2(g) + O2(g) → SO3(g)
Từ đó, hãy cho biết phản ứng trên có thuận lợi về mặt năng lượng không.
Lời giải:
Giá trị biến thiên enthalpy chuẩn của phản ứng là:
= (−395,7) − (−296,8) = −98,9 (kJ)
Giá trị biến thiên enthalpy chuẩn của phản ứng có giá trị âm, tức phản ứng toả nhiệt nên thuận lợi về mặt năng lượng.
H2S(g) + O2(g) → SO2(g) + H2O(g) (1)
H2S(g) + O2(g) → S(s) + H2O(g) (2)
Cho biết giá trị enthalpy tạo thành chuẩn của H2S(g), SO2(g) và H2O(g) lần lượt là: −20,7 kJ mol−1; −296,8 kJ mol−1 và −241,8 kJ mol−1.
a) Tính giá trị biến thiên enthalpy chuẩn của mỗi phản ứng trên. Ở 298 K, mỗi phản ứng có thuận lợi về mặt năng lượng không?
b) Trong môi trường không khí mà nồng độ oxygen bị suy giảm, hãy dự đoán hydrogen sulfide sẽ dễ chuyển hoá thành sulfur dioxide hay sulfur. Giải thích.
Lời giải:
a) Cả hai phản ứng đều thuận lợi về mặt năng lượng vì giá trị biến thiên enthalpy chuẩn của hai phản ứng đều âm (−517,9 kJ và −221,1 kJ).
b) Hydrogen sulfide sẽ dễ chuyển thành sulfur dioxide theo phản ứng (2), vì phản ứng (2) cần ít oxygen hơn so với phản ứng (1).
CaCO3(s) + SO2(g) ⟶ CaSO3(s) + CO2(g)
a) Vì sao phản ứng trên được gọi là phản ứng khử sulfur trong khí thải?
|
Hợp chất |
CaSO3(s) |
CaCO3(s) |
SO2(g) |
CO2(g) |
|
(kJ mol−1) |
−1 634,9 |
−1 207,6 |
−296,8 |
−393,5 |
c) Trong phản ứng trên, vì sao đá vôi phải được dùng ở dạng bột?
Lời giải:
a) Vì S trong khí thải (SO2) được thay thế bằng C (trong CO2).
b) = −524,0 kJ. Phản ứng toả nhiệt nên thuận lợi về năng lượng.
c) Để tăng diện tích tiếp xúc giữa calcium carbonate với khí nhằm tăng tốc độ phản ứng.
d) Là phản ứng oxi hoá − khử vì làm tăng số oxi hoá của sulfur từ +4 (trong CaSO3) lên +6 (trong CaSO4).
Xem thêm giải Sách bài tập Hóa học 11 bộ sách Cánh diều hay, chi tiết khác:
Bài 2: Sự điện li trong dung dịch nước. Thuyết Br∅nsted – Lowry về acid - base
Bài 3: PH của dung dịch. Chuẩn độ acid – base
Xem thêm các chương trình khác:
- Soạn văn lớp 11 Cánh diều (hay nhất)
- Văn mẫu lớp 11 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 11 – Cánh diều
- Tác giả tác phẩm Ngữ văn 11 - Cánh diều
- Giải SBT Ngữ văn 11 – Cánh diều
- Bố cục tác phẩm Ngữ văn 11 – Cánh diều
- Giải Chuyên đề học tập Ngữ văn 11 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn lớp 11 – Cánh diều
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 – Cánh diều
- Giải Chuyên đề học tập Toán 11 – Cánh diều
- Lý thuyết Toán 11 - Cánh diều
- Giải sbt Toán 11 – Cánh diều
- Giải sgk Tiếng Anh 11 – ilearn Smart World
- Giải sbt Tiếng Anh 11 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh 11 ilearn Smart World đầy đủ nhất
- Giải sgk Vật lí 11 – Cánh diều
- Lý thuyết Vật lí 11 – Cánh diều
- Giải sbt Vật lí 11 – Cánh diều
- Giải Chuyên đề học tập Vật lí 11 – Cánh diều
- Giải sgk Sinh học 11 – Cánh diều
- Lý thuyết Sinh học 11 – Cánh diều
- Giải Chuyên đề học tập Sinh học 11 – Cánh diều
- Giải sbt Sinh học 11 – Cánh diều
- Giải sgk Giáo dục Kinh tế và Pháp luật 11 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 11 – Cánh diều
- Lý thuyết Kinh tế pháp luật 11 – Cánh diều
- Giải sbt Kinh tế pháp luật 11 – Cánh diều
- Giải sgk Lịch sử 11 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 11 – Cánh diều
- Lý thuyết Lịch sử 11 - Cánh diều
- Giải sbt Lịch sử 11 – Cánh diều
- Giải sgk Địa lí 11 – Cánh diều
- Giải Chuyên đề học tập Địa lí 11 – Cánh diều
- Lý thuyết Địa lí 11 - Cánh diều
- Giải sbt Địa lí 11 – Cánh diều
- Giải sgk Công nghệ 11 – Cánh diều
- Lý thuyết Công nghệ 11 - Cánh diều
- Giải sbt Công nghệ 11 – Cánh diều
- Giải sgk Tin học 11 – Cánh diều
- Giải Chuyên đề học tập Tin học 11 – Cánh diều
- Lý thuyết Tin học 11 - Cánh diều
- Giải sbt Tin học 11 – Cánh diều
- Giải sgk Giáo dục quốc phòng an ninh 11 – Cánh diều
- Lý thuyết Giáo dục quốc phòng 11 – Cánh diều
- Giải sbt Giáo dục quốc phòng 11 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 – Cánh diều