Pha chế 100 ml dung dịch natri clorua có nồng độ 0,2M
Với giải thực hành 2 trang 152 sgk Hóa học lớp 8 được biên soạn lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập môn Hóa 8. Mời các bạn đón xem:
Giải Hóa 8 Bài 45: Bài thực hành 7: Pha chế dung dịch theo nồng độ
Thực hành 2 trang 152 Hóa học lớp 8: Pha chế 100 ml dung dịch natri clorua có nồng độ 0,2M.
Phần tính toán:
Đổi 100 ml = 0,1 lít
Số mol chất tan (NaCl) cần dùng là:
nNaCl = CM.V = 0,2.0,1 = 0,02 mol
Khối lượng NaCl cần dùng là:
mNaCl = nNaCl.MNaCl
= 0,02.(23 + 35,5) = 1,17 gam
Phần thực hành:
|
Chuẩn bị |
Cách tiến hành |
|
- Dụng cụ: + Cốc chia độ có dung tích 200 ml. + Cân điện tử. + Đũa, thìa. |
- Cân 1,17g NaCl khan cho vào cốc chia độ - Rót từ từ nước cất vào cốc và khuấy đều cho đến vạch 100ml → Ta được 100 ml dung dịch NaCl 0,2M.
|
|
- Hóa chất + Muối natri clrua + Nước cất. |
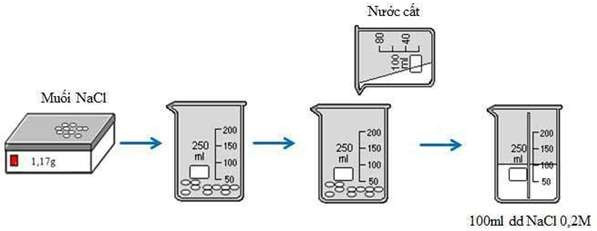
Hình 2: Quá trình pha chế 100 ml dung dịch NaCl 0,2M
Xem thêm lời giải sách bài tập Hóa học lớp 8 hay, chi tiết khác:
Thực hành 1 trang 152 Hóa 8: Pha chế 50 g dung dịch đường có nồng độ 15%...
Thực hành 3 trang 153 Hóa 8: Pha chế 50 g dung dịch đường 5% từ dung dịch đường có nồng độ 15% ở trên...
Thực hành 4 trang 153 Hóa 8: Pha chế 50 ml dung dịch natri clorua có nồng độ 0,1M...
Xem thêm các chương trình khác:
- Tóm tắt tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Soạn văn 8 (hay nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Soạn văn 8 (ngắn nhất) | Để học tốt Ngữ văn lớp 8 (sách mới)
- Văn mẫu lớp 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Tác giả - tác phẩm Ngữ văn 8 (Sách mới) | Kết nối tri thức, Cánh diều, Chân trời sáng tạo
- Giải sgk Vật Lí 8
- Giải sbt Vật Lí 8
- Lý thuyết Vật Lí 8
- Giải vở bài tập Vật lí 8
- Giải SGK Toán 8 | Giải bài tập Toán 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Toán 8 (sách mới) | Sách bài tập Toán 8
- Bài tập Ôn luyện Toán lớp 8
- Các dạng bài tập Toán lớp 8
- Lý thuyết Toán lớp 8 (sách mới) | Kiến thức trọng tâm Toán 8
- Giáo án Toán lớp 8 mới nhất
- Bài tập Toán lớp 8 mới nhất
- Chuyên đề Toán lớp 8 mới nhất
- Giải sgk Tiếng Anh 8 (sách mới) | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2
- Giải sgk Tiếng Anh 8 | Giải bài tập Tiếng Anh 8 Học kì 1, Học kì 2 (sách mới)
- Giải sbt Tiếng Anh 8 (sách mới) | Sách bài tập Tiếng Anh 8
- Giải sbt Tiếng Anh 8 (thí điểm)
- Giải sgk Tin học 8 | Giải bài tập Tin học 8 Học kì 1, Học kì 2 (sách mới)
- Giải sgk Lịch Sử 8 | Giải bài tập Lịch sử 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Lịch sử 8 (sách mới) | Kiến thức trọng tâm Lịch sử 8
- Giải vở bài tập Lịch sử 8
- Giải Tập bản đồ Lịch sử 8
- Đề thi Lịch Sử 8
- Giải vở bài tập Sinh học 8
- Giải sgk Sinh học 8
- Lý thuyết Sinh học 8
- Giải sgk Giáo dục công dân 8 | Giải bài tập Giáo dục công dân 8 Học kì 1, Học kì 2 (sách mới)
- Lý thuyết Giáo dục công dân 8 (sách mới) | Kiến thức trọng tâm GDCD 8
- Lý thuyết Địa Lí 8 (sách mới) | Kiến thức trọng tâm Địa Lí 8
- Giải sgk Địa Lí 8 | Giải bài tập Địa Lí 8 Học kì 1, Học kì 2 (sách mới)
- Giải Tập bản đồ Địa Lí 8
- Đề thi Địa lí 8
