Giải Hóa 12 Bài 20 (Cánh diều): Sơ lược về kim lại chuyển tiếp dãy thứ nhất
Với giải bài tập Hóa 12 Bài 20: Sơ lược về kim lại chuyển tiếp dãy thứ nhất sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa 12 Bài 20.
Giải Hóa 12 Bài 20: Sơ lược về kim lại chuyển tiếp dãy thứ nhất
Mở đầu trang 135 Hóa học 12: Kim loại chuyển tiếp dãy thứ nhất gồm 9 nguyên tố từ Sc (Z =21) đến Cu (Z=29) trong bảng tuần hoàn các nguyên tố hoá học. Các nguyên tố này thường thể hiện nhiều trạng thái oxi hoá khác nhau. Chẳng hạn, nguyên tố sắt (Z = 26) có số oxi hoá +2 trong hợp chất FeCl2, có số oxi hoá +3 trong hợp chất FeCl3.
a) Vì sao kim loại chuyển tiếp dãy thứ nhất thường tạo được nhiều hợp chất với các số oxi hoá dương khác nhau?
b) Nêu một số tính chất và ứng dụng của đơn chất kim loại chuyển tiếp dãy thứ nhất.
Lời giải:
a) Nguyên tử của kim loại chuyển tiếp dãy thứ nhất có electron hóa trị ở cả phân lớp 4s và 3d nên có nhiều electron hóa trị. Đồng thời có độ âm điện nhỏ nên nguyên tử của nguyên tố kim loại chuyển tiếp thể hiện nhiều số oxi hóa dương khác nhau trong hợp chất.
b) Tính chất: khối lượng riêng lớn, cứng và khó nóng chảy.
Ứng dụng: tạo hợp kim, làm lớp bảo vệ chống ăn mòn cho các dụng cụ, máy móc, thiết bị, xe cộ, đồ gia dụng, …
Câu hỏi 1 trang 136 Hóa học 12: Dựa vào Bảng 20.1, giải thích vì sao nhiều kim loại chuyển tiếp dãy thứ nhất thường có số oxi hoá +2 trong các hợp chất.
Lời giải:
Dựa vào Bảng 20.1, ta thấy cấu hình electron lớp ngoài cùng của kim loại chuyển tiếp dãy thứ nhất đa số là 4s2 do xu hướng xếp đầy electron ở phân lớp 4s và tăng dần số electron ở phân lớp 3d.
Do đó, kim loại chuyển tiếp dãy thứ nhất thường nhường 2 electron lớp ngoài cùng (ở phân lớp 4s) để có số oxi hoá +2 trong các hợp chất.
Câu hỏi 2 trang 137 Hóa học 12: Xác định số oxi hoá của sắt trong các hợp chất sau: FeO, Fe2O3, Fe3O4 (hay FeO.Fe2O3).
Lời giải:
Số oxi hóa của Fe trong FeO là +2.
Số oxi hóa của Fe trong Fe2O3 là +3.
Số oxi hóa của Fe trong Fe3O4 là +8/3 (hay +2 và + 3).
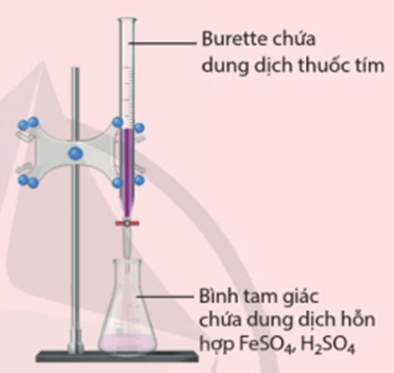
Thí nghiệm 1 trang 138 Hóa học 12: Xác định nồng độ của dung dịch FeSO4 bằng dung dịch KMnO4 (dung dịch thuốc tím)
Chuẩn bị:
- Hoá chất: Dung dịch thuốc tím KMnO4 có nồng độ chính xác 0,02 M, dung dịch FeSO4 có nồng độ khoảng 0,1 M; dung dịch H2SO4 20%.
- Dụng cụ : Burette loại 25 mL, bình tam giác loại 100 mL.
Tiến hành:
Hình 20.1. Bộ dụng cụ thí nghiệm chuẩn độ muối FeSO4 trong môi trường acid bằng dung dịch thuốc tím
- Lắp bộ dụng cụ như Hình 20.1. Cho dung dịch thuốc tím vào burette đến vạch 0, đồng thời bảo đảm không còn bọt khí trong burette. Cho 10 mL dung dịch FeSO4 và 5 mL dung dịch H2SO4 20% vào bình tam giác.
- Mở khoá để nhỏ từ từ từng giọt dung dịch thuốc tím vào bình tam giác, đồng thời lắc đều bình.
- Tiếp tục nhỏ dung dịch thuốc tím (vẫn duy trì lắc đều bình) tới khi dung dịch trong bình tam giác xuất hiện màu hồng nhạt bởi một giọt thuốc tím dư, không mất màu trong khoảng 20 giây thì kết thúc chuẩn độ (khoá burette).
- Ghi lại thể tích dung dịch thuốc tím đã dùng.
Lặp lại thí nghiệm ít nhất hai lần nữa.
Yêu cầu: Xác định nồng độ của dung dịch FeSO4. Biết phương trình hoá học của phản ứng diễn ra trong quá trình chuẩn độ là:
5Fe2+(aq) + (aq) + 8H+(aq) →5Fe3+(aq) + Mn2+(aq) + 4H₂O(1)
Lời giải:
Gọi thể tích dung dịch KMnO4 đã dùng ở các lần đo lần lượt là V1, V2, …, Vn
Ta có thể tích trung bình của dung dịch KMnO4 là:
Theo phương trình chuẩn độ, ta có:
⇒
Thay số liệu vào công thức trên ta xác định được nồng độ của dung dịch FeSO4.
Thí nghiệm 2 trang 138 Hóa học 12: Kiểm tra sự có mặt của cation Cu2+ hoặc Fe3+ trong dung dịch
Chuẩn bị:
- Hoá chất: Các dung dịch CuSO4 0,1 M; FeCl3 0,1 M; NaOH 0,1 M.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt.
Tiến hành:
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch CuSO4.
- Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm chứa khoảng 1 mL dung dịch FeCl3.
Yêu cầu: Quan sát, giải thích hiện tượng và viết phương trình hoá học minh hoạ.
Lời giải:
Hiện tượng:
- Ở ống nghiệm chứa dung dịch CuSO4: xuất hiện kết tủa màu xanh, đó là Cu(OH)2.
- Ở ống nghiệm chứa dung dịch FeCl3: xuất hiện kết tủa màu nâu đỏ, đó là Fe(OH)3.
Phương trình hóa học:
2NaOH(aq) + CuSO4(aq) ⟶ Cu(OH)2(s) + Na2SO4(aq)
3NaOH(aq) + FeCl3(aq) ⟶ Fe(OH)3(s) + 3NaCl(aq)
Luyện tập trang 140 Hóa học 12: Có nên sử dụng các kim loại chuyển tiếp dãy thứ nhất làm dây chảy trong các cầu chì không? Giải thích.
Lời giải:
Không nên sử dụng các kim loại chuyển tiếp dãy thứ nhất làm dây chảy trong các cầu chì. Vì các kim loại chuyển tiếp dãy thứ nhất có nhiệt độ nóng chảy cao nên không thể kịp thời ngắt mạch khi chập cháy điện, gây hiện tượng nổ thiết bị.
Bài tập
Bài 1 trang 141 Hóa học 12:
a) Từ Bảng 20.1, hãy chỉ ra xu hướng biến đổi về số electron hoá trị của các nguyên tử nguyên tố từ scandium đến cobalt.
b) Từ Bảng 20.4, hãy chỉ ra xu hướng biến đổi về khối lượng riêng của các kim loại từ scandium đến đồng.
Lời giải:
a) Từ Bảng 20.1, ta thấy số electron hoá trị của các nguyên tử nguyên tố từ scandium đến cobalt có xu hướng tăng dần (tăng từ 3 đến 9).
b) Từ Bảng 20.4, ta thấy khối lượng riêng của các kim loại từ scandium đến đồng có xung hướng tăng dần.
Bài 2 trang 141 Hóa học 12: Potassium là nguyên tố họ s, thuộc cùng chu kì 4 với các nguyên tố chuyển tiếp dãy thứ nhất.
Từ Bảng 17.1 và Bảng 20.4, hãy chỉ ra sự khác biệt về khối lượng riêng, độ cứng và nhiệt độ nóng chảy giữa các kim loại chuyển tiếp dãy thứ nhất với kim loại potassium.
Lời giải:
Từ Bảng 17.1 và Bảng 20.4, ta thấy khối lượng riêng, độ cứng và nhiệt độ nóng chảy của các kim loại chuyển tiếp dãy thứ nhất lớn hơn nhiều so với của kim loại potassium.
Bài 3 trang 141 Hóa học 12: Một mẫu chất có thành phần chính là muối Mohr. Muối Mohr có công thức hoá học là (NH4)2SO4.FeSO4.6H2O. Hoà tan 0,2151 g mẫu chất trong dung dịch sulfuric acid loãng dư, thu được dung dịch có chứa cation Fe2+. Lượng Fe2+ trong dung dịch này phản ứng vừa đủ với 5,40 mL dung dịch thuốc tím nồng độ 0,020 M (Các chất và ion khác trong dung dịch không phản ứng với thuốc tím). Xác định:
a) Số mg sắt có trong mẫu chất.
b) Phần trăm khối lượng của (NH4)2SO4.FeSO4.6H2O trong mẫu chất.
Lời giải:
Phương trình hóa học:
5Fe2+(aq) + (aq) + 8H+(aq) →5Fe3+(aq) + Mn2+(aq) + 4H₂O(1)
Ta có: = 0,02 . 5,4 . 10-3 = 1,08 . 10-4 (mol)
Theo phương trình: = 5 . 1,08 . 10-4 = 5,4 . 10-4 (mol)
a) Khối lượng sắt có trong mẫu chất là: 56 . 5,4 . 10-4 = 0,03024 (g) = 30,24 (mg)
b) Ta có: = 5,4 . 10-4 (mol)
⇒ = 392 . 5,4 . 10-4 = 0,21168 (g)
⇒ =
Xem thêm các chương trình khác:
- Soạn văn 12 Cánh diều (hay nhất)
- Văn mẫu 12 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 12 – Cánh diều
- Tác giả tác phẩm Ngữ văn 12 - Cánh diều
- Bố cục tác phẩm Ngữ văn 12 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn 12 – Cánh diều
- Giải sgk Toán 12 – Cánh diều
- Giải Chuyên đề học tập Toán 12 – Cánh diều
- Lý thuyết Toán 12 – Cánh diều
- Giải sbt Toán 12 – Cánh diều
- Giải sgk Tiếng Anh 12 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh lớp 12 ilearn Smart World đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh lớp 12 ilearn Smart World đầy đủ nhất
- Giải sbt Tiếng Anh 12 – iLearn Smart World
- Giải sgk Vật lí 12 – Cánh diều
- Giải Chuyên đề học tập Vật lí 12 – Cánh diều
- Lý thuyết Vật lí 12 – Cánh diều
- Giải sbt Vật lí 12 – Cánh diều
- Giải sgk Sinh học 12 – Cánh diều
- Giải Chuyên đề học tập Sinh học 12 – Cánh diều
- Lý thuyết Sinh học 12 – Cánh diều
- Giải sbt Sinh học 12 – Cánh diều
- Giải sgk Lịch sử 12 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 12 – Cánh diều
- Giải sbt Lịch sử 12 – Cánh diều
- Giải sgk Địa lí 12 – Cánh diều
- Giải Chuyên đề học tập Địa lí 12 – Cánh diều
- Giải sbt Địa lí 12 – Cánh diều
- Giải sgk Tin học 12 – Cánh diều
- Giải Chuyên đề học tập Tin học 12 – Cánh diều
- Giải sbt Tin học 12 – Cánh diều
- Lý thuyết Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 – Cánh diều
- Giải sgk Kinh tế pháp luật 12 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Cánh diều
- Giải sbt Kinh tế pháp luật 12 – Cánh diều
- Giải sgk Giáo dục quốc phòng 12 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 – Cánh diều