Giải Hóa 12 Bài 11 (Cánh diều): Nguồn điện hoá học
Với giải bài tập Hóa 12 Bài 11: Nguồn điện hoá học sách Cánh diều hay nhất, chi tiết giúp học sinh dễ dàng làm bài tập Hóa 12 Bài 11.
Giải Hóa 12 Bài 11: Nguồn điện hoá học
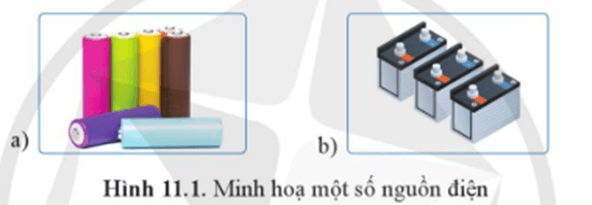
Mở đầu trang 76 Hóa học 12: Quan sát hình dưới đây:
Hình 11.1 mô tả một số loại pin thường được sử dụng trong đời sống. Vậy hoạt động của các pin trên dựa trên loại phản ứng hoá học nào?
Lời giải:
Hoạt động của các pin trên dựa trên phản ứng oxi hóa – khử.
Câu hỏi 1 trang 77 Hóa học 12: Khi nhúng một thành kẽm vào dung dịch CuSO4 thì electron từ thanh kẽm sẽ chuyển trực tiếp hay gián tiếp đến ion Cu2+ trong dung dịch? Giải thích.
Lời giải:
Electron từ thanh kẽm sẽ chuyển trực tiếp đến ion Cu2+ trong dung dịch vì thanh kẽm được nhúng (tiếp xúc trực tiếp) với CuSO4.
Luyện tập 1 trang 77 Hóa học 12: Hãy mô tả cấu tạo mỗi pin Galvani sau:
a) Fe-Cu.
b) Cu-Ag.
c) Fe-Ag.
Lời giải:
a) Pin Galvani Fe-Cu được tạo nên từ hai cặp oxi hóa – khử là: Fe2+/Fe và Cu2+/Cu, thanh kim loại Fe được nhúng trực tiếp vào cốc đựng dung dịch Fe2+, thanh kim loại Cu được nhúng trực tiếp vào cốc đựng dung dịch Cu2+. Hai cốc đựng dung dịch muối trong pin Galvani được nối với nhau bởi một cầu muối. Hai thanh kim loại được nối vào 1 vôn kế bằng dây dẫn để xác định được hoạt động của pin.
b) Pin Galvani Cu-Ag được tạo nên từ hai cặp oxi hóa – khử là: Cu2+/Cu và Ag+/Ag thanh kim loại Cu được nhúng trực tiếp vào cốc đựng dung dịch Cu2+, thanh kim loại Ag được nhúng trực tiếp vào cốc đựng dung dịch Ag+. Hai cốc đựng dung dịch muối trong pin Galvani được nối với nhau bởi một cầu muối. Hai thanh kim loại được nối vào 1 vôn kế bằng dây dẫn để xác định được hoạt động của pin.
c) Pin Galvani Fe-Ag được tạo nên từ hai cặp oxi hóa – khử là: Fe2+/Fe và Ag+/Ag thanh kim loại Fe được nhúng trực tiếp vào cốc đựng dung dịch Fe2+, thanh kim loại Ag được nhúng trực tiếp vào cốc đựng dung dịch Ag+. Hai cốc đựng dung dịch muối trong pin Galvani được nối với nhau bởi một cầu muối. Hai thanh kim loại được nối vào 1 vôn kế bằng dây dẫn để xác định được hoạt động của pin.
Luyện tập 2 trang 78 Hóa học 12: Hãy nêu nguyên tắc hoạt động của pin Galvani Zn-Ag và viết phương trình hoá học của phân ứng xảy ra trong pin.
Lời giải:
Nguyên tắc hoạt động của pin Galvani Zn-Ag:
|
Pin Galvani Zn-Ag |
|
|
Anode (Zn): Zn nhường electron, chuyển thành ion Zn2+ tan vào dung dịch. |
Cathode (Ag): Ion Ag+ trong dung dịch nhận electron (từ điện cực Zn qua dây dẫn chuyển sang điện cực Ag) chuyển thành Ag bám lên điện cực Ag. |
|
Phản ứng diễn ra trong pin là: Zn(s) + 2Ag+(aq) ⟶ Zn2+(aq) + 2Ag(s) |
|
Câu hỏi 2 trang 78 Hóa học 12: Cho biết thế điện cực chuẩn của cặp = -0,763V và = 0,340V.
Hãy tìm biểu thức liên hệ hai giá trị này với giá trị sức điện động chuẩn của pin Zn-Cu (bằng 1,103 V).
Lời giải:
Zn-Cu = - = 0,340 – (–0,763) = 1,103 V.
Luyện tập 3 trang 78 Hóa học 12: Từ Bảng 10.1, hãy so sánh sức điện động chuẩn của pin Galvani Zn-Ni và Sn-Cu.
Lời giải:
Zn-Ni = - = –0,257 – (–0,763) = 0,506 V
Sn-Cu = - = 0,340 – (–0,138) = 0,478 V
So sánh: Sn-Cu < Zn-Ni
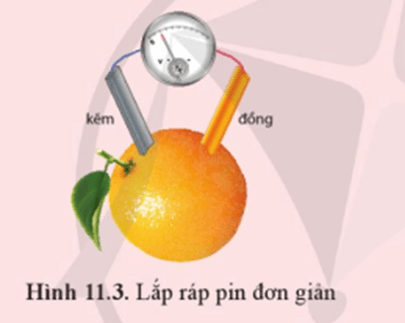
Thí nghiệm trang 79 Hóa học 12: Thực hành lắp pin đơn giản
Chuẩn bị:
- Hoá chất: Hai thanh (hoặc dây) kim loại khác nhau (ví dụ đồng, kẽm,...), dung dịch chất điện li (ví dụ dung dịch HCI, H2SO4 loãng, NaCl,... hoặc quả chanh, quả táo,...).
- Dụng cụ: Vôn kế (hoặc đèn led nhỏ để nhận biết sự xuất hiện của dòng điện), dây dẫn, cốc thuỷ tinh.
Tiến hành:
- Cắm hai thanh (hoặc dây) kim loại vào cốc chứa dung dịch chất điện li (hoặc quả chanh, quả táo,.....)
- Đo sức điện động giữa hai thanh (hoặc dây) kim loại bằng vôn kế (Hình 11.3).
Yêu cầu: Quan sát và mô tả hiện tượng xảy ra.
Chú ý an toàn: Hai thanh kim loại trong pin không được chạm vào nhau.
Lời giải:
Hiện tượng: Kim chỉ trong vôn kế dịch chuyển vì có sự xuất hiện của dòng điện.
Vận dụng 1 trang 79 Hóa học 12: Tìm hiểu và cho biết một số hạn chế nếu sử dụng pin Galvani Zn-Cu trong đèn pin.
Lời giải:
Một số hạn chế nếu sử dụng pin Galvani Zn-Cu trong đèn pin là:
- Gây ô nhiễm môi trường.
- Năng lượng chứa trong pin thấp.
- Tuổi thọ pin thấp.
Luyện tập 4 trang 80 Hóa học 12: Hãy nêu một số trường hợp sử dụng acquy trong thực tế mà em biết.
Lời giải:
Acquy trong xe máy, xe đạp điện, ô tô điện, quạt tích điện chạy bằng acquy, …
Câu hỏi 3 trang 81 Hóa học 12: Mỗi phát biểu sau đây là đúng hay sai?
a) Pin mặt trời biến đổi trực tiếp quang năng thành điện năng.
b) Pin mặt trời là nguồn năng lượng xanh.
c) Khi hoạt động, pin mặt trời không gây hiệu ứng nhà kính.
d) Khi hoạt động, pin mặt trời gây mưa acid và làm Trái Đất nóng lên.
Lời giải:
a) Đúng. Pin mặt trời biến đổi trực tiếp quang năng thành điện năng.
b) Đúng vì khi hoạt động pin mặt trời sử dụng nguồn năng lượng vô tận là ánh sáng mặt trời, không tạo ra bất cứ sản phẩm hóa học nào trong quá trình hoạt động nên thân thiện với môi trường.
c) Đúng. Khi hoạt động, pin mặt trời không gây hiệu ứng nhà kính.
d) Sai. Vì pin mặt trời không tạo ra bất kì một sản phẩm hoá học nào trong quá trình hoạt động nên thân thiện với môi trường.
Vận dụng 2 trang 81 Hóa học 12: Tìm hiểu và giải thích những vùng miền nào ở Việt Nam thích hợp với việc phát triển điện mặt trời.
Lời giải:
Các tỉnh Tây Nguyên, Nam Bộ và Nam Trung Bộ có bức xạ mặt trời cao thích hợp với việc phát triển điện mặt trời.
Bài tập
Bài 1 trang 82 Hóa học 12: Sử dụng bảng thế điện cực chuẩn, xác định sức điện động chuẩn của pin Galvani tạo bởi các cặp oxi hoá – khử sau, đồng thời chỉ ra điện cực dương, điện cực âm của pin trong mỗi trường hợp:
a) Ni2+/Ni và Ag+/Ag.
b) Zn2+/Zn và 2H+/H2
Lời giải:
a) Ni-Ag = - = 0,799 – (–0,257) = 1,056 V
Anode hay cực âm (Ni), cathode hay cực dương (Ag)
b) = - = 0 – (–0,763) = 0,763 V
Anode hay cực âm (Zn), cathode hay cực dương (H2)
Bài 2 trang 82 Hóa học 12: Nêu ý kiến của em về nhận định: Pin nhiên liệu hydrogen và pin mặt trời sẽ ngày càng được sử dụng rộng rãi trong tương lai.
Lời giải:
Theo em nhận định trên là đúng vì:
- Pin nhiện liệu hydrogen mang lại hiệu suất cao, không tạo ra các sản phẩm gây ô nhiễm môi trường.
- Pin mặt trời sử dụng nguồn năng lượng vô tận là ánh sáng mặt trời, không tạo ra bất cứ sản phẩm hóa học nào trong quá trình hoạt động nên thân thiện với môi trường.
Với ưu điểm vượt trội hơn so với nhược điểm thì tương lai con người sẽ khắc phục được những nhược điểm đang tồn tại để các nhiên liệu trên sẽ ngày càng được sử dụng rộng rãi.
Bài 3 trang 82 Hóa học 12: Phát biểu nào sau đây là đúng khi nói về pin Galvani?
A. Anode là điện cực dương.
B. Cathode là điện cực âm.
C. Ở điện cực âm xảy ra quá trình oxi hoá.
D. Dòng electron di chuyển từ cathode sang anode.
Lời giải:
Đáp án đúng là: C
A. Phát biểu sai vì: trong pin Galvani thì Anode là điện cực âm.
B. Phát biểu sai vì: trong pin Galvani thì Cathode là điện cực đương.
C. Phát biểu đúng.
D. Phát biểu sai vì: trong pin Galvani thì dòng electron di chuyển từ anode sang cathode.
Bài 4 trang 82 Hóa học 12: Những phát biểu nào sau đây là đúng?
a) Phản ứng hoá học xảy ra trong pin Galvani là phản ứng tự diễn biến.
b) Trong pin Galvani, điện cực âm là nơi xảy ra quá trình khử.
c) Sức điện động của pin Galvani là hiệu điện thế giữa hai điện cực.
d) Pin Galvani tạo ra dòng điện từ quá trình vật lí.
Lời giải:
Những phát biểu đúng là: (a)
Phát biểu b) sai vì trong pin Galvani, điện cực âm là nơi xảy ra quá trình oxi hóa.
Phát biểu c) sai vì sức điện động của pin Galvani là hiệu giữa thế điện cực chuẩn của các cặp oxi hóa khử.
Phát biểu d) sai vì pin Galvani tạo ra dòng điện từ phản ứng oxi hóa – khử gián tiếp.
Bài 5 trang 82 Hóa học 12: Cho phản ứng trong một pin Galvani như sau:
2Cr(s) + 3Cu2+(aq) → 2Cr3+(aq) + 3Cu(s)
Hãy cho biết quá trình xảy ra ở anode và cathode khi pin hoạt động.
Lời giải:
|
Pin Galvani Cr-Cu |
|
|
Anode (Cr): Quá trình oxi hóa Cr nhường electron, chuyển thành ion Cr3+ tan vào dung dịch |
Cathode (Cu): Quá trình khử Ion Cu2+ trong dung dịch nhận electron (từ điện cực Cr qua dây dẫn chuyển sang điện cực Cu) chuyển thành Cu bám lên điện cực Cu. |
Xem thêm các chương trình khác:
- Soạn văn 12 Cánh diều (hay nhất)
- Văn mẫu 12 - Cánh diều
- Tóm tắt tác phẩm Ngữ văn 12 – Cánh diều
- Tác giả tác phẩm Ngữ văn 12 - Cánh diều
- Bố cục tác phẩm Ngữ văn 12 – Cánh diều
- Nội dung chính tác phẩm Ngữ văn 12 – Cánh diều
- Giải sgk Toán 12 – Cánh diều
- Giải Chuyên đề học tập Toán 12 – Cánh diều
- Lý thuyết Toán 12 – Cánh diều
- Giải sbt Toán 12 – Cánh diều
- Giải sgk Tiếng Anh 12 - ilearn Smart World
- Trọn bộ Từ vựng Tiếng Anh lớp 12 ilearn Smart World đầy đủ nhất
- Trọn bộ Ngữ pháp Tiếng Anh lớp 12 ilearn Smart World đầy đủ nhất
- Giải sbt Tiếng Anh 12 – iLearn Smart World
- Giải sgk Vật lí 12 – Cánh diều
- Giải Chuyên đề học tập Vật lí 12 – Cánh diều
- Lý thuyết Vật lí 12 – Cánh diều
- Giải sbt Vật lí 12 – Cánh diều
- Giải sgk Sinh học 12 – Cánh diều
- Giải Chuyên đề học tập Sinh học 12 – Cánh diều
- Lý thuyết Sinh học 12 – Cánh diều
- Giải sbt Sinh học 12 – Cánh diều
- Giải sgk Lịch sử 12 – Cánh diều
- Giải Chuyên đề học tập Lịch sử 12 – Cánh diều
- Giải sbt Lịch sử 12 – Cánh diều
- Giải sgk Địa lí 12 – Cánh diều
- Giải Chuyên đề học tập Địa lí 12 – Cánh diều
- Giải sbt Địa lí 12 – Cánh diều
- Giải sgk Tin học 12 – Cánh diều
- Giải Chuyên đề học tập Tin học 12 – Cánh diều
- Giải sbt Tin học 12 – Cánh diều
- Lý thuyết Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 – Cánh diều
- Giải sgk Kinh tế pháp luật 12 – Cánh diều
- Giải Chuyên đề học tập Kinh tế pháp luật 12 – Cánh diều
- Giải sbt Kinh tế pháp luật 12 – Cánh diều
- Giải sgk Giáo dục quốc phòng 12 – Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 – Cánh diều